Гиперосмия в очаге воспаления это
Оглавление темы «Изменения клеток при воспалении.»:
1. Изменение клеток при воспалении. Изменение морфологии и обмена веществ при воспалении.
2. Метаболизм углеводов при воспалении. Нарушение обмена углеводов при воспалении.
3. Метаболизм липидов при воспалении. Нарушение обмена липидов при воспалении.
4. Метаболизм белков при воспалении. Нарушение обмена белков при воспалении.
5. Метаболизм ионов и воды при воспалении. Нарушение обмена ионов и воды при воспалении.
6. Физико-химические изменения в очаге воспаления. Ацидоз.
7. Гиперосмия в очаге воспаления. Гиперонкия в очаге воспаления.
8. Изменение поверхностного натяжения мембран в очаге воспаления. Изменения коллоидного состояния цитозоля в очаге воспаления.
9. Медиаторы воспаления. Виды медиаторов воспаления.
10. Биогенные амины. Серотонин. Адреналин. Норадреналин.
В очаге воспаления в большей или меньшей мере повышается осмотическое давление.
Причины гиперосмии в очаге воспаления
• Повышенное ферментативное и неферментное разрушение макромолекул (гликогена, гликозаминогликанов, протеогликанов и др.).
• Усиленный в условиях ацидоза гидролиз солей и соединений, содержащих неорганические вещества.
• Поступление осмотически активных соединений из повреждённых и разрушенных клеток.
Последствия гиперосмии в очаге воспаления
• Гипергидратация очага воспаления.
• Повышение проницаемости сосудистых стенок.
• Стимуляция эмиграции лейкоцитов.
• Изменение тонуса стенок сосудов и кровообращения в очаге воспаления.
• Формирование чувства боли.

Гиперонкия в очаге воспаления
Увеличение онкотического давления в воспалённой ткани — закономерный феномен.
Причины гиперонкии в очаге воспаления
• Увеличение концентрации белка в очаге воспаления в связи с усилением ферментативного и неферментного гидролиза пептидов.
• Повышение гидрофильности белковых мицелл и других коллоидов в результате изменения их конформации при взаимодействии с ионами.
• Выход белков (в основном альбуминов) из крови в очаг воспаления в связи с повышением проницаемости стенок микрососудов.
Последствия гиперонкии в очаге воспаления
Основное: развитие отёка в очаге воспаления.
Заряд и электрические потенциалы
Альтерация тканей при воспалении ведёт к нарушениям электрофизиологаческих процессов в клетках: изменению (как правило, снижению) поверхностного их заряда, а также к расстройствам электрогенеза в возбудимых клетках.
Причины нарушения электрофизиологаческих процессов в клетках
• Повреждение клеточных мембран.
• Нарушение энергообеспечения трансмембранного переноса ионов.
• Нарушения ионного баланса во внеклеточной жидкости. Последствия
• Изменение порога возбудимости клеток.
• Колебание чувствительности клеток к действию БАБ (цитокинов, гормонов, нейромедиаторов и др.).
• Потенцирование миграции фагоцитов за счёт электрокинеза.
• Стимуляция кооперации клеток в связи со снижением величины отрицательного поверхностного их заряда, нейтрализацией его или даже перезарядкой (у повреждённых и погибших клеток внешняя поверхность цитолеммы заряжена положительно в связи с избытком на ней К+, Н+ и других катионов).
— Читать далее «Изменение поверхностного натяжения мембран в очаге воспаления. Изменения коллоидного состояния цитозоля в очаге воспаления.»
Альтерационные процессы, нарушение обмена веществ и кровообращения в очагах воспаления вызывают ряд физико-химических изменений – ацидоз, гипертонию, дистонию, гиперосмию, гиперонкию и гипертермию.
Ацидоз
Ацидоз (H hiperjonija) очаг воспаления, возникающий в результате увеличения количества молочной и кетоновых кислот, плохо насыщенных кислородом промежуточных продуктов цикла Кребса (яблочная, янтарная и т. д.) и аминокислот. Первоначально буферная система ткани и воспалительный экссудат нейтрализуют кислотные соединения, образующиеся в тканевом метаболизме, и pH ткани не снижается – ацидоз компенсируется. Декомпенсированный ацидоз возникает при истощении буферной системы. PH экссудата снижается.
Ацидоз и алкалоз
Чем острее воспаление, тем сильнее выражен ацидоз. Особенно тяжелый ацидоз возникает при гнойном воспалении. В условиях хронического воспаления pH ткани обычно не опускается ниже 6,5 единиц, в то время как pH при остром гнойном абсцессе может упасть до 5,3. Наиболее выражен ацидоз в центре воспалительного очага, где он усиливает повреждение (альтерацию).
Альтерация
До выделения биологически активных веществ изменения связаны только с ацидозом. Слабый ацидоз на периферии очага воспаления стимулирует пролиферацию. Следовательно, разрастание ткани происходит в направлении от периферии очага воспаления к центру. Этот пример показывает, что один и тот же фактор может работать двумя способами.
Гипериония и дизиония
Наряду с разрастанием ионов водорода в воспалительных очагах увеличивается количество ионов натрия, кальция и хлора, а в результате повреждения клеток – количество ионов калия и анионов фосфорной кислоты. В нормальных тканях концентрация ионов К не превышает 20 мг%, но в гнойном экссудате может достигать 100-200 мг%. Отношение K:Na к K:Ca увеличивается. Дизион в основном проявляется увеличением количества ионов К в воспалительной жидкости и крови, оттекающей от места воспаления.
Гиперосмия (осмотическая гипертензия)
Концентрация ионов в очаге воспаления увеличивается, в том числе при усилении диссоциации солей. Кроме того, в результате активных ферментативных процессов большие молекулы распадаются на более мелкие и концентрация молекул увеличивается. В процессе интенсивного гликолиза, липолиза и главным образом протеолиза выделяется:
- много аминокислот;
- органических кислот цикла Кребса;
- жирных кислот;
- молочной кислоты.
Концентрация молекул увеличивается в основном за счет аминокислот – когда одна молекула белка (аминокислотного полимера) разрушается, высвобождается много молекул аминокислот. В результате осмотическое давление в очагах воспаления резко повышается – в нормальных тканях оно составляет 7-8 атмосфер, но очаги воспаления могут увеличиваться вдвое и более.
Кроме того, наибольшее осмотическое давление находится в центре воспалительного процесса. Гиперосмии тканей играют важную роль в развитии экссудации и боли.
Гиперонкия
Повышение коллоидосмотического давления вызывается увеличением количества мелкодисперсных белков в тканях. В то же время белки плазмы, в основном альбумины, попадают в ткани из сосудов с повышенной проницаемостью стенки.
Онкотическое давление низкое (всего около 1% от осмотического), но оно играет важную роль в обмене жидкости между кровеносными сосудами и тканями – обычно белки плазмы не проходят через стенку сосудов и удерживают жидкость в крови.
При ацидозе гидрофильность белков тканей увеличивается, и они набухают. Экссудация вызывает местный воспалительный отек. Развивается один из основных местных признаков воспаления – опухоль. Отек опухших тканей вызывает боль.
Отек и боль
Гипертермия
Вызывает один из характерных признаков воспаления – жар. Если воспаление развивается на поверхности тела, например на коже, повышение температуры происходит главным образом из-за артериальной гиперемии. Гораздо более теплая артериальная кровь поступает в относительно низкотемпературную область тела. Однако температура тканей также повышается, когда воспаление локализуется на большой глубине, например, во внутренних органах.
Причиной локальной гипертермии считается разделение процессов биологического окисления и окислительного фосфорилирования. В результате энергия не накапливается в АТФ, а выделяется в виде тепла.
Роль нервной и эндокринной систем в развитии воспаления
Регуляторная роль нервной системы проявляется на всех стадиях воспаления. Например, воспалительная гиперемия и экссудация могут быть вызваны у человека, при убеждении, что монета, помещенная на кожу, горячая, хотя на самом деле монета холодная.
Анестезия тормозит развитие воспаления, но местная анестезия способствует созреванию очагов гноя. Состояние вегетативной нервной системы считается важным в развитии воспаления, однако воспаление также возникает в полностью денервированных тканях. Нарушения микроциркуляции в очаге воспаления возникают в результате локальных нервных процессов (аксональный рефлекс) и гуморальных влияний.
На развитие воспаления значительное влияние оказывают гормоны коры надпочечников. Поэтому кортикоиды дезоксикортикостерон и альдостерон также называют воспалительными гормонами. В фазе воспалительной гипергидратации они увеличивают проницаемость сосудистой стенки и более позднюю пролиферацию. Во время фазы гипогидратации обычно увеличивается выработка адренокортикотропного гормона и глюкокортикоидов.
Глюкокортикоиды (кортизон, гидрокортизон) – это так называемые противовоспалительные гормоны. Кортизон снижает активность гистидиндекарбоксилазы и увеличивает активность гистамина, тем самым снижая уровень гистамина. Одновременно снижается активность 5-окситриптаминдекарбоксилазы и, как следствие, продукция серотонина. В результате снижается проницаемость сосудистой стенки, подавляется гиперемия и экссудация.
Глюкокортикоиды
Из-за ингибирующего действия глюкокортикоидов на ферментные системы снижается энергетический потенциал клеток, деление и подвижность клеток (эмиграция лейкоцитов и фагоцитоз). Глюкокортикоиды стабилизируют лизосомные мембраны и инактивируют кислую фосфатазу, рибонуклеазу и другие ферменты. Глюкокортикоиды подавляют не только воспаление, но и защитные реакции организма – экссудацию, эмиграцию лейкоцитов, фагоцитоз, пролиферацию и образование антител.
Другие гормоны также влияют на течение воспаления. Давно известно, что воспаление активно у пациентов с гипертиреозом и инертно у пациентов с микседемой.
Инсулин регулирует не только углеводный обмен, но и метаболизм белков. При отсутствии инсулина сопротивляемость организма инфекционным агентам снижается, и воспаление протекает гораздо тяжелее. Фурункулез часто встречается у диабетиков.
Эстрогенные половые гормоны подавляют активность гиалуронидазы и течение воспаления.
Продолжение статьи
- Часть 1. Этиология и патогенез воспаления. Классификация.
- Часть 2. Особенности обмена веществ при воспалении.
- Часть 3. Физико – химические изменения. Роль нервной и эндокринной систем в развитии воспаления.
- Часть 4. Изменения в периферическом кровообращении при воспалении.
- Часть 5. Экссудация. Экссудат и транссудат.
- Часть 6. Эмиграция лейкоцитов. Хемотаксис.
- Часть 7. Фагоцитоз. Асептическое и острое воспаление.
- Часть 8. Распространение. Последствия. Принципы лечения воспаления.
Поделиться ссылкой:
Этиология воспаления
Любой этиологический фактор, вызывающий развитие воспаления, называется флогогенным фактором. К флогогенным факторам относятся:
1. Факторы физического происхождения: механические (травма), температуры, ионизирующая радиация, УФ и т.д.
2. Химические факторы: кислоты, щелочи, соли тяжелых металлов, фенолы, альдегиды, метаболиты.
3. Биологические агенты: вирусы, бактерии, простейшие и т.д.
По отношению к организму флогогенные агенты могут быть экзогенными и эндогенными.
Патогенез воспаления
В патогенезе воспаления различают три сосуществующих компонента:
1. Альтерация.
2. Нарушения микроциркуляции с явлениями экссудации и эмиграции.
3. Пролиферация.
Особенность: как правило, сосуществуя вместе, три компонента воспаления выражаются на разных этапах воспалительной реакции по-разному.
Альтерация — это повреждение тканей в процессе воспаления. В основе альтерации лежат 2 группы явлений:
1. Повреждение клеток и внеклеточных структур
2. Образование медиаторов воспаления
Выделяют первичную и вторичную альтерацию.
Первичная альтерация – это повреждение ткани, возникающее вследствие непосредственного действия флогогенных агентов. По степени выраженности первичная альтерация слабее вторичной.
Вторичная альтерация – это повреждения ткани, возникающие в результате повреждения тканей, которые образовались вследствие первичной альтерации. Факторы, вызывающие развитие вторичной альтерации:
1. Медиаторы воспаления: лизосомальные факторы, активированный комплемент, лимфокины, лимфотоксины
2. Свободные радикалы и пероксиды
3. Гипоксия в результате местных расстройств кровообращения
4. Местный ацидоз
5. Повышение осмотического и онкотического давления в очаге воспаления
Местный ацидоз в очаге воспаления делится на первичный и вторичный.
Первичный ацидоз возникает в первые тридцать минут вследствие деполимеризации основного межуточного вещества и освобождения карбоксильных и сульфатных групп.
Вторичный ацидоз обусловлен нарушениями обмена веществ в очаге воспаления. К нему приводят: накопление молочной кислоты, накопление недоокисленных продуктов цикла Кребса, освобождение свободных жирных кислот, аминокислот, фосфорной кислоты, в результате расщепления триглицеридов, фосфолипидов, АТФ.
Гиперонкия и гиперосмия в очаге воспаления
Увеличение осмотического давления в очаге воспаления связано с выходом ионов калия из поврежденных клеток. Увеличение онкотического давления (гиперонкия) обусловлена:
1. Поступлением белков в ткань из крови в процессе экссудации (плазменный источник);
2. Расщеплением больших белковых молекул на более мелкие под действием лизосомальных ферментов (тканевой источник);
3. В результате имеем гиперосмию и гиперонкию.
Гипоксия и «пожар обмена» в очаге воспаления: при воспалении всегда имеет место нарушение обмена веществ. В остром периоде воспаления преобладают процессы распада – катаболизма. Происходит увеличение интенсивности потребления кислорода и активация процессов гликолиза. Под действием лизосомальных ферментов крупные молекулы расщепляются на мелкие, все это характеризуют термином «пожар обмена». Аналогия состоит не только в том, что обмен в очаге воспаления резко повышен, но и в том, что обмен идет с образованием недоокисленных продуктов, поэтому в очаге воспаления будет иметь место гипоксия и ацидоз. В дальнейшем активируются анаболические процессы и начинается размножение клеток, в первую очередь, СТ.
Медиаторы воспаления
Это БАВ, которые образуются в очаге воспаления и определяют его патогенез. Различают медиаторы:
1. клеточного происхождения- образуются в клетках
2. плазменного происхождения – образуются и поступают из плазмы
Наибольшее значение имеют следующие медиаторы воспаления:
1. Лизосомальные факторы
2. Продукты дегрануляции тканевых базофилов
3. Кинины
4. Лимфокины и монокины
5. Продукты арахидоновой кислоты
6. Продукты активации комплимента
7. Продукты свертывающей и фибринолитической систем.
Лизосомальные факторы
К ним относятся лизосомальные ферменты (гидролазы), неферментные катионные белки, свободные радикалы и пероксиды. Роль лизосомальных ферментов:
1. вызывают вторичную альтерацию
2. принимают участие в образовании и активации других медиаторов воспаления
3. непосредственно повышают проницаемость капилляров
4. вызывают развитие физико-химических и метаболических изменений в очаге воспаления.
Это приводит к ацидозу и гиперонкии.
Тканевые базофилы
При дегрануляции тканевых базофилов выделяются БАВ, важнейшими из которых являются гистамин и серотонин. Эти вещества:
1. расширяют артериолы, вызывая развитие артериальной гиперемии
2. повышают проницаемость стенки сосудов на уровне венул, вызывая экссудацию и эмиграцию
3. раздражают нервные окончания – боль.
Лимфокины и монокины
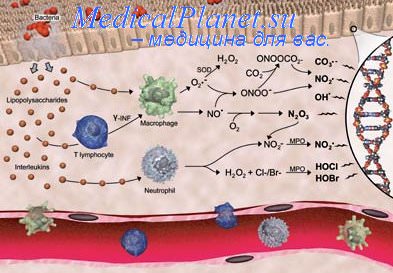
Лимфокины — это продукции деятельности Т-лимфоцитов, которые вызывают активацию хемотаксиса лейкоцитов и активируют пролиферацию в очаге воспаления. Монокины являются продуктами деятельности макрофагов. Основной монокин – это интерлейкин-1. Он вызывает лихорадку, боль, а воздействую на ЦНС – апатию и сонливость.
В результате выработки БАВ, а также нарушения обмена веществ, в исходе альтерации закладывается фундамент для развития экссудации, эмиграции и пролиферации.
Альтерация приводит к нарушению местного кровообращения в очаге воспаления. Механизм и проявления этих нарушений следующие:
1. Кратковременная ишемия
2. Артериальная гиперемия
3. Венозная гиперемия
4. Стаз
Из-за нарушения микроциркуляции наблюдается резкое повышение сосудистой стенки, застой крови, накопление хемотаксинов. Это создает благоприятные условия для развития второго компонента воспаления – экссудации.
Экссудация
Это выход жидкости и растворенных в ней компонентов плазмы крови из кровеносных сосудов в ткань. В широком смысле слова это понятии включает и эмиграцию лейкоцитов. В основе экссудации лежать три механизма:
1. Повышение проницаемости сосудистой стенки
2. Увеличение гидростатического давления в сосудах
3. Увеличение осмотического и онкотического давления в ткани.
Ведущим фактором в развитие экссудации является повышение проницаемости сосудистой стенки.
Этиология повышения проницаемости сосудистой стенки: продукты дегрануляции базофилов, кинины (брадикинин и калледин), простагландины и лейкотриены, лизосомальные ферменты, ацидоз.
Механизм повышения проницаемости сосудистой стенки при экссудации:
1. Активация микровезикулярного транспорта через эндотелий
2. Образование сквозных трансклеточных каналов в эндотелиоцитоах
3. Увеличение просвета межэндотелиальных щелей
4. Десквамация (слущивание) эндотелия
5. Деполимеризация веществ, соединяющих эндотелиоциты сосудов
Эмиграция
Это переход лейкоцитов крови из кровеносных сосудов в ткань. Вначале выходят полинуклеарные фагоциты – нейтрофилы. Они уничтожают микробы. Затем, мононуклеарные фагоциты. Они фагоцитируют погибшие клетки, тканевой детрит и расчищают очаг воспаления. На конечном этапе в ткань поступают лимфоциты. Процесс эмиграции лейкоцитов в воспаленную ткань включает следующие процессы:
1. Краевое состояние лейкоцитов – маргинация. Это переход лейкоцитов из циркулирующего пула в пристеночный маргинальный. В основе лежат следующие механизмы: лейкоциты, как наиболее легкие элементы, отбрасываются на периферию. На поверхности эндотелия сосудов происходит выпадение нитей фибрины. Образовавшаяся «бахрома» задерживает лейкоциты. Имеет место электростатическое взаимодействие лейкоцитов с эндотелиоцитами. На поверхности лейкоцитов и эндотелиоцитов появляются адгезивные белки. Адгезивные белки синтезируются в лейкоцитах и эндотелиальных клетках и хранятся во внутриклеточных везикулах. Под действием медиаторов воспаления везикулы открываются и адгезивные белки выходят, что приводит к взаимодействию лейкоцитов и эндотелиоцитов.
2. Преодолевание лейкоцитами сосудистой стенки и эмиграция их в очаг воспаления. Эмигрируя в ткань лейкоциты преодолевают два барьера капиллярной стенки: эндотелий и базальную мембрану. Нейтрофилы и макрофаги проходят через эндотелий по межэндотелиальным щелям, они выпускают псевдоподии в щели и раздвигают клетки. Преодоление базальной мембраны обусловлено двумя механизмами. Первый механизм заключается в явлении тиксотропии: при контакте с базальной мембраной ее коллоиды переходят из состояния геля в состояние золя, то есть разжижаются. Нейтрофил легко преодолевает золь, после чего золь базальной мембраны превращается в гель. Второй механизм заключается в выделении нейтрофилами нейтральных протеаз, которые расщепляют волокнистые структуры базальной мембраны. После этого нейтрофилы, макрофаги и другие лейкоциты благодаря явлению хемотаксиса проникают в очаг воспаления (см. тему «Фагоцитоз»).
Пролиферация
Пролиферация или размножение клеток в очаге воспаления включает два процесса включает два процесса: размножение клеток (собственно пролиферация) и синтез внеклеточных компонентов СТ (коллагена, эластина, протеогликанов, гликопротеинов).
Механизмы пролиферации
I. Уменьшение концентрации в ткани кейлонов.
Это вещества белковой природы, которые образуются зрелыми клетками.
Кейлоны — ингибиторы клеточного деления. Чем выше их концентрация, тем меньше развиты в ткани процессы пролиферации.При повреждении и гибели клеток в очаге воспаления концентрации кейлонов в ткани уменьшается и снимается тормозное влияние кейлонов на малодифференцированные камбиальные клетки: они начинают делиться. Деление продолжается до тех пор, пока концентрация кейлонов не увеличиться до уровня, который существовал в неповрежденной ткани.
II. Увеличение концентрации в тканях стимуляторов пролиферации – факторов роста.
Факторы роста поступают из плазмы или являются продуктами клеток. Это фактор роста эпидермиса, фактор роста фибробластов, фактор роста тромбоцитарного происхождения, фактор роста нервов, фактор некроза опухолей, соматомедины (инсулиноподобные факторы роста), лимфокины. Интимный механизм их действия заключается в активации внутриклеточных протеинкиназ. В итоге в очаге воспаления размножаются клеточные элементы (в первую очередь СТ) и формируется волокнистая СТ.
Пентада Цельса-Галена
(кардинальные признаки воспаления или местные клинические признаки воспаления).
1. Calor – повышение местной температуры воспаленного очага
Обусловлено повышение интенсивности катаболических процессов в очаге воспаления, а также артериалной гиперемией, во время которой в ткань поступает много теплой артериальной крови.
2. Rubor – покраснение воспалительного очага. Связано с развитием артериальной, а затем, венозной гиперемией.
3. Tumor – припухание воспаленного очага. Развивается в результате экссудации.
4. Dolor – боль в области воспаленного очага. Возникает в результате раздражения рецепторов медиаторами воспаления, а также в результате механического давления экссудата, ацидоза и гиперосмии.
5. Functio Laesa – нарушение функции. Является следствием гибели клеток в очаге воспаления.
Общие проявления воспаления
1. Лихорадка: развивается вследствие выделения нейтрофилами и макрофагами лейкоцитарных пирогенов, в первую очередь ИЛ-1.
2. Лейкоцитоз: при остром воспалении, вызванном гноеродными микроорганизмами, наблюдается нейтрофилез, то есть увеличение нейтрофилов. Также может увеличиваться количество лимфоцитов, эозинофилов и других лейкоцитов.
3. Повышенное содержание в крови «белков острой фазы воспаления». Это белки, концентрация которых в плазме крови при остром воспалении увеличивается более чем на 50% процентов. Они образуются в основном в печени под влиянием продуктов альтерации, ИЛ-1. Известно более 10 белков острой фазы воспаления. Все они имеют в основном защитное значение. К ним относятся: ингибиторы протеаз, антиоксиданты, иммуноглобулины и антителоподобные вещества.
4. Увеличение СОЭ: связано с увеличением содержания в плазме крови грубодисперсных белков (глобулинов, фибриногена). В результате этого поверхностный заряд эритроцитов уменьшается и они легко агрегируют.
5. Интоксикация: обусловлена поступлением в кровь продуктов альтерации из воспаленной ткани.
Классификация воспаления
I . По течению:
1. острое
2. хроническое
II . По степени выраженности, проявлению, манифестации:
1. нормергическое
2. гиперергическое
3. гипоергическое
Диалектика воспаления
С одной стороны воспаление является защитно-приспособительной реакцией, с другой – типичным патологическим процессом. Этим объясняется двойственность воспаления. Защитное значение при воспалении имеют: эмиграция лейкоцитов, уничтожение флогогенных ферментов, активация процессов репарации поврежденных тканей, общие реакции организма, направленные на повышение его резистентности (лихорадка, лейкоцитоз, увеличение содержания белков острой фазы воспаления).
Патологическими явлениями при воспалении являются первичная и вторичная альтерация, отек, боль, нарушение функции, физико-химические изменения и нарушения обмена веществ в очаге воспаления. Иногда одно и то же проявление воспаления имеет как патологическую, так и защитную стороны.
Особенность: учитывая двойственность воспаления, ветеринарный врач при лечении воспалительного процесса должен направлять свои усилия на борьбу с собственно патологическими явлениями и усиливать защитно-компенсаторные явления.
Этиология воспаления
Любой этиологический фактор, вызывающий развитие воспаления, называется флогогенным фактором. К флогогенным факторам относятся:
1. Факторы физического происхождения: механические (травма), температуры, ионизирующая радиация, УФ и т.д.
2. Химические факторы: кислоты, щелочи, соли тяжелых металлов, фенолы, альдегиды, метаболиты.
3. Биологические агенты: вирусы, бактерии, простейшие и т.д.
По отношению к организму флогогенные агенты могут быть экзогенными и эндогенными.
Патогенез воспаления
В патогенезе воспаления различают три сосуществующих компонента:
1. Альтерация.
2. Нарушения микроциркуляции с явлениями экссудации и эмиграции.
3. Пролиферация.
Особенность: как правило, сосуществуя вместе, три компонента воспаления выражаются на разных этапах воспалительной реакции по-разному.
Альтерация — это повреждение тканей в процессе воспаления. В основе альтерации лежат 2 группы явлений:
1. Повреждение клеток и внеклеточных структур
2. Образование медиаторов воспаления
Выделяют первичную и вторичную альтерацию.
Первичная альтерация – это повреждение ткани, возникающее вследствие непосредственного действия флогогенных агентов. По степени выраженности первичная альтерация слабее вторичной.
Вторичная альтерация – это повреждения ткани, возникающие в результате повреждения тканей, которые образовались вследствие первичной альтерации. Факторы, вызывающие развитие вторичной альтерации:
1. Медиаторы воспаления: лизосомальные факторы, активированный комплемент, лимфокины, лимфотоксины
2. Свободные радикалы и пероксиды
3. Гипоксия в результате местных расстройств кровообращения
4. Местный ацидоз
5. Повышение осмотического и онкотического давления в очаге воспаления
Местный ацидоз в очаге воспаления делится на первичный и вторичный.
Первичный ацидоз возникает в первые тридцать минут вследствие деполимеризации основного межуточного вещества и освобождения карбоксильных и сульфатных групп.
Вторичный ацидоз обусловлен нарушениями обмена веществ в очаге воспаления. К нему приводят: накопление молочной кислоты, накопление недоокисленных продуктов цикла Кребса, освобождение свободных жирных кислот, аминокислот, фосфорной кислоты, в результате расщепления триглицеридов, фосфолипидов, АТФ.
Гиперонкия и гиперосмия в очаге воспаления
Увеличение осмотического давления в очаге воспаления связано с выходом ионов калия из поврежденных клеток. Увеличение онкотического давления (гиперонкия) обусловлена:
1. Поступлением белков в ткань из крови в процессе экссудации (плазменный источник);
2. Расщеплением больших белковых молекул на более мелкие под действием лизосомальных ферментов (тканевой источник);
3. В результате имеем гиперосмию и гиперонкию.
Гипоксия и «пожар обмена» в очаге воспаления: при воспалении всегда имеет место нарушение обмена веществ. В остром периоде воспаления преобладают процессы распада – катаболизма. Происходит увеличение интенсивности потребления кислорода и активация процессов гликолиза. Под действием лизосомальных ферментов крупные молекулы расщепляются на мелкие, все это характеризуют термином «пожар обмена». Аналогия состоит не только в том, что обмен в очаге воспаления резко повышен, но и в том, что обмен идет с образованием недоокисленных продуктов, поэтому в очаге воспаления будет иметь место гипоксия и ацидоз. В дальнейшем активируются анаболические процессы и начинается размножение клеток, в первую очередь, СТ.
Медиаторы воспаления
Это БАВ, которые образуются в очаге воспаления и определяют его патогенез. Различают медиаторы:
1. клеточного происхождения- образуются в клетках
2. плазменного происхождения – образуются и поступают из плазмы
Наибольшее значение имеют следующие медиаторы воспаления:
1. Лизосомальные факторы
2. Продукты дегрануляции тканевых базофилов
3. Кинины
4. Лимфокины и монокины
5. Продукты арахидоновой кислоты
6. Продукты активации комплимента
7. Продукты свертывающей и фибринолитической систем.
Лизосомальные факторы
К ним относятся лизосомальные ферменты (гидролазы), неферментные катионные белки, свободные радикалы и пероксиды. Роль лизосомальных ферментов:
1. вызывают вторичную альтерацию
2. принимают участие в образовании и активации других медиаторов воспаления
3. непосредственно повышают проницаемость капилляров
4. вызывают развитие физико-химических и метаболических изменений в очаге воспаления.
Это приводит к ацидозу и гиперонкии.
Тканевые базофилы
При дегрануляции тканевых базофилов выделяются БАВ, важнейшими из которых являются гистамин и серотонин. Эти вещества:
1. расширяют артериолы, вызывая развитие артериальной гиперемии
2. повышают проницаемость стенки сосудов на уровне венул, вызывая экссудацию и эмиграцию
3. раздражают нервные окончания – боль.
