Хроническое воспаление и цитокины

Текущая версия страницы пока не проверялась опытными участниками и может значительно отличаться от версии, проверенной 9 июля 2019;
проверки требуют 4 правки.
Цитокины — небольшие пептидные информационные молекулы.
Цитокины имеют молекулярную массу, не превышающую 30 кD.
Цитокин выделяется на поверхность клетки А и взаимодействует с рецептором находящейся рядом клетки В. Таким образом, от клетки А к клетке В передается сигнал, который запускает в клетке В дальнейшие реакции.
Их основными продуцентами являются лимфоциты.
Кроме лимфоцитов их секретируют макрофаги, гранулоциты, ретикулярные фибробласты, эндотелиальные клетки и другие типы клеток.
Они регулируют межклеточные и межсистемные взаимодействия, определяют выживаемость клеток, стимуляцию или подавление их роста, дифференциацию, функциональную активность и апоптоз, а также обеспечивают согласованность действия иммунной, эндокринной и нервной систем в нормальных условиях и в ответ на патологические воздействия.
Термин предложен Стэнли Коэном (англ. S. Cohen) в 1974 г.[1]
Цитокины активны в очень малых концентрациях. Их биологический эффект на клетки реализуется через взаимодействие со специфическим рецептором, локализованным на клеточной цитоплазматической мембране. Образование и секреция цитокинов происходит кратковременно и строго регулируется.
Все цитокины, а их в настоящее время известно более 30, по структурным особенностям и биологическому действию делятся на несколько самостоятельных групп. Группировка цитокинов по механизму действия позволяет разделить цитокины на следующие группы:
- провоспалительные, обеспечивающие мобилизацию воспалительного ответа (интерлейкины 1,2,6,8, ФНОα, интерферон γ);
- противовоспалительные, ограничивающие развитие воспаления (интерлейкины 4,10, TGFβ);
- регуляторы клеточного и гуморального иммунитета — (естественного или специфического), обладающие собственными эффекторными функциями (противовирусными, цитотоксическими).
Спектры биологических активностей цитокинов в значительной степени перекрываются: один и тот же процесс может стимулироваться в клетке более чем одним цитокином. Во многих случаях в действиях цитокинов наблюдается синергизм. Цитокины — антигеннеспецифические факторы, поэтому специфическая диагностика инфекционных, аутоиммунных и аллергических заболеваний с помощью определения уровня цитокинов невозможна. Но определение их концентрации в крови даёт информацию о функциональной активности различных типов иммунокомпетентных клеток; о тяжести воспалительного процесса, его переходе на системный уровень и о прогнозе заболевания.
Цитокины регулируют активность гормональной оси гипоталамус-гипофиз-надпочечники:[2] например, Интерлейкин 1, воздействуя на гипоталамус, усиливает синтез кортиколиберина, что, в свою очередь, повышает выработку АКТГ.
См. также[править | править код]
- Фактор некроза опухоли (ФНО, англ. TNF)
- Фактор переноса
- Остеопонтин
Примечания[править | править код]
Ссылки[править | править код]
- Научно-практический журнал «Цитокины и Воспаление»
- Цитокины — причина парадонтита (недоступная ссылка)
- Все о цитокинах — Иммунинфо
Сюжет Пандемия коронавируса нового типа, распространившегося из Китая
Самыми распространенными осложнениями и причинами смерти при COVID-19 являются тяжелая пневмония, синдром острого респираторного дистресса (поражения), сепсис, полиорганная недостаточность (отказ функционирования многих органов), острое поражение почек или сердца. Кроме этого, ответ иммунной системы организма может привести к цитокиновому шторму и, как следствие, смертельному исходу.
Что такое цитокины и цитокиновый шторм?
Цитокиновый шторм (цитокиновый каскад, гиперцитокинемия) — это неконтролируемое воспаление, которое приводит к повреждению собственных тканей организма. В борьбе с вирусом иммунные клетки выделяют особые вещества — цитокины. Это низкомолекулярные белки активированных клеток иммунной системы, которые обеспечивают межклеточные взаимодействия. К цитокинам, в частности, относятся интерфероны, интерлейкины, хемокины, факторы некроза опухоли и т. д. Сегодня ученым известно более ста цитокинов.
Цитокины. Фото: Commons.wikimedia.org
Эти белки действуют по эстафетному принципу: воздействие цитокина на клетку вызывает образование ею других цитокинов, если реакция иммунной системы очень бурная, возникает так называемый цитокиновый шторм: активированные иммунные клетки вырабатывают все новые и новые порции этих белков.
Из всех инфекционных заболеваний особенно часто наблюдения цитокинового шторма встречаются при гриппе.
Что происходит в результате цитокинового шторма?
Сначала вирус массово поражает клетки, в которые способен проникнуть, размножается в них, затем выходит из клеток и распространяется дальше. Клетки при этом погибают, и в ответ на это включается защитная реакция иммунной системы, которая выражается в чрезмерном выделении цитокинов и неконтролируемом воспалении.
Во время цитокинового шторма ткани очага воспаления разрушаются, иммунная система начинает работать на предельной мощности, чтобы побороть инфекцию, и в результате воспаление распространяется на соседние ткани. Со временем цитокиновый шторм охватывает весь организм, и все может закончиться смертью пациента.
Какие признаки цитокинового шторма?
Состояние, называемое цитокиновым штормом, проявляется лихорадкой, рвотой, диареей, слабостью, болями в различных частях тела и снижением уровня кислорода в крови. В анализах можно увидеть цитопению (снижение количества клеток), лимфопению (снижение количества лимфоцитов), повышенный уровень ферритина.

У больных COVID-19 в таком состоянии отмечается высокий уровень интерлейкина-2 (IL), фактора некроза опухолей альфа (TNF-α). В половине случаев происходит поражение легких, поэтому необходима искусственная вентиляция легких, а также терапия сепсиса и регулирование выброса цитокинов.
Можно ли остановить цитокиновый шторм?
Цитокиновый шторм можно остановить только в условиях клиники, но это удается сделать не всегда. Во время выработки огромного количества цитокинов может возникнуть полиорганная недостаточность и, как следствие, смерть пациента. Гиперцитокинемия является одной из причин смертей во время гриппа, цитокиновым штормом ряд ученых объясняет, в частности, большое количество жертв среди молодых людей во время эпидемии «испанки» — пандемии гриппа 1918 года.
Как показывают результаты исследований, необходимо вовремя определять время начала такого шторма, а сделать это возможно исключительно при помощи анализа крови. В условиях нынешней пандемии коронавируса медики применяют различные препараты, в частности, тоцилизумаб и гидроксихлорохин (иммунодепрессанты), которые имеют свойство приглушать активность специфических цитокинов.
Оставить
комментарий (0)
Основные статьи: Цитокины, Воспаление
Действие цитокинов лишь на начальном этапе воспаления ограничивается очагом, а позже распространяется на весь организм (генерализуется). Одновременно реализуется множество механизмов, способствующих недопущению генерализации инфекционного агента.
Принципиально важным свойством макрофага является синтез мощных провоспалительных цитокинов (в первую очередь, ФНО-α, ИЛ-1β, ИЛ-6), которые, с одной стороны, поддерживают развитие воспалительной реакции, а с другой — активируют иммунокомпетентные клетки, готовя их к предстоящей антигенной презентации. Именно с высвобождением макрофагальных цитокинов связаны метаболические перестройки при воспалении и возникновение симптомов интоксикации.
Самым мощным цитокином этой группы является фактор некроза опухоли α (ФНО-α). Он выполняет ряд важнейших функций:
- стимулирует фагоцитоз и продукцию свободных радикалов фагоцитами;
- усиливает экспрессию адгезионных молекул эндотелием (например, Е-селектина, ICAM-1);
- является хемоаттрактантом для макрофагов и клеток Лангерганса;
- увеличивает продукцию гепатоцитами белков острой фазы;
- активирует липопротеинлипазу, способствуя тем самым мобилизации липидов из депо;
- действует на терморегуляторный центр (через высвобождение ПГЕ2), повышая температуру тела.
Кроме этого, ФНО-α способен самостоятельно индуцировать апоптоз скомпрометированных клеток путем взаимодействия с мембранным белком р55 (отсюда и не совсем правильное название данного цитокина).
Функции фактора некроза опухоли α частично перекрываются ИЛ-1β и ИЛ-6, поэтому тандем этих цитокинов практически неразрывно действует в очаге воспаления.
Так, интерлейкин-1β (ИЛ-1β) стимулирует Т-лимфоциты и повышает синтез ими интерлейкина-2 (ИЛ-2) и экспрессию рецептора к ИЛ-2. При действии ИЛ-1β преактивированные В-лимфоциты усиливают пролиферацию, а также экспрессию поверхностных молекул HLA II и рецепторов к ИЛ-2.
Эндотелиоциты под влиянием ИЛ-1β усиливают экспрессию молекул адгезии, начинают повышенный синтез простациклина, с чем связана вазодилатация и повышение сосудистой проницаемости.
ИЛ-1β вызывает выброс биогенных аминов, в первую очередь гистамина из тучных клеток. В костной, хрящевой и мышечных тканях ИЛ-1β индуцирует синтез протеиназ, что обуславливает развитие остеопороза, резорбции хряща, миомаляции. Данный цитокин также влияет на клетки миелоидного ряда, действуя синергически с ГМ-КСФ. Одновременно угнетается эритропоэз, так как ИЛ-1β является антагонистом эритропоэтина. В табл. 1 перечислены основные эффекты ИЛ-1β.
ИЛ-6 оказывает некоторые контррегуляторные эффекты по отношению к ИЛ-1β и ФНО-α, однако стимулирующее влияние на синтез белков острой фазы гепатоцитами позволяет отнести его к провоспалительным цитокинам.
Мишень | Эффект |
Т-лимфоциты | Повышение синтеза ИЛ-2, увеличение экспрессии рецепторов к ИЛ-2 |
В-лимфоциты | Усиление экспрессии HLA II |
Естественные киллеры Материал с сайта https://wiki-med.com | Повышение экспрессии рецепторов к ИЛ-2 |
Макрофага | Усиление фагоцитоза, продукции свободных радикалов и провоспалительных цитокинов, повышение экспрессии HLA II |
Эндотелиоциты | Повышение экспрессии молекул адгезии и синтеза простациклина |
Тучные клетки | Выброс гистамина |
Естественные киллеры также отвечают на действие ИЛ-1β усилением экспрессии рецептора к ИЛ-2. У макрофагов усиливается фагоцитоз, синтез свободных радикалов, повышается экспрессия молекул HLA II, синтез ФНО-α, ИЛ-6 и самого ИЛ-1β.
 На этой странице материал по темам:
На этой странице материал по темам:
цитокин что это
фно цитокин
опишите цитокиновый ответ
цитокины классификация
цитокины в иммунном ответе
Цитокины, являясь медиаторами межклеточных взаимоотношений, играют Центральную роль в регуляции воспалительного ответа. Цитокиновая сеть представлена множеством протеинов или гликопротеинов, вырабатываемых преимущественно активированными лимфоцитами и моноцитарно-макрофа-гальной системой, а также в меньшей мере фибробластами, эндотелиальными, соматическими клетками, в том числе клетками эндометрия и трофобласта.
Первыми представителями этого класса явились ИФН, впервые описанные в 1957 г. A.Isaacs и J.Lindemann. В 1960-х годах были обнаружены новые белковые регуляторные молекулы, способные управлять процессами активации,
54Глава I
Таблица 1.10 Участие цитокинов в реакции воспаления
| Функция | Цитокин |
| Провоспалительные | ИЛ-ip, ИЛ-6, ИЛ-8, ИЛ-12, ИЛ-18, ФНО-а, ИФН-у |
| Противовоспалительные | ИЛ-4, ИЛ-10, ТФР-р |
| Регуляторные | ИЛ-2, ИЛ-4, ИЛ-5, ИЛ-6, ИЛ-7, ИФН-у, ТФР-р |
пролиферации и дифференцировки лимфоцитов и гемопоэтических клеток. L.A.Aarden в 1979 г. предложил термин «интерлейкин», подчеркивая способность цитокинов служить коммуникационными сигналами для клеток различных популяций лейкоцитов.
Цитокины представляют собой обширное семейство биологически активных пептидов, оказывающих гормоноподобное действие и обеспечивающих взаимодействие клеток иммунной, кроветворной, нервной и эндокринной систем. Цитокины объединяют следующие общие свойства: 1) они служат медиаторами иммунной и воспалительной реакций; 2) проявляют свою активность при концентрациях порядка 10—11 моль/л; 3) действуют как факторы роста и факторы дифференцировки клеток; 4) образуют регуляторную сеть; 5) обладают плейо-тропной активностью и перекрывающимися функциями. Хотя цитокины и называют иногда гормонами иммунной системы, от гормонов их отличает способ передачи сигнала клетке. Так, если гормоны вступают во взаимодействие с цито-зольными рецепторами, которые встраиваются затем в ДНК, то цитокины специфически связываются с поверхностным рецептором, через который происходит передача сигнала внутрь клетки с помощью системы вторичных мессенджеров. Как правило, рецептор для цитокина состоит из нескольких полипептидных цепей. Последние могут отличаться по своей специфичности, аффинности и способности передавать сигнал. Существует два принципиально различных механизма торможения биологической активности цитокинов. Один — быстрый, за счет связывания цитокина растворимыми рецепторами или специфическими антагонистами. Другой механизм торможения (медленный) обеспечивается гормонами (например, глюкокортикоидами) или другими цитокинами, воздействие которых тормозит синтез цитокинов клеткой. В зависимости от выполняемой функции принято различать провоспалительные, противовоспалительные и регуляторные цитокины (табл. 1.10). С учетом такого важного свойства цитокинов, как плейо-тропность, это разделение носит в достаточной мере условный характер.
Одной из важнейших функций системы цитокинов является обеспечение согласованного действия иммунной, эндокринной и нервной систем в развитии реакции воспаления. Так, на месте внедрения инфекции обычно имеет место массивный выброс провоспалительных цитокинов (ИЛ-1в, ИЛ-6, ИЛ-12, ФНО-а). При превышении в крови пороговых концентраций эти цитокины способны преодолевать в преоптической области гематоэнцефалический барьер и стимулировать высвобождение кортикотропин-рилизинг-гормона, который, в свою очередь, стимулирует продукцию АКТГ гипофизом.
Следующим этапом является усиление синтеза кортизола надпочечниками. Одновременно происходит активация симпатической нервной системы, что сопровождается повышенным высвобождением катехоламинов (адреналина и норадреналина). Как глюкокортикоиды, так и катехоламины активно вмешиваются в течение воспалительного процесса. Основными мишенями кортизола и норадреналина являются моноциты/макрофаги и Тh1-лимфоциты. В резуль-
Генитальные инфекции и факторы противоинфекционной защиты в генезе
воспалительных заболеваний женских половых органов 55
тате происходит торможение продукции макрофагами провоспалительных цитокинов и стимулируется синтез противовоспалительного цитокина ИЛ-10. Последний вместе с кортизолом и норадреналином снижает продукцию ИЛ-2 и ИФН-у Тh1-лимфоцитами. Таким образом, активация гипоталамо-гипофи-зарно-надпочечниковой оси (ГГНО) и симпатической нервной системы снижает интенсивность воспалительного процесса, предотвращая тем самым повреждение внутренних органов медиаторами воспаления. Однако в ряде случаев, например при хронической инфекции, подавить реакцию воспаления не удается. В очаг воспаления продолжается рекрутирование лимфоцитов, и синтез цитокинов остается достаточно высоким. Это приводит к формированию порочного круга, при котором равновесие между про- и противовоспалительными цитокинами оказывается нарушенным. При этом противовоспалительные агенты (глюкокортикоиды, катехоламины), не будучи в состоянии ликвидировать очаг воспаления, существенно угнетают Тh1 -лимфоциты, практически не влияя при этом на Тh2-клетки. В результате образовавшегося сдвига в пользу Тh2 имеет место повышение продукции таких цитокинов, как ИЛ-4 и ИЛ-5, которые являются медиаторами синтеза низкоаффинных IgE-антител В-лимфоцитами (Пухальский А.Л., Шмарина Г.В., Капранов Н.И., 2004).
Воспалительный процесс может проявляться в виде как локальных, так и системных изменений, свидетелями которых могут быть различные маркеры воспаления, включая цитокины (Pukhalsky A.L., Shmarina G.V. et al., 2004). Для получения объективной картины патологического процесса при воспалительных заболеваниях женских половых органов необходимо исследовать маркеры воспаления в крови и цервикальной слизи.
Наиболее информативными маркерами воспаления при исследовании цервикальной слизи являются ФНО-а, ИЛ-4, ИФН-у, ИЛ-10 и ТФР-р. Эти показатели не только могут дать представление об интенсивности местного воспалительного процесса, но и укажут на сдвиги равновесия между Тh1- и Тh2-компо-нентами иммунного ответа, а также о преобладании про- или противовоспалительных механизмов его реализации. Однако многие цитокины (ФНО-а и ИЛ-10) могут присутствовать в биологических жидкостях не только в виде свободных биологически активных молекул, но и в связанном виде — в виде комплекса, состоящего из цитокина и его ингибитора. Исходя из этого целесообразно использовать соответствующие диагностические наборы, способные определять как свободный цитокин, так и общий (свободный + связанный). Так, например, обнаружение высокого содержания общего ФНО-а при низком или нулевом содержании свободного цитокина, с одной стороны, свидетельствует об активации клеток — продуцентов ФНО-а, что может быть связано с наличием хронического источника инфекции, а с другой стороны — указывает на активную роль противовоспалительных механизмов. Исследование соотношения между уровнем ИФН-у и ИЛ-4 позволяет судить о развитии иммунного ответа по ТЫ- или Тп2-типу.
Исследование сыворотки крови позволяет судить о наличии системных изменений у данного пациента в условиях наличия локального очага воспаления. При этом, помимо исследования содержания цитокинов, может быть использован метод оценки индивидуальной чувствительности лимфоцитов периферической крови к антипролиферативному действию глюкокортикоид-ных гормонов. Производят определение параметра Ah, который характеризует количество активированных лимфоцитов в кровотоке и может иметь как отрицательное, так и положительное значение (Pukhalsky A.L., Kapranov N.I. et al., 1999; Pukhalsky A.L., Kalashnikova E.A. et al., 1990). Если величина 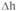 <0, это
<0, это
56 Глава I
свидетельствует о том, что большую часть лимфоцитов периферической крови составляют покоящиеся лимфоциты, чей пролиферативный ответ на стимуляцию фитогемагглютинином (ФГА) может быть заблокирован глюкокортикои-дами. Положительные значения 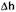 свидетельствуют о наличии в периферической крови большого количества активированных лимфоцитов, резистентных к антипролиферативному действию гормона. Такого рода резистентность связана с тем, что в активированных лимфоцитах уже произошло образование мРНК для ИЛ-2, и глюкокортикоиды не могут подавить синтез этого цитоки-на. Если средние значения величины Дп существенно превышают ноль, это можно рассматривать как свидетельство персистенции в крови большого количества клеток, активированных в очаге воспаления. В результате успешной антибактериальной терапии воспалительная реакция затухает и количество активированных лимфоцитов в крови уменьшается. Отражением этого процесса является повышение чувствительности лимфоцитов к антипролиферативному действию глюкокортикоидных гормонов. Важным элементом мониторинга реакции воспаления является определение высоты пролиферативного ответа лимфоцитов на Т-клеточные митогены (ФГА). Обычно при хронизации воспалительного процесса в результате сдвига иммунного ответа в направлении Th2 ответ лимфоцитов на ФГА оказывается сниженным. Напротив, при положительной динамике заболевания происходит переключение иммунного ответа на Thl-тип, что сопровождается существенным повышением высоты пролиферативного ответа лимфоцитов периферической крови на стимуляцию ФГА.
свидетельствуют о наличии в периферической крови большого количества активированных лимфоцитов, резистентных к антипролиферативному действию гормона. Такого рода резистентность связана с тем, что в активированных лимфоцитах уже произошло образование мРНК для ИЛ-2, и глюкокортикоиды не могут подавить синтез этого цитоки-на. Если средние значения величины Дп существенно превышают ноль, это можно рассматривать как свидетельство персистенции в крови большого количества клеток, активированных в очаге воспаления. В результате успешной антибактериальной терапии воспалительная реакция затухает и количество активированных лимфоцитов в крови уменьшается. Отражением этого процесса является повышение чувствительности лимфоцитов к антипролиферативному действию глюкокортикоидных гормонов. Важным элементом мониторинга реакции воспаления является определение высоты пролиферативного ответа лимфоцитов на Т-клеточные митогены (ФГА). Обычно при хронизации воспалительного процесса в результате сдвига иммунного ответа в направлении Th2 ответ лимфоцитов на ФГА оказывается сниженным. Напротив, при положительной динамике заболевания происходит переключение иммунного ответа на Thl-тип, что сопровождается существенным повышением высоты пролиферативного ответа лимфоцитов периферической крови на стимуляцию ФГА.
Таким образом, исследование маркеров воспаления при заболеваниях женских половых органов позволяют ответить на ряд важных вопросов, существенных для выбора тактики дальнейшей терапии. Прежде всего можно установить, в какой мере затронуты центральные механизмы иммунорегуля-ции. Существенный сдвиг иммунного ответа в сторону Th2 требует назначения адекватной иммунокорригирующей терапии. При обнаружении признаков центральной иммуносупрессии следует попытаться разорвать сложившийся порочный круг, воздействуя на различные его звенья.
