Изменение белкового состава при воспалении
Гипопротеинемия— снижение общего содержания белков в
плазме крови. Она может встречаться при
белковом голодании, заболеваниях
желудочно–кишечного тракта, печени,
почек.
Диспротеинемия— изменение соотношения отдельных
фракций белков (в норме альбумин-глобулиновый
коэффициент равен 1,5:1,9). В острой стадии
воспалительных заболеваний в плазме
увеличивается содержание глобулинов
α и β фракций. К белкам острой стадии
воспаления относятся, в частности,
гаптоглобин, орозомукоид, с– реактивный
белок. Считается, что белки острой фазы
воспаления оказывают защитное действие
на ткани, угнетают агрессивные
протеолитические ферменты тканей. При
хронических заболеваниях в плазме
увеличивается содержание иммуноглобулинов.
Парапротеинемия
— появление в плазме патологических
белков, таких как криоглобулины
(осаждаются при температуре ниже 37
о), пироглобулинов (осаждается при
60-80о С), фетопротеин (эмбриональный
белок).
11.3.2. Небелковые азотсодержащие вещества крови
Сумма низкомолекулярных
азотистых веществ, остающихся в крови
после осаждения белков, называется
остаточным азотом(RN).
В норме он составляет 15-25 ммоль/л. 50%
остаточного азота составляетмочевина,
концентрация которой равняется 3,3-8
ммоль/л, 25% остаточного азота приходится
нааминокислоты.В состав остаточного
азота крови входят такжепептиды,мочевая кислота (0,2-0,4 ммоль/л),аммиак(20-80 мкмоль/л),билирубин (2-8,20
мкмоль/л),креатинин (60-130 мкмоль/л).
Большинство
компонентов остаточного азота являются
конечными продуктами азотистого обмена,
которые выводятся через почки. В связи
с этим при патологии почек содержание
RNрезко увеличивается,
развивается симптом ретенционнойазотемии. Продукционная азотемия
встречается при увеличенном распаде
белков, онкологических заболеваниях.
11.3.2.1. Кининовая система крови.
Кинины представлены
пептидом брадикинином(9 аминокислотных
остатков),каллидином(10 остатков
аминокислот) илизил-метионил-брадикинином(содержит 11 аминокислот).
Б иологическое
иологическое
действие кининов моногообразно. Они
регулируют гемодинамику, увеличивают
работу сердца, расширяют сосуды, вызывают
спазм гладкой мускулатуры бронхов,
матки, являются медиаторами воспаления,
участвуют в регуляции свёртывающей и
антисвёртывающей системы крови, обладают
иммуномодуляторным действием.
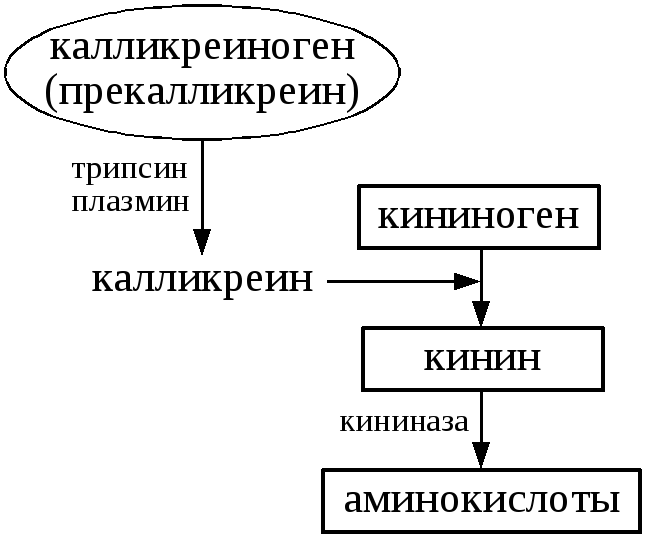
Кинины синтезируются
из неактивных белков предшественников
— кининогенов. В синтезе кининов участвуют
протеолитические ферменты каликренины.
Калликренины, в свою очередь, образуются
из не активных каликрииногенов
(прекалликреиногенов), при участии
трипсина, плазмина крови.Распад
кининов до аминокислот осуществляется
ферментами кининаазами.
11.3.3. Безазотистые органические вещества крови
К безазотистым
органическим веществам крови относятся
углеводы и липиды. Глюкоза содержится
в крови в концентрации 3,3-5,5 ммоль/л. В
крови присутствуют различные метаболиты
углеводного обмена (пируват, лактат, и
другие). Содержание сиаловых кислот
составляет 2,2-2,6 ммоль/л. Общее содержание
липидов у взрослых людей находится в
интервале 4-8 г/л. Концентрация
триацилглицеринов составляет 1,5-2,5
ммоль/л, фосфолипидов — 2,5-3,5 ммоль/л,
холестерина — 3,5-5,2 ммоль/л, свободных
жирных кислот — 0,4-0,8 ммоль/л. У детейсодержание всех видов жиров, кроме
свободных жирных кислот, ниже, чем у
взрослых.
Соседние файлы в предмете [НЕСОРТИРОВАННОЕ]
- #
- #
- #
- #
09.03.201623.62 Mб20Belov_Yu_V_Rukovodstvo_po_sosudistoy_khirurgii_s.djvu
- #
- #
- #
- #
- #
- #
- #
ГЛАВА 9. НАРУШЕНИЯ ОБМЕНА БЕЛКОВ И НУКЛЕИНОВЫХ КИСЛОТ
Белки
и их комплексы выполняют в организме такие важные функции как
информационная, рецепторная, каталитическая, структурная и некоторые
другие. Нарушения обмена аминокислот и белка приводят к существенным
расстройствам функций органов, их систем и организма в целом.
БАЛАНС АЗОТА
Азотистый баланс — суточная разница между поступающим и выделяемым азотом.
Виды азотистого баланса.
• Нулевой (количество поступающего и выводящегося азота совпадает).
•
Положительный (количество поступающего в организм азота больше,
чем выводящегося). Наблюдается как в норме (например, при регенерации
тканей или беременности), так и в условиях патологии (например, при
гиперпродукции СТГ или полицитемии).
•
Отрицательный (количество поступающего в организм азота меньше,
чем выводящегося). Наблюдается, например, при голодании, стрессе,
тяжёлом течении СД, гиперкортицизме.
ОСТАТОЧНЫЙ АЗОТ
Интегративный
параметр обмена белков и нуклеиновых кислот в организме — содержание
небелкового (остаточного) азота крови (табл. 9-1). Аммиак обладает
наиболее выраженными патогенными (цитотоксическими) свойствами из всех
компонентов остаточного азота. Он беспрепятственно проникает через
мембраны клеток, оказывая повреждающее действие на ферменты, компоненты
цитозоля и мембран. В норме аммиак инактивируется внутриклеточно,
вовлекаясь в реакции аминирования кетокислот с образованием
нетоксических веществ. Мочевина сама по себе не обладает токсическим действием. Большая часть мочевины образуется в печени (в орнитиновом цикле, или цик-
Таблица 9-1. Содержание небелкового (остаточного) азота в крови (в ммоль/л)
ле
мочевины) и выводится почками и потовыми железами. При почечной
недостаточности большое количество мочевины удаляется из организма через
кишечник, где она подвергается катаболизму кишечной флорой с
образованием внеклеточного аммиака. Креатин и креатинин. Уровни
креатина и креатинина в крови и моче, как правило, существенно меняются
при почечной недостаточности, гипотрофии мышц, миозитах и миастении,
длительном голодании, СД.
Мочевая кислота является
финальным метаболитом обмена пуринов и образуется, главным образом, в
гепатоцитах и энтероцитах с участием ксантиноксидазы, а разрушается в
кишечнике при участии бактерий с образованием глиоксалевой кислоты и
аммиака.
ТИПОВЫЕ НАРУШЕНИЯ БЕЛКОВОГО ОБМЕНА
К
типовым нарушениям белкового обмена относят: несоответствие
потребностям организма количества и аминокислотного состава поступающего
белка, нарушение расщепления белка в ЖКТ, расстройства трансмембранного
переноса аминокислот, дефекты метаболизма аминокислот, нарушения
содержания белков в плазме крови, нарушения конечных этапов катаболизма
белков, диспротеинозы.
Несоответствие потребностям организма количества и аминокислотного состава поступающего белка
Выделяют
несколько видов несоответствия количества и состава белка потребностям
организма: недостаток или избыток поступления белка в организм и
нарушение аминокислотного состава потребляемого белка.
НЕДОСТАТОЧНОЕ ПОСТУПЛЕНИЕ БЕЛКА
Оптимальное
количество белка, которое должно поступать в организм, колеблется в
диапазоне 1,5-2,5 г на кг массы тела в сутки. Основная причина
недостаточного поступления белка в организм — голодание. Выделяют
несколько видов голодания.
• Абсолютное (прекращение поступления в организм пищи и воды).
• Полное (прекращение поступления в организм пищи, но не воды).
• Неполное (недостаточное количество принимаемой пищи, в том числе белка).
• Частичное (недостаток в пище отдельных её компонентов — белков, липидов, углеводов, химических элементов, витаминов).
Проявления белкового голодания
При белковом голодании могут развиваться такие заболевания, как квашиоркор и алиментарная дистрофия.
Квашиоркор — несбалансированная алиментарная белково-энергетическая недостаточность.
Вызывается рационом с
недостаточным содержанием белка и незаменимых аминокислот, а также
избытком калорийных небелковых продуктов (крахмала, сахара).
Алиментарная дистрофия (алиментарный маразм) — сбалансированная белково-калорическая недостаточность.
Полное
или частичное белковое голодание приводит к мобилизации белка костей,
мышц, кожи, в значительно меньшей мере — белка внутренних органов.
ИЗБЫТОЧНОЕ ПОСТУПЛЕНИЕ БЕЛКА
• Причины:
♦ Переедание.
♦ Несбалансированная диета (длительный приём пищи с высоким содержанием белка).
♦ Активация протеосинтеза (например, при гиперпродукции
СТГ).
• Проявления:
♦ Положительный азотистый баланс.
♦ Повышенное содержание белка в крови.
♦ Диспептические расстройства (поносы, запоры).
♦ Дисбактериоз кишечника с аутоинтоксикацией.
♦ Отвращение к пище, особенно богатой белком.
НАРУШЕНИЯ АМИНОКИСЛОТНОГО СОСТАВА ПОТРЕБЛЯЕМОГО БЕЛКА
В
состав белков входят 22 аминокислоты, в том числе 8 незаменимых (валин,
изолейцин, лейцин, лизин, метионин, треонин, триптофан, фенилаланин).
Незаменимые аминокислоты не могут быть синтезированы в необходимом
объёме в организме человека и должны поступать с пищей.
Дефицит незаменимых аминокислот
• Общие проявления характерны для недостатка любой незаменимой аминокислоты:
♦ Отрицательный азотистый баланс.
♦ Замедление роста и нарушения развития у детей.
♦ Снижение регенераторной активности тканей и органов.
♦ Уменьшение массы тела.
♦ Снижение аппетита и усвоения белка пищи.
• Специфические проявления характерны для дефицита конкретной незаменимой аминокислоты.
Избыток отдельных аминокислот
• Общие проявления. Избыточное
поступление и образование аминокислот в организме приводит к нарушению
вкуса, снижению аппетита, уменьшению массы тела, расстройствам обмена
других аминокислот, нарушениям функций органов и тканей.
• Специфические проявления характерны для избытка конкретной аминокислоты.
Расстройства переваривания белка в желудке и кишечнике
Расстройства пищеварения в желудке и в тонком кишечнике приводят к нарушению обмена белка.
Нарушения расщепления белка в желудке
• Причины: гипоацидные состояния, снижение содержания или активности пепсина, резекция части желудка.
• Последствия и проявления: недостаточное расщепление белков, замедление эвакуации пищи в двенадцатиперстную кишку.
Нарушения переваривания белка в тонком кишечнике
• Причины: расстройство полостного и пристеночного расщепления белка в кишечнике, а также нарушение всасывания (синдромы мальабсорбции).
• Проявления:
♦ Креаторея.
♦ Целиакия
глютеновая — синдром, характеризующийся нарушением полостного и
мембранного переваривания белков, а также торможением всасывания
аминокислот.
♦ Диспептические расстройства.
Нарушения трансмембранного переноса аминокислот
Нарушения
трансмембранного переноса аминокислот обусловлены мембранопатиями
различного генеза, которые приводят к расстройствам транспорта
аминокислот на нескольких этапах: из кишечника в кровь, из крови в
гепатоциты, из первичной мочи в кровь, из крови в клетки органов и
тканей.
Примеры: синдром Фанкони, цистинурия,
цистиноз нефропатический, отравления солями тяжёлых металлов (например,
меди, кадмия, свинца, ртути), эндотоксинемии (например, при избытке
соединений меди).
Расстройства метаболизма аминокислот
Различают
первичные (наследственные, врождённые) и вторичные (приобретённые,
симптоматические) расстройства метаболизма аминокислот.
Примеры первичных
расстройств: фенилкетонурия, тирозинопатии (альбинизм, тирозинемии,
тирозинозы), алкаптонурия, ацидемия изовалериановая, лейциноз,
гомоцистеинурия.
Нарушение содержания белков в плазме крови
Уровень
протеинемии является результатом соотношения процессов протеосинтеза и
протеолиза в различных тканях и органах. В норме содержание белков в
плазме крови составляет около 7% её массы. Белок крови представлен
альбуминами (около 56%) и глобулинами (примерно 44%).
Диспротеинемии — типовые формы нарушения содержания белков в плазме крови.
Выделяют гиперпротеинемии, гипопротеинемии и парапротеинемии.
Гиперпротеинемии
Различают две разновидности увеличения общего содержания белков в плазме крови:
• Гиперсинтетическую (истинную, протеосинтетическую). Наблюдается гиперпродукция либо нормального белка (например, Ig),
либо парапротеинов (например, при плазмоцитомах, миеломной болезни);
•
Гемоконцентрационную (ложную). Гипопротеинемия развивается в
результате гемоконцентрации без усиления протеосинтеза (например, при
ожоговой болезни, диарее, повторной рвоте, длительном усиленном
потоотделении).
Гипопротеинемии
Известны два варианта уменьшения общей концентрации белков в плазме крови:
• Гипосинтетический (истинный). Этот вариант гипопротеинемии может быть двух видов.
♦ Первичной (наследственной или врождённой; например, гипопротеинемия при болезни Брутона).
♦ Вторичной
(приобретённой, симптоматической; например, при печёночной
недостаточности, белковом голодании, почечной недостаточности, ожоговой
болезни).
• Гемодилюционный. Эта гипопротеинемия
обусловлена гиперволемией (например, при гиперальдостеронизме или
почечной недостаточности).
Парапротеинемии
Парапротеинемии наблюдают при:
♦ миеломной болезни: опухолевые плазмоциты продуцируют аномальные лёгкие или тяжёлые цепи молекул Ig;
♦ лимфомах (лимфоцитарных или плазмоцитарных). Лимфомы синтезируют аномальные IgM, обладающие повышенной агрегируемостью.
Расстройства финальных этапов катаболизма белка
Расстройства
конечных стадий катаболизма белка характеризуются нарушением
образования и дальнейших изменений мочевины, аммиака, креатинина,
индикана, а также их выведения из организма.
Диспротеинозы
Диспротеинозы — патологические состояния, характеризующиеся изменением физико-химических свойств белков и расстройством их функций.
По преимущественной локализации патологического процесса различают клеточные и внеклеточные (амилоидоз, гиалиноз, мукоидное
и фибриноидное набухание) диспротеинозы. Подробно о диспротеинозах смотрите в разделе «Дистрофии» главы 4.
НАРУШЕНИЯ ОБМЕНА НУКЛЕИНОВЫХ КИСЛОТ
Нарушения обмена нуклеиновых кислот характеризуются расстройствами синтеза и деструкции пиримидиновых и пуриновых оснований.
• Пиримидиновые основания: урацил, тимин, цитозин, метил- и оксиметилцитозин.
•
Пуриновые основания: аденин, гуанин, метиладенин, метилгуанин.
Они являются составной частью макроэргических соединений — аденинди- и
трифосфата, гуанинди- и трифосфата. Финальный метаболит обмена пуринов —
мочевая кислота.
Расстройства метаболизма пиримидиновых оснований
К
расстройствам, сопровождающимся нарушением метаболизма пиримидиновых
оснований, относятся оротацидурия, гемолитическая анемия и
аминоизобутиратурия вследствие недостаточности 3-гидрок- сиизобутират
дегидрогеназы.
Нарушения обмена пуриновых оснований
К
основным проявлениям, вызванным нарушениями обмена пуриновых оснований,
относят подагру, гиперурикемию, синдром ЛешаНайена и гипоурикемию.
ГИПЕРУРИКЕМИЯ
Гиперурикемия — состояние, проявляющееся повышенной концентрацией мочевой кислоты в крови и, как следствие — в моче.
ПОДАГРА
Подагра —
заболевание, характеризующееся хронической гиперурикемией, отложением
уратов в органах и тканях, уратной нефропатией и уролитиазом.
Этиология
• Причины:
♦ Первичные. Представляют собой генетический дефект ферментов обмена мочевой кислоты.
♦ Вторичные. Наиболее часто это сахарный диабет, гиполипопротеинемии, артериальная гипертензия, ожирение.
• Факторы риска:
♦ Повышенное
поступление в организм пуриновых оснований (например, при употреблении
большого количества мяса, молока, икры, рыбы, кофе, какао, шоколада).
♦ Увеличение
катаболизма пуриновых нуклеотидов (например, при противоопухолевой
терапии; массивном апоптозе у пациентов с аутоиммунными болезнями).
♦ Торможение выведения мочевой кислоты с мочой (например, при почечной недостаточности).
♦ Повышенный
синтез мочевой кислоты при одновременном снижении выведения её из
организма (например, при злоупотреблении алкоголем, шоковых состояниях,
гликогенозе с недостаточностью глюкозо-6-фосфатазы).
Патогенез подагры
Наиболее важными звеньями патогенеза подагры являются:
♦ активация
системы комплемента с образованием факторов хемотаксиса C5a и C3a под
влиянием избытка уратов в плазме крови и межклеточной жидкости;
♦ накопление
лейкоцитов в местах отложения кристаллов мочевой кислоты: в коже,
почках, хрящах, в околосуставных тканях под влиянием хемотаксических
веществ;
♦ фагоцитоз кристаллов мочевой кислоты, который сопровождается высвобождением БАВ, инициирующих асептическое воспаление;
♦ повреждение
клеток и неклеточных элементов медиаторами воспаления и непосредственно
уратами, сопровождающееся образованием антигенных структур, что
активирует реакции иммунной аутоагрессии;
♦ развитие
(в зоне отложения уратов) хронического пролиферативного воспаления,
образования подагрических гранулём и подагрических «шишек» — tophi urici, обычно вокруг составов.
Проявления подагры
• Постоянно повышенная концентрация мочевой кислоты в плазме крови и в моче.
• Воспаление суставов по типу моноартритов, что сопровождается сильной болью и лихорадкой.
• Уролитиаз и рецидивирующие пиелонефриты, завершающиеся нефросклерозом и почечной недостаточностью.
ГИПОУРИКЕМИЯ
Гипоурикемия — состояние, характеризующееся снижением концентрации мочевой кислоты в крови ниже нормы.
• Возможная причина: недостаточность ксантиноксидазы или сульфитоксидазы.
• Проявления
♦ Образование кристаллов ксантина в ткани почек, вокруг суставов и в мышцах.
♦ Мышечные судороги и нистагм (обусловлены миозитами, поражением центральных и периферических нейронов).
При остром воспалительном процессе в крови накапливаются синтезируемые гепатоцитами, макрофагами и другими клетками так называемые “белки острой фазы”. Для хронического течения воспаления характерно увеличение в крови содержания a- и особенно g-глобулинов, дисбаланс альбуминов и глобулинов.
Увеличение скорости оседания эритроцитов (СОЭ), что особенно имеет место при хронических воспалительных процессах, обусловлено повышением вязкости крови, снижением отрицательного заряда и агломерацией эритроцитов, изменениями физико-химических констант, состава белков (диспротеинемии) крови, подъемом температуры.
Изменения содержания гормонов в крови заключаются, как правило, в увеличении концентрации катехоламинов и кортикостероидов.
Классификация воспаления и выделение его различных форм, основанные на клиническом опыте, учитывают вклад в развитие воспаления свойств и болезнетворных факторов, и самого организма. Выделяют инфекционное и неинфекционное (асептическое) воспаление; инфекционное воспаление в свою очередь разделяют на банальное и специфическое. По выраженности основных компонентов воспаление разделяют на альтеративное, экссудативное и пролиферативное (продуктивное).В зависимости от вида экссудата экссудативное воспаление может быть серозным, фибринозным (крупозным и дифтеритическим), гнойным, геморрагическим и гнилостным, а продуктивное воспаление — межуточным, гранулематозным и полипозным. По выраженности местных и общих проявлений можно выделить гиперергическое, гипергическое и нормергическое, а по скорости развития и продолжительности — острое и хроническое воспаление.
Классификация и формы воспаления служат целям диагностики и терапии. Некоторые формы воспаления, выделенные по разным критериям, нередко сочетаются или же одна форма переходит в другую: например острое экссудативное воспаление переходит в хроническое продуктивное, что имеет важное клиническое значение. Инфекционное специфическое воспаление нередко является пролиферативным (продуктивным), относится к гранулематозному воспалению и часто имеет хроническое рецидивирующее течение, как это наблюдается при туберкулезе, сифилисе, проказе, бруцеллезе, сапе, ревматизме, грибковых и паразитарных заболеваниях. Хотя гранулематозное воспаление имеет общие черты и в его возникновении существенную роль играют иммунные перестройки, конкретное клинико-морфологическое выражение гранулем (в том числе клеточный состав) определяется характером патогенного воздействия, свойствами организма и локализацией процесса. Далеко неоднозначны также морфологические, а особенно клинические исходы и осложнения гранулематозного процесса: творожистый некроз при туберкулезе, гуммозный распад при сифилисе, колликвационный некроз с нагноением при сапе и грибковых поражениях, переход в склероз или инкапсуляцию с петрификацией очага. Результатом этого могут быть блокада проводимости в сердце или пороки сердца при ревматизме, аневризма аорты или коронарная недостаточность, дольчатая печень и легкие при сифилисе, недостаточность надпочечников при туберкулезе, рубцевание мозговой ткани с возникновением эпилепсии при сыпном тифе и т.д.
Вместе с тем классификация и выделение форм воспаления имеют относительный характер: появляются промежуточные и переходные варианты в связи с нередкой комбинацией действия нескольких патогенных факторов, изменением реактивных свойств организма в динамике процесса, с его локализацией и др. Поэтому выделяют альтеративно-экссудативное, серозно-фибринозное и серозно-геморрагическое воспаление; воспаление, начавшееся остро, может переходить в хроническое с периодами обострения и затухания (ремиссии). По мнению И. В. Давыдовского, специфической предпосылкой хронической формы следует считать невозможность завершения острого воспаления регенерацией. Это зависит прежде всего от условий регенерации, а не от каких-либо особых причин, которым будто бы свойственно вызывать именно хроническое воспаление. Исходя из положения о том, что само возникновение, особенности развития, т. е. формы воспаления, а также его исходы определяются в большей или меньшей мере свойствами патогенного фактора и свойствами организма, мнение И. В. Давыдовского о том, что любое воспаление является острым, кажется дискуссионным. Существуют экзо- и эндогенные факторы, которые при соответствующем состоянии реактивности изначально формируют хронический, вяло протекающий, процесс (паразиты, патогенные грибы, отложение в тканях солей вследствие нарушенного обмена и т.п.). Хронический воспалительный процесс в динамике своего развития периодически обостряется вследствие дополнительного изменения свойств макроорганизма и нередко активации персистирующей инфекции. Несомненно, что регенерация является важным механизмом ограничения и изоляции очага воспаления, а также устранения дефекта ткани, т. е. прекращения острого воспаления. Однако усиленная регенерация иммуноцитов и мезенхимальных клеток является обязательным компонентом возникновения хронического продуктивного воспаления или перехода острого альтеративно-экссудативного воспаления в хроническую продуктивную его форму.
Переход острого воспаления в хроническое связан с незавершенностью воспаления, когда конечная цель воспаления, заключающаяся в уничтожении патогенного агента и его удалении из организма, не достигается. Природа хронизации процесса воспаления также зависит от свойств и вида возбудителя (лейшмании, малярийный плазмодий, эхинококк, амебная инвазия и др.) и от свойств макроорганизма, от взаимного приспособления микро- и макроорганизма с установлением неустойчивого равновесия. Это равновесие может нарушаться, и возникают периоды обострения в случае ослабления антиинфекционной защиты и активации инфекта. Конкретные механизмы хронизации воспаления при всех его вариантах в полной мере не изучены; выделяют местные, регионарные и общие факторы, которые препятствуют реализации конечной цели воспаления. По И. В. Давыдовскому (1964), к местным причинам хронизации воспаления следует отнести образования, постоянно травмирующие ткани (например, костные осколки в ране, секвестры, инородные тела, нарастающее отложение солей и др.). Среди регионарных факторов, поддерживающих воспаление, следует назвать расстройства крово- и лимфообращения, в том числе нарушения, вызванные атеросклерозом, артериитами, варикозным расширением вен, слоновостью, расстройствами иннервации разного происхождения. Эти факторы при воспалении нередко способствуют возникновению язвенного процесса и длительному незаживлению язв. Важное значение в хронизации воспаления имеют общие расстройства, обусловленные нарушением работы неспецифических и специфических механизмов иммунитета, например недостаточность фагоцитоза и некоторые так называемые селективные формы иммунодефицитных состояний. Чаще иммунодефицитные состояния приводят к нарушению механизмов изоляции воспалительного очага и развитию сепсиса. Все же обычно хронизация воспаления связана с двумя взаимодействующими явлениями — персистенцией причинного фактора и развитием иммунопатологических процессов. Возникновение иммунопатологических процессов и хронизация воспаления могут быть следствием появления аутоаллергенов в очаге воспаления и/или трансформации свойств иммунной системы. Пролонгированию воспаления также способствуют общее истощение организма, авитаминозы, анемии, недостаточность кровообращения, белковое голодание, сахарный диабет и многие другие явления. При данных состояниях нередко возникает недостаточность механизмов иммунитета, которая способствует переходу острого воспаления в хроническое.
