Кишечные инфекции воспаление суставов

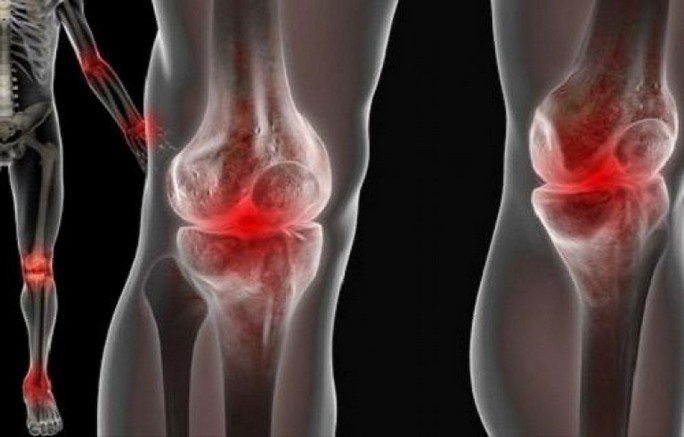
Реактивный артрит развивается у 3% пациентов, перенесших хламидийную урогенитальную инфекцию. Он диагностируется у 4% больных кишечными инфекционными заболеваниями. У детей патология обнаруживается исключительно редко. Наиболее часто реактивный артрит поражает мужчин 20-40 лет, у женщин он выявляется в 20 раз реже. В его лечении используются консервативные методы — прием антибиотиков и анальгетиков, проведение физиотерапевтических и массажных процедур, ЛФК.
Общие сведения о реактивном артрите
Важно знать! Врачи в шоке: «Эффективное и доступное средство от АРТРИТА существует…» Читать далее…
Реактивный артрит — воспалительное заболевание крупных и мелких суставов. Он развивается на фоне урогенитальной, кишечной инфекции или спустя некоторое время после ее излечения. Для патологии характерно последовательное вовлечение в воспалительный процесс органов мочеполовой системы, глаз, суставов. Не у всех людей, в чей организм проникли инфекционные возбудители, возникает реактивный артрит. Установлена взаимосвязь между воспалительным поражением суставов и носительством антигена НLA-B27. В этом случае вероятность развития аутоиммунного заболевания выше в 50 раз.
Причины возникновения патологии
Избирательность реактивного артрита обусловлена генетической предрасположенностью. После внедрения в организм возбудителей урогенитальных и кишечных инфекций они гематогенным путем проникают в синовиальную жидкость. В результате их контакта с антигенами НLA-B27 образуются сложные белковые комплексы, сходные по структуре с клетками суставных тканей. Иммунной системой вырабатываются антитела для уничтожения чужеродных белков, но атакуют они собственные клетки организма, что приводит к развитию асептического воспалительного процесса.
Хламидиоз
Хламидии — шаровидные болезнетворные бактерии, паразитирующие в организме человека в форме цитоплазматических включений. Возбудителем урогенитального реактивного артрита становятся C. trachomatis. В большинстве случаев заражение происходит при незащищенном половом контакте. Реже хламидии передаются от человека к человеку бытовым путем, например, через постельные и туалетные принадлежности. Возможно также заражение ребенка во время его прохождения по родовым путям.
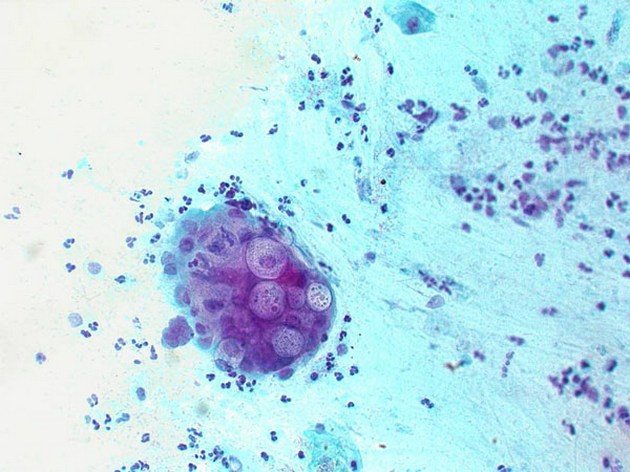
Хламидии под микроскопом.
Другие мочеполовые инфекции
Реже в роли этиофакторов реактивного артрита выступают возбудители уреаплазмоза и микоплазмоза. Это мельчайшие микроорганизмы семейства микоплазм — промежуточное звено между вирусами и бактериями (не имеют ДНК и клеточной оболочки). В 70-80% случаев заболевание протекает в форме бессимптомного носительства. Но при некорректной работе иммунной системы после проникновения бактерий в организм запускается воспалительный процесс в суставах.
Кишечные инфекции
Спровоцировать развитие реактивного артрита способны возбудители кишечных инфекций — иерсинии, сальмонеллы, дизентерийная палочка, кампилобактерии, клостридии. Эти болезнетворные бактерии передаются от человека к человеку обычно бытовым путем, попадают в организм вместе с продуктами питания. Риск заражения кишечными инфекциями повышается при употреблении пищи, не подвергшейся термической обработке.
Дыхательные инфекции
Возбудители инфекций, поражающих верхние и нижние дыхательные пути, крайне редко становятся причиной развития реактивного артрита. Тем не менее, в медицинской литературе описаны подобные случаи. Наиболее часто в роли этиофакторов выступают вирусы. Они содержат особые белки, сходные по структуре с клетками синовиальных оболочек. Поэтому иммунная система атакует не только вирусы, но и суставные структуры.
Другие инфекционные болезни
Предпосылкой к реактивному артриту могут стать вирусные гепатиты, ВИЧ и другие бактериальные и вирусные инфекции. Основное отличие патогенеза — отсутствие возбудителей непосредственно в суставах. Толчком к развитию воспаления становятся исключительно продуцируемые иммунной системой антитела. Поэтому есть вероятность постановки неправильного диагноза. Проводится комплексное лечение инфекционного артрита, в то время как необходимо использование иммуномодуляторов.
Характерные признаки и симптомы патологии
Для реактивного артрита характерна классическая триада клинических проявлений — последовательное поражение глаз, урогенитального тракта и суставов. Первые признаки возникают примерно через 2-4 недели после симптомов инфекции. Клиника сохраняется на протяжении 3-12 месяцев. Затем выраженность симптомов начинает постепенно ослабевать, вплоть до их полного исчезновения. Это не означает, что человек полностью выздоровел. Под действием провоцирующих внешних или внутренних факторов может возникнуть рецидив реактивного артрита с вовлечением в хронический воспалительный процесс здоровых суставов.
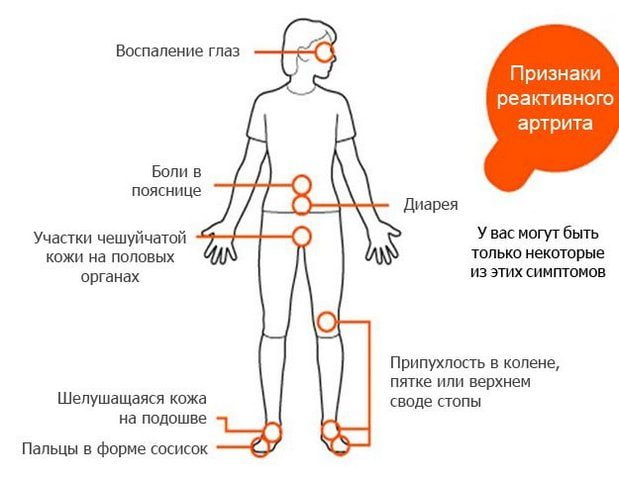
Суставные
Реактивный артрит всегда манифестирует остро, с поражением нескольких суставов ног. Чаще всего в воспалительный процесс вовлекаются межфаланговые, плюснефаланговые, пяточные, коленные, голеностопные сочленения. Возникают ноющие, давящие боли, усиливающиеся при ходьбе. Суставы увеличиваются в размерах, кожа над ними отекает, краснеет, становится горячей на ощупь. Температура тела повышается до 37-38 градусов, появляются слабость, недомогание, быстрая утомляемость.
Внесуставные
Внесуставные признаки реактивного артрита возникают перед суставными. Вначале развевается уретрит — воспаление стенок мочеиспускательного канала. Для патологии характерны болезненные ощущения, жжение, зуд при опорожнении мочевого пузыря. Учащаются позывы к мочеиспусканию, при этом отделяется незначительное количество мочи.
Вскоре к уретриту присоединяется конъюнктивит. Веки краснеют, отекают, воспаляется слизистая, появляются светобоязнь, зрительные расстройства, перед глазами мелькают черные точки, цветные пятна.
К какому врачу обратиться
Лечением реактивного артрита занимается ревматолог. Но так как самостоятельно установить причину болей в суставах маловероятно, то целесообразно обратиться к врачу общего профиля — терапевту. Он назначит необходимые диагностические мероприятия, а после изучения их результатов направит пациента к ревматологу. В обследовании, а также дальнейшем лечении могут принимать участие инфекционисты, венерологи, урологи, гинекологи, отоларингологи, гастроэнтерологи.
Методы диагностики болезни
Под симптомы реактивного артрита могут маскироваться другие патологии, поражающие суставы ног. Это деформирующий остеоартроз, в том числе гонартроз, инфекционный, ревматоидный, подагрический артрит, бурсит, тендовагинит, синовит. Поэтому проводится тщательная дифференциальная диагностика для исключения этих заболеваний, а также для выявления причины ухудшения самочувствия пациента.
Сбор анамнеза
Первичный диагноз может быть выставлен на основании сочетанного поражения глаз, мелких и крупных суставов ног, уретры. Значение также имеют данные анамнеза. На развитие реактивного артрита указывают недавно перенесенные или еще протекающие урогенитальные, кишечные, респираторные инфекции. Врач расспрашивает пациента о наличии аутоиммунных патологий у родственников, например, псориаза или анкилозирующего спондилоартрита.

Лабораторные исследования
Протекающий в организме воспалительный процесс обнаруживается на этапе проведения общеклинических анализов по увеличению уровня лейкоцитов, повышенной скорости оседания эритроцитов. В биохимической и серологической диагностике реактивного артрита наиболее востребован метод полимеразной цепной реакции, позволяющий установить видовую принадлежность инфекционных агентов.
Дополнительно исследуется синовиальная жидкость. Признаками патологии становятся ее низкая вязкость, повышенный уровень лейкоцитов, плохое формирование муциновых сгустков.

Инструментальные исследования
С помощью рентгенографии можно выявить признаки поражения суставов — сужение суставной щели, эрозии костных поверхностей. На выполненных в двух проекциях снимках визуализируются пяточные шпоры, паравертебральная оссификация, периостит костей стоп. В большинстве случаев не требуется проведение артроскопии.
Для более детального изучения суставных структур иногда назначается МРТ, позволяющая оценить состояние хрящей, мышц, связочно-сухожильного аппарата, нервных стволов, кровеносных сосудов.
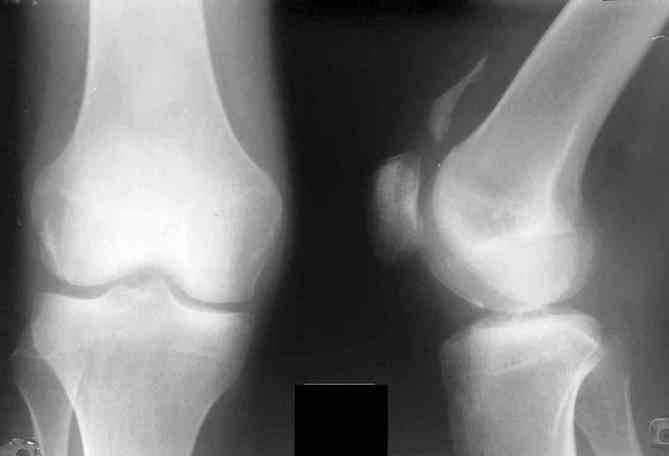
Как проходит лечение реактивного артрита
Пациентам показана комплексная терапия патологии. Одновременно проводится лечение инфекции, спровоцировавшей развитие артрита, устранение симптомов поражения уретры, слизистой глаз и суставов. Основная задача терапии — достижение устойчивой ремиссии.
Медикаменты
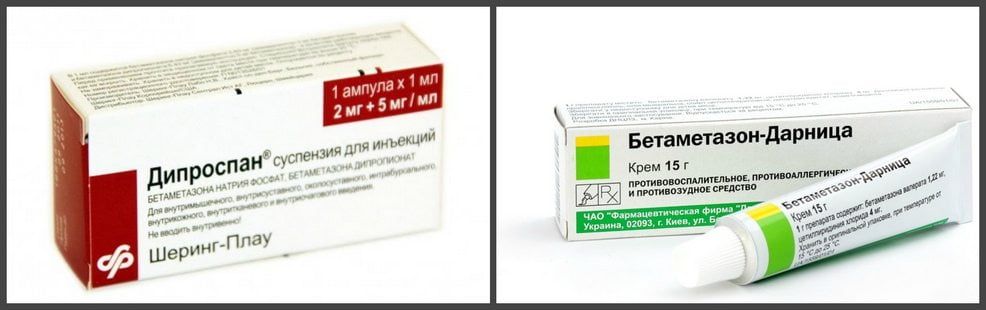
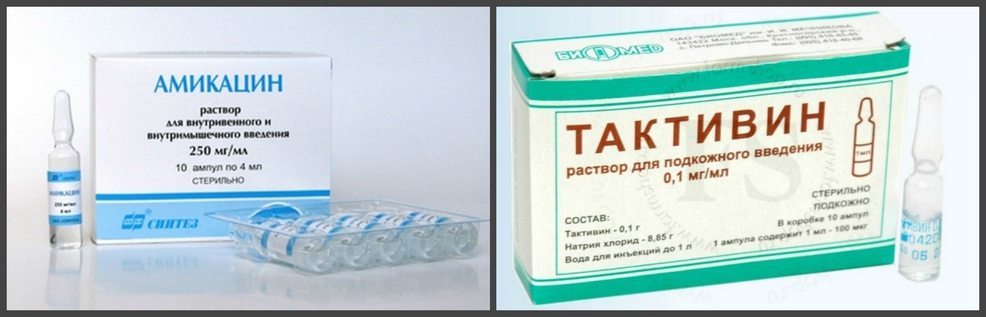
В лечебные схемы включаются антибиотики, к которым патогенные микроорганизмы наиболее чувствительны. Чаще всего используются тетрациклины, макролиды, фторхинолоны, цефалоспорины, полусинтетические пенициллины. Для профилактики осложнений антибиотикотерапии применяются противогрибковые средства, гепатопротекторы, эубиотики, сбалансированные комплексы витаминов и микроэлементов.
| Группа препаратов для лечения реактивного артрита | Наименования лекарственных средств |
| Иммуносупрессоры | Азатиоприн, Сульфасалазин, Метотрексат |
| Ингибиторы ФНО | Этанерцепт, Инфликсимаб |
| Глюкокортикостероиды | Метилпреднизолон, Дипроспан, Флостерон, Дексаметазон |
| Нестероидные противовоспалительные средства | Диклофенак, Индометацин, Мелоксикам, Кеторолак, Нимесулид, Лорноксикам, Ибупрофен, Эторикоксиб, Целекоксиб, Рофекоксиб |
| Препараты для локального нанесения | Димексид, Вольтарен, Ортофен, Найз, Кеторол, Нурофен, Долгит, Быструмгель |
Физиолечение
В физиотерапии реактивного артрита применяются магнитотерапия, синусоидально-модулирующие токи, криотерапия, лазеротерапия, озокеритолечение, аппликации с парафином, УВЧ-терапия.
Для купирования выраженных болей проводится фонофорез или электрофорез с глюкокортикостероидами, анестетиками, витаминами группы B, хондропротекторами.

Оперативное лечение
Необходимости в хирургическом лечении пациентов не возникает. В некоторых случаях с помощью пункции из сустава извлекается экссудат, а его полость обрабатывается растворами с противомикробной и антисептической активностью.
Лечебная гимнастика и массаж
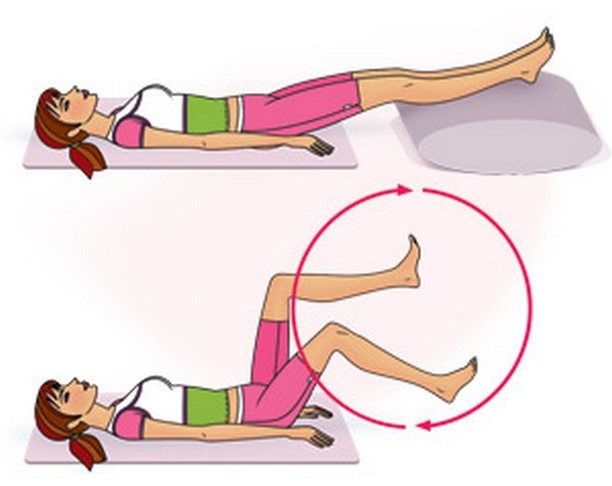
Занятия лечебной физкультурой проводятся под руководством врача ЛФК сразу после купирования сильных болей и острого воспаления. Целями ежедневного выполнения упражнений становятся укрепление мышц, улучшение кровообращения, повышение объема движений в суставах. Пациентам показаны неглубокие выпады и приседания, имитация езды на велосипеде в положении лежа.
Лечебная гимнастика всегда сочетается с сеансами классического, вакуумного, акупунктурного массажа. Во время процедур массажист воздействует на напряженные мышцы, выполняя разминания, поглаживания, вибрации. После проведения 10-20 сеансов устраняются болезненные ощущения, нарушения чувствительности, тугоподвижность, мышечные спазмы.
Народные методы
На стадии ремиссии врачи разрешают пациентам избавляться от остаточных дискомфортных ощущений с помощью народных средств. Используются мази домашнего приготовления, настои и отвары лекарственных трав, водочные и масляные настойки, компрессы. Их слабый терапевтический эффект обусловлен местнораздражающим, согревающим, отвлекающим действием.

Диета
Лечебная диета не является самостоятельным методом терапии реактивного артрита. Ее соблюдение не позволяет снижать выраженность симптоматики, ослаблять воспалительные процессы. Ревматологи рекомендуют только исключить из рациона продукты с высоким содержанием жиров и алкоголь, провоцирующие обострение заболевания.
Возможные последствия
У каждого десятого пациента после перенесенного реактивного артрита наблюдается деформация стоп, развивается плоскостопие. При отсутствии врачебного вмешательства хронический воспалительный процесс приводит к постепенному разрушению хрящевых и костных структур, провоцирует появления деформирующего артроза. В результате частичного или полного сращения суставной щели возникает анкилоз, или обездвиживание сустава.
Прогноз заболевания
Только в 35% диагностированных случаев можно говорить о полном излечении. Симптомы патологии исчезают в течение 5-6 месяцев и больше не появляются. Примерно у такого же количества больных отмечены рецидивы артрита спустя несколько лет. У 25% пациентов патология медленно, но упорно прогрессирует. К тяжелому поражению суставов и позвоночного столба течение реактивного артрита приводит в 5% случаев.
Меры профилактики
Основная профилактика заболевания исключается в предупреждении развития урогенитальных или кишечных инфекций. Если не удалось избежать заражения, то необходимо обратиться за медицинской помощью при первых признаках патологии. Врачи рекомендуют также 1-2 раза в год проходить полное обследование, особенно при наличии у родственников каких-либо аутоиммунных заболеваний.
Похожие статьи
Как забыть о болях в суставах и артрите?
- Боли в суставах ограничивают Ваши движения и полноценную жизнь…
- Вас беспокоит дискомфорт, хруст и систематические боли…
- Возможно, Вы перепробовали кучу лекарств, кремов и мазей…
- Но судя по тому, что Вы читаете эти строки — не сильно они Вам помогли…
Но ортопед Валентин Дикуль утверждает, что действительно эффективное средство от АРТРИТА существует! Читать далее >>>
загрузка…
Изучение хронических воспалительных заболеваний кишечника (ХВЗК) является актуальной проблемой не только детской гастроэнтерологии, но и детской ревматологии вследствие частого дебюта этих патологических состояний именно с суставных проявлений и дальнейшего течения клинически взаимосвязанных кишечного и суставного синдромов.
Распространенность ХВЗК среди детского населения составляет 2,2–6,8 на 100 тыс. детей [1, 2]. С наибольшей частотой в детском возрасте диагностируются такие заболевания этой группы, как болезнь Крона и язвенный колит. Отмечено, что язвенный колит чаще встречается у мальчиков, а болезнь Крона — у мальчиков и девочек с примерно с одинаковой частотой [2].
Болезнь Крона (регионарный энтерит, гранулематозный илеит) — воспалительное заболевание с вовлечением в процесс всех слоев кишечной стенки; характеризуется прерывистым (сегментарным) характером поражения различных разделов желудочно-кишечного тракта. Для него характерна диарея с примесью слизи и крови, боли в животе (часто в правой подвздошной области), потеря массы тела, лихорадка.
Язвенный колит (неспецифический язвенный колит, идиопатический колит) — язвенно-деструктивное поражение слизистой оболочки толстой кишки, которое локализуется преимущественно в ее дистальных отделах. В клинической картине характерны: кровотечения из прямой кишки, учащенное опорожнение кишечника, тенезмы; боли в животе менее интенсивны, чем при болезни Крона, локализуются чаще всего в левой подвздошной области. Примерно у 30% пациентов юношеского возраста язвенный колит начинается внезапно с появления болей в животе и диареи с примесью крови.
По данных разных авторов, внекишечные проявления ХВЗК отмечаются в 5–25% случаев. Наибольшая их доля приходится на тотальные формы неспецифического язвенного колита (87,5%) и болезни Крона с вовлечением в процесс толстой (29%) или толстой и тонкой кишки (58,1%) [3]. Системные проявления ХВЗК по патогенетическому принципу разделяют на три группы. К первой группе относят проявления, возникающие вследствие системной гиперсенсибилизации, — поражения суставов, глаз, кожи, слизистой оболочки рта; ко второй — обусловленные бактериемией и антигенемией в портальной системе — поражения печени и билиарного тракта. Выделяют также явления, развивающиеся вторично при длительно существующих нарушениях в толстой кишке, — анемии, электролитные расстройства.
Патогенез суставных проявлений остается неясным. Обсуждается значение повышенной проницаемости стенки кишечника, отмечающейся у больных язвенным колитом и болезнью Крона, в результате чего в кровь в большом количестве попадают компоненты оболочки стенок бактерий. Эти компоненты выступают в качестве пептидных антигенов, способных приводить к развитию артритов. Связываясь с молекулами комплексов гистосовместимости и активируя в дальнейшем Т-лимфоциты, пептиды приводят к возникновению воспаления суставов [3].
С точки зрения ревматолога суставные проявления ХВЗК относят к т. н. серонегативным спондилоартропатиям. Это большая гетерогенная группа клинически пересекающихся, хронических воспалительных ревматических заболеваний [4]. Помимо артритов, связанных с воспалительными заболеваниями кишечника, в эту группу включают такие ревматические заболевания детского возраста, как ювенильный спондилоартрит, ювенильный реактивный артрит, ювенильный псориатический артрит, а также недифференцированные спондилоартропатии (дактилит, увеит, сакроилеит в отсутствии полного набора критериев). Несмотря на гетерогенность заболеваний данной группы, клинически серонегативные спондилоартропатии имеют общие признаки и характеризуются:
- патологическими изменениями в крестцово-подвздошном отделе и/или других суставах позвоночника;
- синдромом периферической воспалительной артропатии, проявляющейся асимметричным артритом преимущественно нижних конечностей;
- энтезопатическим синдромом;
- ассоциацией с антигеном гистосовместимости HLA-B27;
- тенденцией к накоплению этих заболеваний в семьях;
- частым наличием внесуставных симптомов (поражение глаз, клапанов аорты, кожи) [5, 6]. В МКБ-10 поражения суставов при рассматриваемых нами заболеваниях кодируются следующим образом: М07.4 Артропатия при болезни Крона (К50); М07.5 Артропатия при язвенном колите (К51).
Поражения суставов при ХВЗК встречаются в 20–40% случаев и протекают в виде артритов (периферической артропатии), сакроилеита и/или анкилозирующего спондилита [3].
Артриты
Артриты относятся к наиболее частым суставным проявлениям хронических воспалительных заболеваний кишечника. Нередко они сочетаются с поражением кожи в виде узловатой эритемы. Частота возникновения артритов, распространенность поражения толстой кишки коррелируют с воспалительной активностью основного заболевания. В некоторых случаях артриты могут предшествовать кишечным проявлениям за много месяцев и даже лет, а также сохраняться в фазу ремиссии [7].
Клиническая картина артритов при болезни Крона и язвенном колите идентична. Характерно ассиметричное, мигрирующее поражение суставов чаще нижних конечностей. Преимущественно страдают коленные и голеностопные суставы, далее следуют локтевые, тазобедренные, межфаланговые и плюснефаланговые суставы. Число пораженных суставов обычно не превышает пяти. Суставной синдром течет с чередованием периодов обострений, длительность которых не превышает 3–4 месяцев, и ремиссий. Могут выявляться энтезопатии, талалгии. Артриты, как правило, начинаются остро. Однако нередко больные предъявляют жалобы только на артралгии, и при объективном обследовании изменения не обнаруживаются. Со временем обострения артритов становятся реже. У большинства больных артриты не приводят к деформации или деструкции суставов.
Выделяют два типа поражения периферических суставов. Для первого характерно поражение небольшого количества крупных суставов, ассиметричность суставного синдрома, острое течение. Часто при этом типе суставной синдром предшествует клинической картине основного заболевания, ассоциируется с его обострениями и сочетается с другими внекишечными проявлениями ХВЗК. Второй тип протекает по типу симметричного полиартрита, его обострения не совпадают по времени с обострениями основного процесса в кишечнике и другими системными проявлениями заболевания [7, 8].
Проведение колэктомии у больных язвенным колитом способствует прекращению рецидивирующих артритов [3].
Сакроилеит
По данным рентгенологического исследования, сакроилеит обнаруживается примерно у 50% больных ХВЗК. При этом у 90% он имеет бессимптомное течение. Он не ассоциируется с повышенной частотой выявления у больных HLA-B27. Также наличие сакроилеита не коррелирует с активностью воспалительного заболевания кишечника. Существуя на протяжении нескольких лет, может быть предшественником язвенного колита или болезни Крона. Сакроилеит может быть единственной локализацией изменений со стороны суставов, но часто сочетается с первым типом течения артритов. Необходимо помнить, что сакроилеит может быть ранним симптомом анкилозирующего спондилита. Терапия кишечного синдрома не приводит к изменению клинической картины сакроилеита [7].
Анкилозирующий спондилит
Анкилозирующий спондилит (АС) при ХВЗК клинически, как и сакроилеит, не отличается от идиопатического анкилозирующего спондилита. Чаще встречается у лиц мужского пола. По наблюдениям, у лиц женского пола поражение шейного отдела позвоночника манифестирует в более молодом возрасте и протекает тяжелее. Симптомы АС обычно предшествуют манифестации болезни Крона или язвенного колита и не коррелируют с активностью воспаления в кишечнике. Отмечаются боли в позвоночнике, чувство утренней скованности, нарастает ограничение подвижности в шейном, грудном, поясничном отделах позвоночника. Активная терапия основного заболевания не приводит к изменению клинической картины спондилита [3, 7, 9, 10].
Клиническое наблюдение
Иллюстрацией к вышеизложенному материалу может служить клиническое наблюдение за течением болезни Крона с внекишечными суставными проявлениями у пациента подросткового возраста.
Клинический диагноз: болезнь Крона (поражение тонкого, толстого кишечника, желудка, пищевода), фаза ремиссии, внекишечные проявления (лихорадка в анамнезе, лимфаденопатия, гепатомегалия, железодефицитная анемия). Осложнения: стеноз устья баугиниевой заслонки, сужение входа в слепую кишку.
Ювенильный спондилоартрит, активность I степени, рентгенологическая стадия I–II, НФ-1.
Из анамнеза жизни следует отметить, что мальчик от 2-й беременности, протекавшей физиологически, от первых срочных родов, осложнившихся слабостью родовой деятельности (акушерское пособие — наложение проходных щипцов). Находился на раннем искусственном вскармливании. На первом году жизни наблюдался неврологом. В дальнейшем редкие ОРВИ. Привит по календарю. Детскими инфекциями не болел. Наследственность отягощена по заболеваниям сердечно-сосудистой системы.
Анамнез заболевания: в сентябре 2008 г. после травмы левого голеностопного суставе у ребенка отмечался отек и болезненность в левом голеностопном сустава. Получал местно мази с нестероидными противовоспалительными препаратами (НПВП). Также применялось физиотерапевтическое лечение, что вызвало ухудшение состояния: появилась субфебрильная лихорадка, усилились артралгии в левом голеностопном суставе, также появилась болезненность в височно-нижнечелюстных суставах с ограничением подвижности в них. За три месяца мальчик похудел на 12 кг. Обследован по месту жительства: в анализе крови скорость оседания эритроцитов (СОЭ) 47–55 мм/ч, лейкоцитоз, в биохимическом анализе повышение аспартатаминотрансферазы (АСТ) до 2 норм, С-реативный белок (СРБ)++. Выявлена кишечная инфекция: титр к S. flexneri 1:400. Проводимая терапия (НПВП, антибиотики — цефазолин, цефтриаксон, амикацин) эффекта не дала. На фоне приема антибиотиков появился неустойчивый, разжиженный стул, боли в околопупочной области. В НИИ фтизиатрии исключен туберкулез. При компьютерной томографии левого голеностопного сустава выявлено: сужение суставной щели, краевая узура в медиальной лодыжке, выпот в полость сустава. Исключена ортопедическая патология. С января 2009 г. наблюдается в Университетской детской клинической больнице (УДКБ) Первого МГМУ им. И. М. Сеченова. При поступлении состояние средней степени тяжести. Бледен, выражены симптомы интоксикации. Дистрофия. Суставной синдром в виде выпота, ограничения подвижности, повышения местной температуры и болезненности в левом голеностопном суставе, ахиллобурсит слева, умеренная атрофия мышц левой голени, походка нарушена. Ригидность грудного отдела позвоночника (+ 1 см), ограничение подвижности в височно-нижнечелюстных суставах. Отмечаются боли в животе, разжиженный стул. Высокая гуморальная активность: СОЭ до 50 мм/ч, лейкоцитоз до 22 000 в 1 мкл с палочкоядерным сдвигом до 24%, анемия — гемоглобин (Hb) 109 г/л, однократно повышения уровней АСТ и аланинаминотрансферазы (АЛТ) до 1,5–2 норм. Обследован на артритогенные инфекции: результат отрицателен. При иммуногенетическом обследование выявлены HLA 1-го класс: А2, В 64 (14), В38 (16). Ребенку выставлен предварительный диагноз: ювенильный спондилоартрит. Использовали пульс-терапию глюкокортикоидами, введение внутривенного иммуноглобулина, НПВП, проведена внутрисуставная пункция левого голеностопного сустава с введением Депо-медрола. В качестве базисного препарата ребенку назначен сульфасалазин 1500 мг/сутки. На фоне проводимой терапии отмечалась положительная динамика, несколько снизилась лабораторная активность, купированы боли в животе, нормализовался стул, возрос объем движений в левом голеностопном суставе, однако сохранялась отечность и утренняя скованность в нем. В марте 2009 г. вновь обострение суставного синдрома, лихорадка до 37,8 °C, боли в животе, неустойчивый стул, появилась отечность правого голеностопного сустава. Ребенок вновь госпитализирован в УДКБ в мае-июне 2009 г.: СОЭ 29 мм/ч, гипохромная анемия, тромбоцитоз, СРБ ++, IgG 2150 мг/дл, в копрограмме эритроциты до 40 в поле зрения однократно. Выполнена ректороманоскопия: сигмоидит, проктит, эндоскопические признаки колита. На эзофагогастродуоденоскопии: эрозивный гастрит, дуоденит, еюнит. Рекомендовано проведение колоноскопии, от проведения которой родители ребенка отказались. Мальчику была повышена доза сульфасалазина до 1750 мг/сутки. Но состояние пациента оставалось нестабильным: сохранялись неустойчивый стул, отечность, болезненность и нарушение функции левого голеностопного сустава. В октябре 2009 г. вновь госпитализирован в УДКБ: СОЭ 34 мм/ч, наросла гипохромная анемия Hb 90 г/л, тромбоцитоз, лейкоцитоз до 16 тыс. в 1 мкл, СРБ ++. Ребенку проведена колоноскопия: болезнь Крона, глубокие язвы в ободочной кишке, язвенный терминальный илеит, проктит, колит, сигмоидит. По данным магнитно-резонасной томографии илеосакральных сочленений — левосторонний сакроилеит. Мальчику проводилась коррекция терапии: сульфасалазин отменен, назначен Салофальк 2000 мг/сутки, продолжал получать НПВП. На фоне терапии состояние с положительным эффектом — купирован кишечный синдром, нормализовался стул. Однако в декабре 2009 г. после ОРВИ вновь обострение основного заболевания: повышение температуры до фебрильных цифр, СОЭ 50 мм/ч, отек голеностопных суставов, скованность в них. С конца декабря 2009 г. отмечаются схваткообразные боли в животе, разжиженный стул. В январе 2010 г. в связи с высокой лабораторной и клинической активностью основного заболевания, неэффективностью традиционной терапии (монотерапии Салофальком), прогрессирующей инвалидизацией пациента начата терапия инфликсимабом. 3.02.2010 г. проведено первое введение, на фоне которого отмечена выраженная положительная динамика, купирован кишечный синдром, возрос объем движений в голеностопных суставах, уменьшилась экссудация в них, снизилась активность лабораторных показателей. 17.02.2010 и 17.03.2010 проведены второе и третье внутривенное введение Ремикейда по 100 мг на 1 введение. На фоне лечения отчетливая положительная динамика, полностью купирован кишечный синдром, прибавил в весе 7 кг, однако сохранялось снижение Hb до 87 г/л. При госпитализации в мае-июле 2010 г. СОЭ 23 мм/ч, Hb 91 г/л. При повторной колоноскопии выявлено сужение поперечной ободочной кишки, не проходимое для эндоскопа. Проведена ирригоскопия: слепая, восходящая, 1/2 поперечной кишок деформированы, с выраженным спазмом, с постстенотическим расширением поперечной и нисходящей ободочной кишки. Продолжилась терапия инфликсимабом, с учетом увеличения веса пациента доза повышена. Всего мальчик получил 24 введений инфликсимаба. Состояние его полностью стабилизировалось. Он поправился на 22 кг, вырос на 25 см. Полностью купированы кишечный и суставные синдромы. Полностью нормализовались лабораторные показатели СОЭ 5–14 мм/час. Hb 151 г/л. Мальчик ведет активный образ жизни.
Литература
- Яблокова Е. А. Клинические особенности и нарушение минерализации костной ткани у детей с воспалительными заболеваниями кишечника. Дисс. канд. мед. наук. М., 2006. 185 с.
- Tourtelier Y., Dabadie A., Tron I., Alexandre J. L., Robaskiewicz M., Cruchant E., Seyrig J. A., Heresbach D., Bretagne J. F. Incidence of inflammatory bowel disease in children in Britani (1994 –1997). Breton association of study and research on digestive system diseases (Abermad) // Arch Pediatr. 2000 Apr; 7 (4): 377–384.
- Гвидо Адлер. Болезнь Крона и язвенный колит. М.: ГЭОТАР-МЕД, 2001.
- Шостак Н. А., Правдюк Н. Г., Абельдяев Д. В. Серонегативные спондилоартропатии — совершенствование подходов к ранней диагностике и лечению // РМЖ. 2013, № 6, 1002–1008.
- Справочник по ревматологии / Хаким А., Клуни Г., Хак И.; пер. с англ. Н. И. Татаркиной. М.: ГЭОТАР-Медиа, 2010. 560 с.
- Dougados M., Hermann K. G., Landewe R. et al. Assess spondyloarthritis to international Society (ASAS) handbook: a guide The Assessment of spondyloArthritis // Ann Rheum Dis. 2009. Vol. 68. Р. 1–44.
- Ревматология. Национальное руководство под ред. Е. Л. Насонова, В. А. Насоновой. М.: ГЭОТАР-Медиа, 2008. 720 с.
- D’Incà R., Podswiadek M., Ferronato A., Punzi L., Salvagnini M., Sturniolo G. C. Articular manifestation in inflammatory bowel disease patients. A prospective study // Dig Liver Dis. 2009, Mar 9.
- Rodriguez V. E., Costas P. J., Vazquez M., Alvarez G., Perez-Kraft G., Climent C., Nazario C. M. Prevalence of spondyloarthropathy in Puerto Rican patients with inflammatory bowel disease/Ethn Dis. 2008, Spring; 18 (2 Suppl 2): S2–225–9.
- Руководство по детской ревматологии / под ред. Н. А. Геппе, Н. С. Подчерняевой, Г. А. Лыскиной. М.: ГЕОТАР-Медиа, 2012. 720 с.
А. В. Мелешкина1, кандидат медицинских наук
С. Н. Чебышева, кандидат медицинских наук
Е. С. Жолобова, доктор медицинских наук, профессор
М. Н. Николаева
ГБОУ ВПО Первый МГМУ им. И. М. Сеченова МЗ РФ, Москва
1 Контактная информация: meleshkina.angel@mail.ru
Abstract. The article covers specifics of development of articular manifestations under chronic inflammatory bowel diseases and provides clinical example of crohn’s disease development starting with un-bowel manifestations in forn of articular syndrome.
Купить номер с этой статьей в pdf
