Клинические проявления воспаления жар


Воспаление

Клинические признаки воспаления ВОСПАЛЕНИЕ жар покраснение опухоль боль нарушение функции
Воспаление: покраснение и отек

Воспаление: реакция живой ткани на повреждение, заключающаяся в определенных изменениях терминального сосудистого ложа, крови и соединительной ткани, направленных на уничтожение агента, вызывающего повреждение, и на восстановление поврежденной ткани

Причины воспаления: Физические факторы: • травма (разрезы, уколы, укусы, ушибы, вибрация, воздействие шума, сдавление) • ионизирующая, ультрафиолетовая радиация • электрическая энергия • высокие (огонь) и низкие (холод) температуры Химические факторы: • кислоты • щелочи • минеральные и органические вещества • эндогенные токсины (желчные кислоты, продукты азотистого обмена) Биологические факторы: • вирусы • бактерии • грибы • животные паразиты • циркулирующие в крови антитела и активированные иммунные комплексы
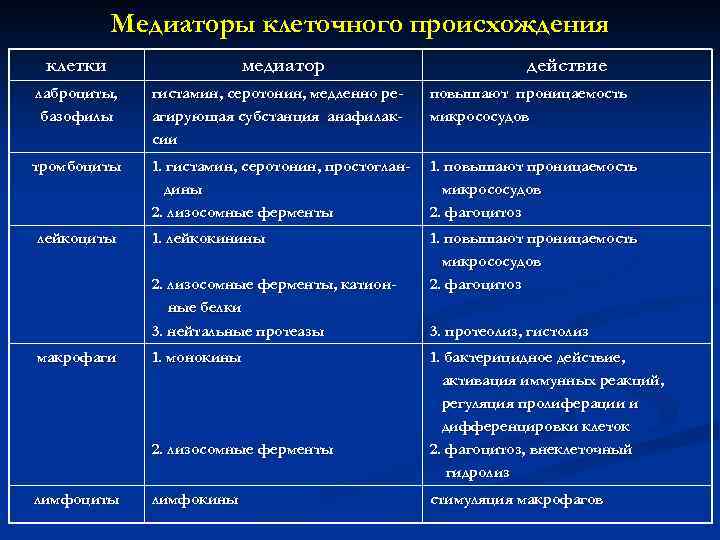
Медиаторы клеточного происхождения клетки медиатор действие лаброциты, базофилы гистамин, серотонин, медленно реагирующая субстанция анафилаксии повышают проницаемость микрососудов тромбоциты 1. гистамин, серотонин, простогландины 2. лизосомные ферменты 1. повышают проницаемость микрососудов 2. фагоцитоз 1. лейкокинины 1. повышают проницаемость микрососудов 2. фагоцитоз лейкоциты 2. лизосомные ферменты, катионные белки 3. нейтальные протеазы макрофаги 1. монокины 2. лизосомные ферменты лимфоциты лимфокины 3. протеолиз, гистолиз 1. бактерицидное действие, активация иммунных реакций, регуляция пролиферации и дифференцировки клеток 2. фагоцитоз, внеклеточный гидролиз стимуляция макрофагов

Медиаторы гуморального происхождения система плазмы крови медиатор действие калликреинкининовая 1. кинины (брадикардин) 2. каллекреины 1. повышает проницаемость сосудов, болевая реакция 2. активируют хемотаксис лейкоцитов и фактор Хагемана свертывающая и противосвертывающая 1. фактор Хагемана 1. активирует кининовую систему 2. плазмин 2. повышает проницаемость сосудов комплементарная С 3 b и С 5 b компоненты комплемента активируют хемотаксис лейкоцитов и фактор Хагемана, стимулируют фагоцитоз
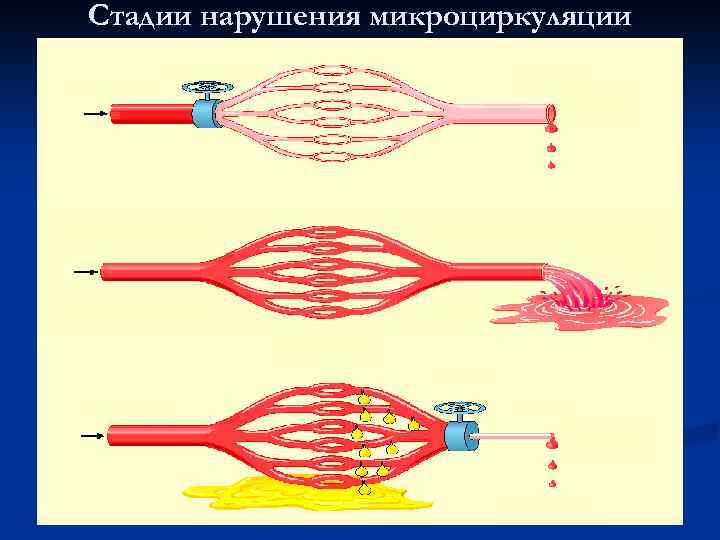
Стадии нарушения микроциркуляции
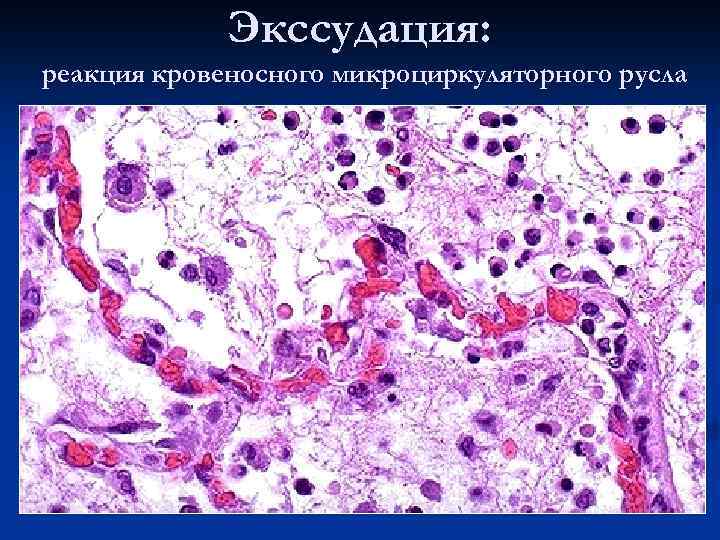
Экссудация: реакция кровеносного микроциркуляторного русла
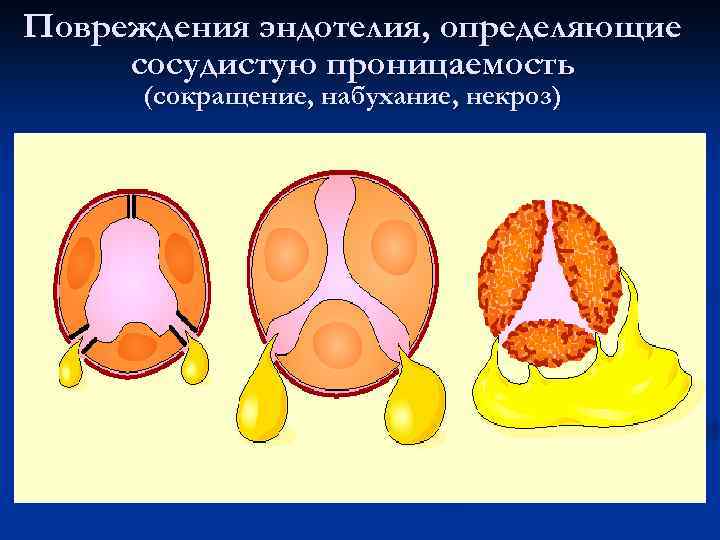
Повреждения эндотелия, определяющие сосудистую проницаемость (сокращение, набухание, некроз)
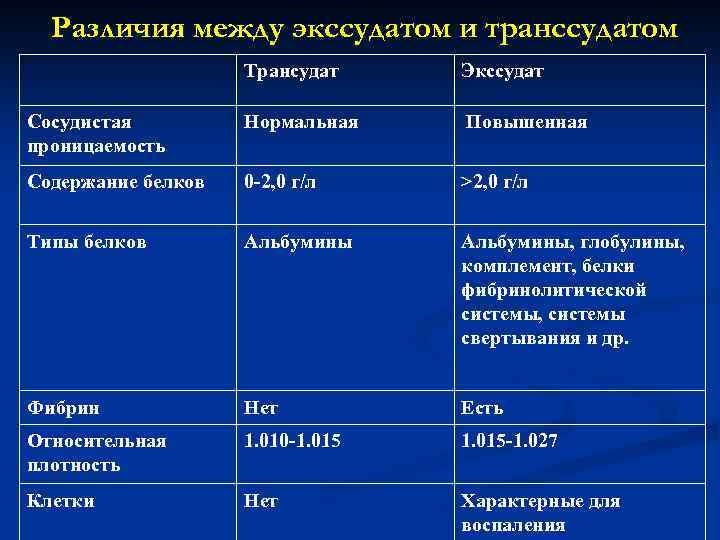
Различия между экссудатом и транссудатом Трансудат Экссудат Сосудистая проницаемость Нормальная Повышенная Содержание белков 0 -2, 0 г/л >2, 0 г/л Типы белков Альбумины, глобулины, комплемент, белки фибринолитической системы, системы свертывания и др. Фибрин Нет Есть Относительная плотность 1. 010 -1. 015 -1. 027 Клетки Нет Характерные для воспаления
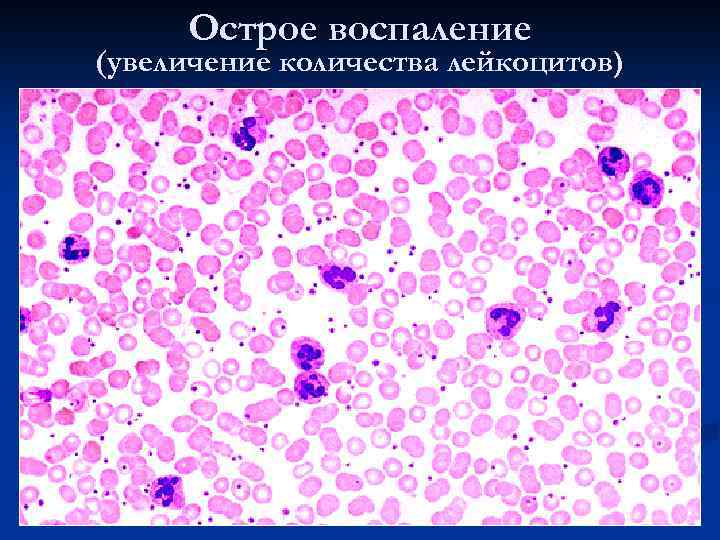
Острое воспаление (увеличение количества лейкоцитов)
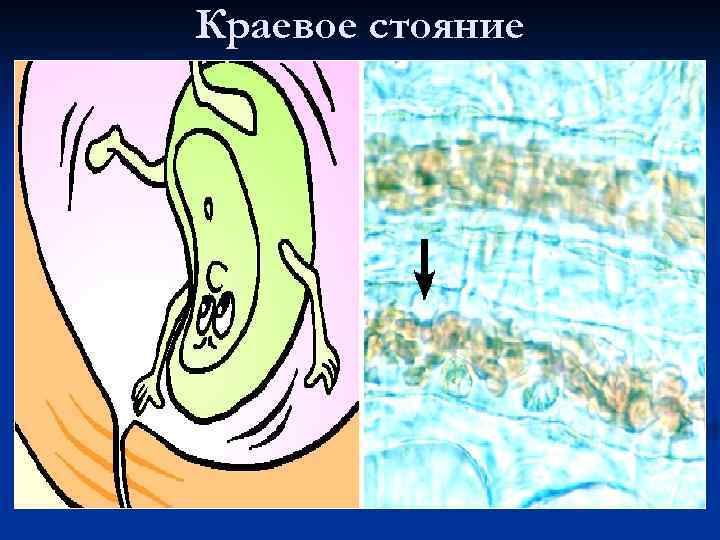
Краевое стояние
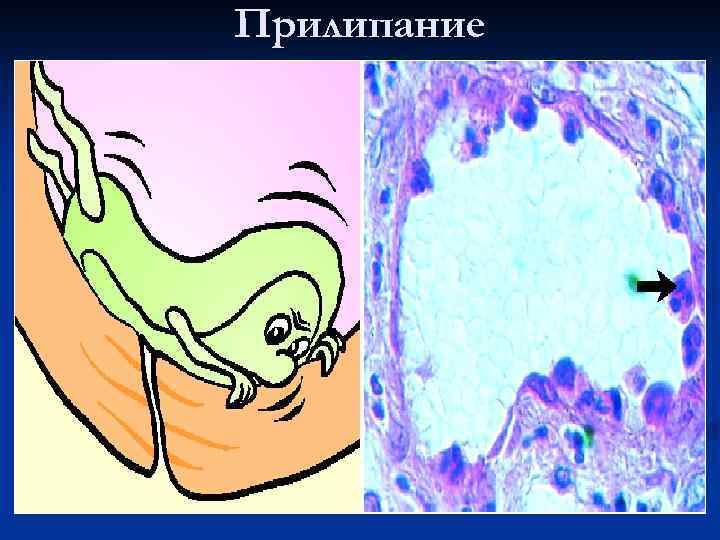
Прилипание
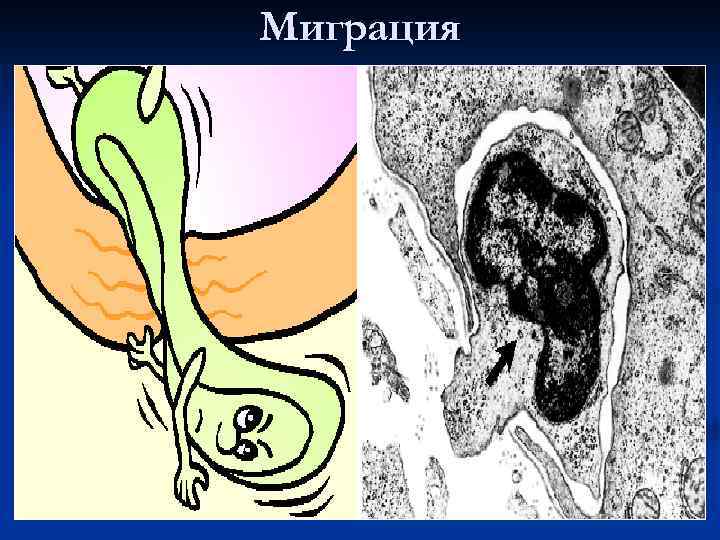
Миграция
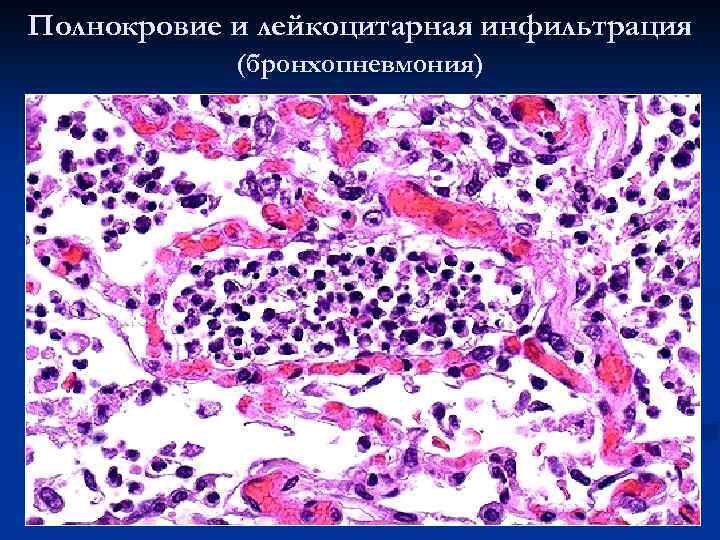
Полнокровие и лейкоцитарная инфильтрация (бронхопневмония)

Стадии фагоцитоза: 1. Распознавание 2. Поглощение 3. Разрушение микроорганизмов
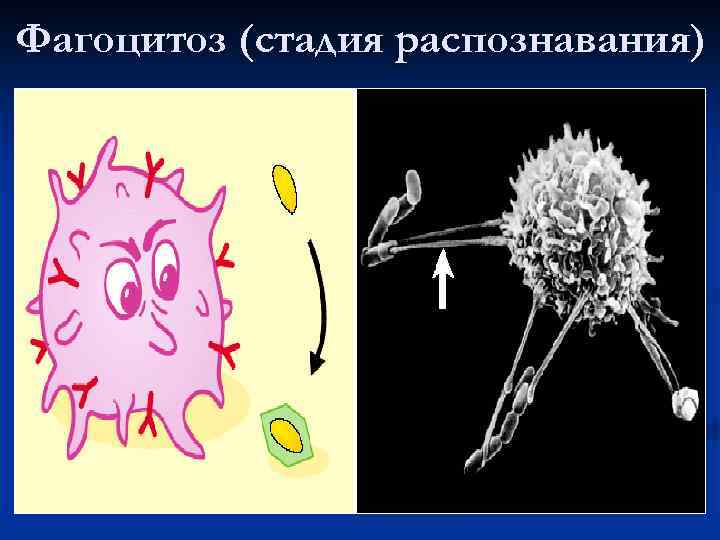
Фагоцитоз (стадия распознавания)
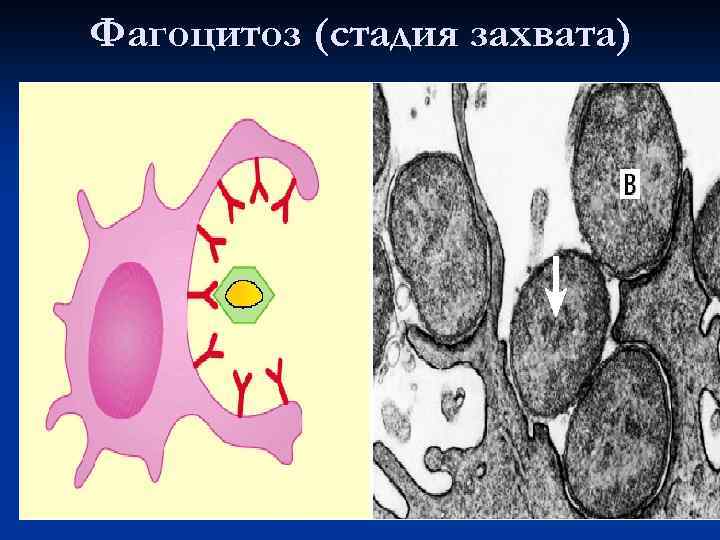
Фагоцитоз (стадия захвата)
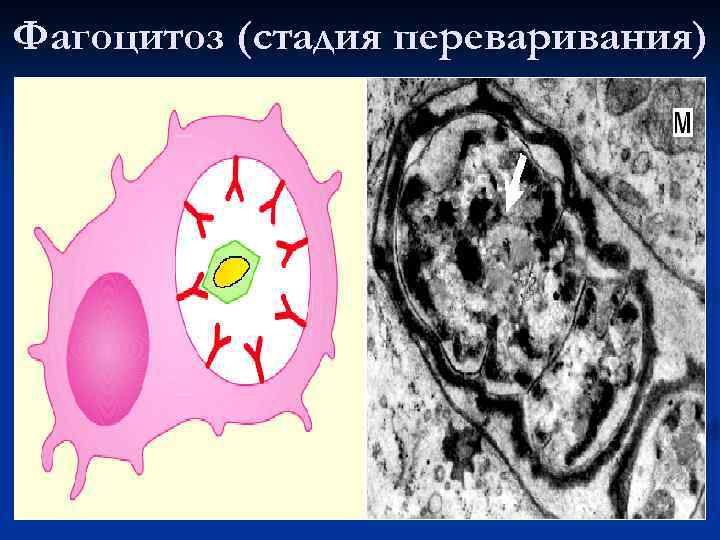
Фагоцитоз (стадия переваривания)
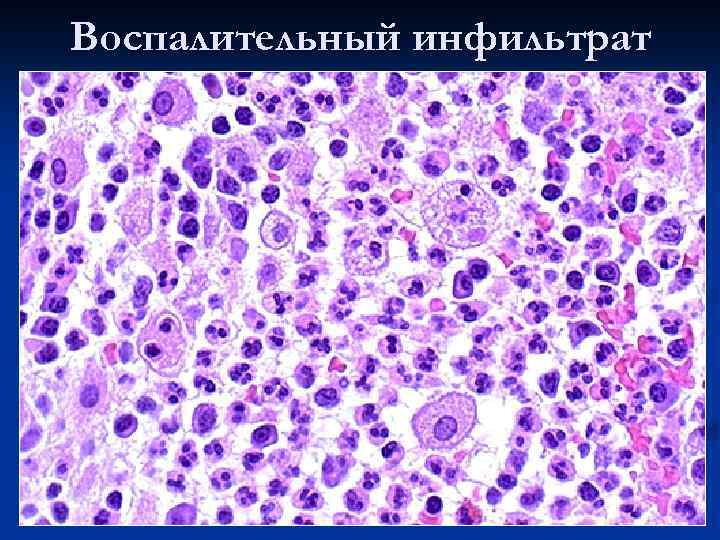
Воспалительный инфильтрат

Классификация воспаления: 1. По морфологии: — экссудативное — пролиферативное 2. По течению: — острое (до 2 мес. ) — подострое (до 6 мес. ) — хроническое (протекает годами) 3. По локализации в органе: — паренхиматозное — интерстициальное (межуточное) — смешанное 4. По типу тканевой реакции: — неспецифическое (банальное) — специфическое

Виды экссудативного воспаления: n Серозное n Фибринозное n Гнойное n Гнилостное (ихорозное) n Геморрагическое n Катаральное n Смешанное
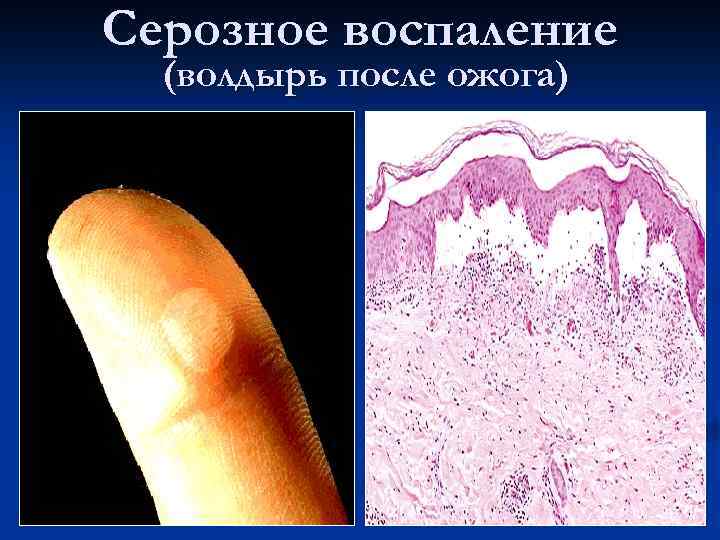
Серозное воспаление (волдырь после ожога)
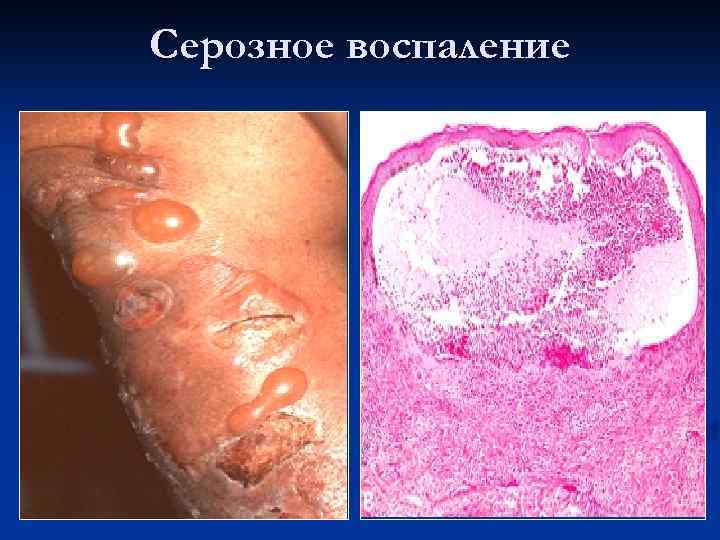
Серозное воспаление
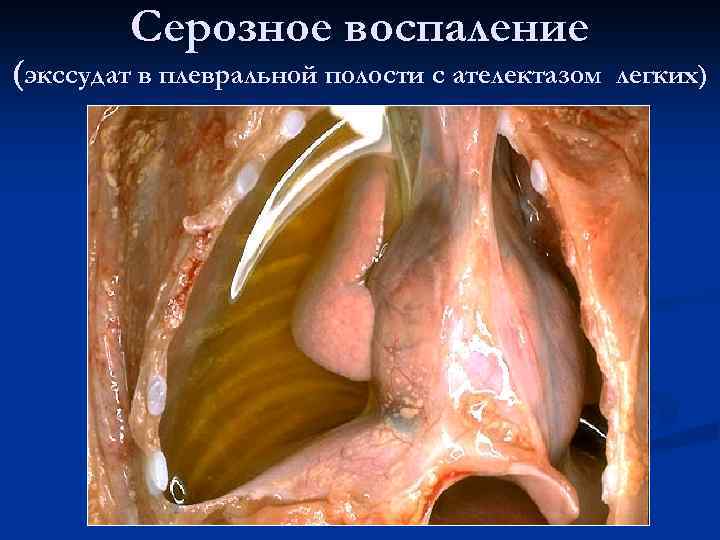
Серозное воспаление (экссудат в плевральной полости с ателектазом легких)
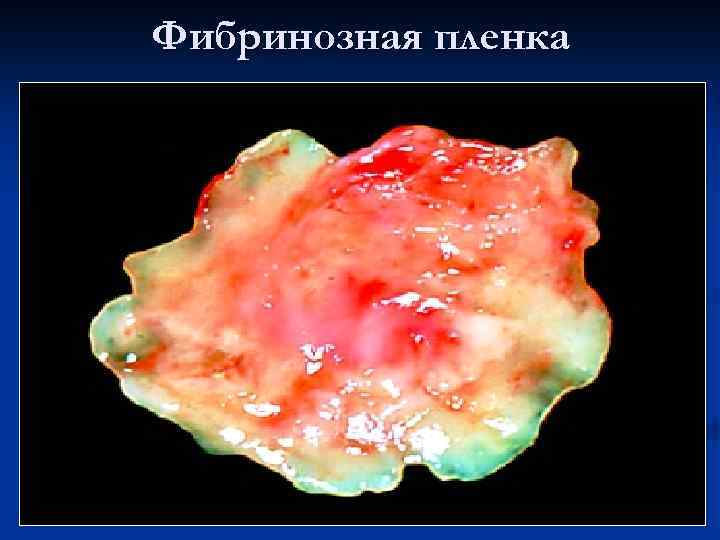
Фибринозная пленка
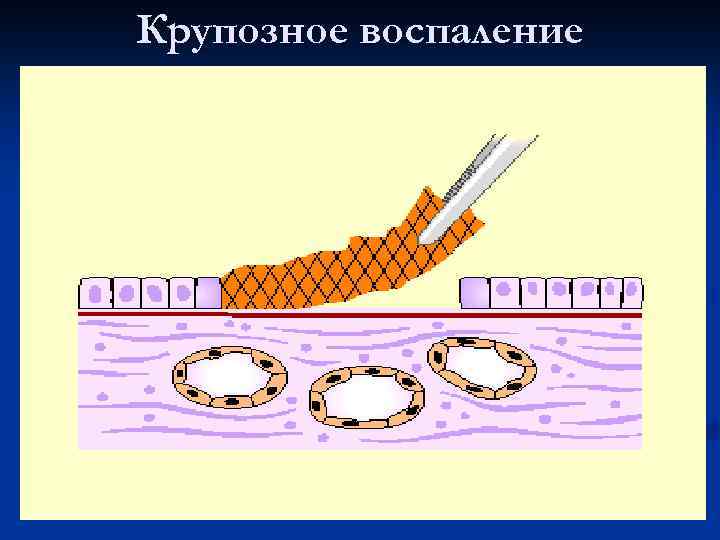
Крупозное воспаление
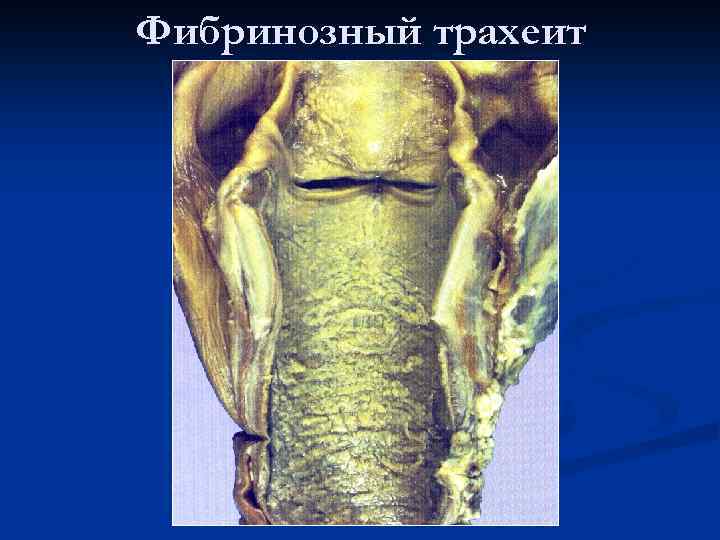
Фибринозный трахеит

Фибринозное воспаление (колит)
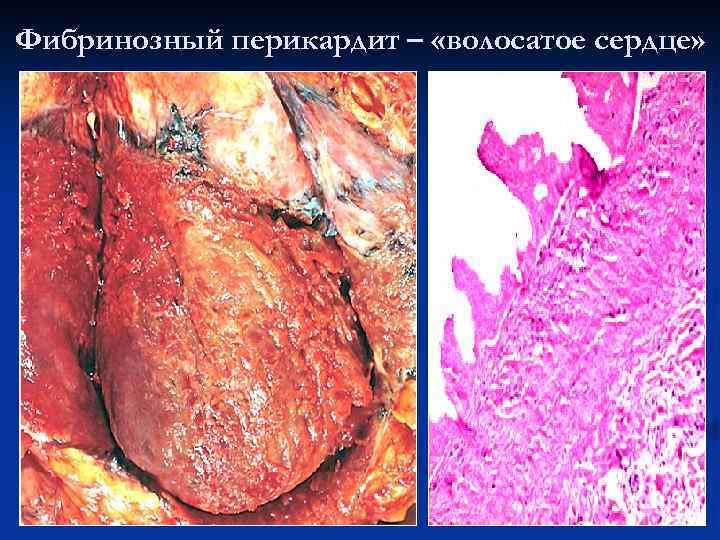
Фибринозный перикардит – «волосатое сердце»
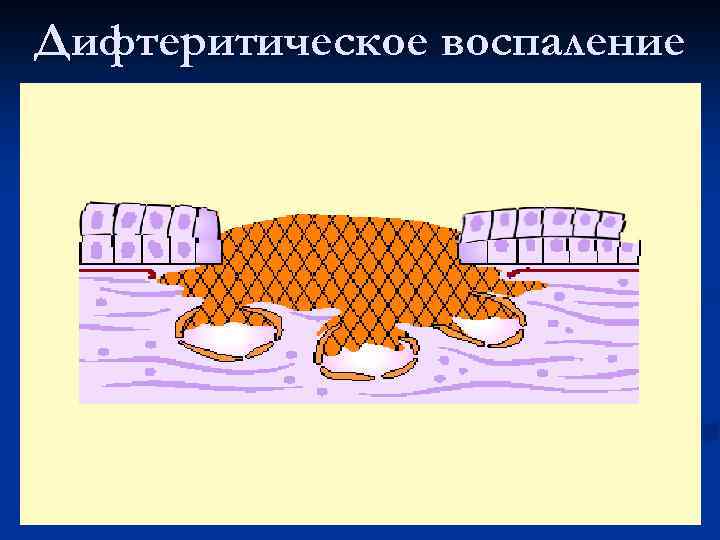
Дифтеритическое воспаление
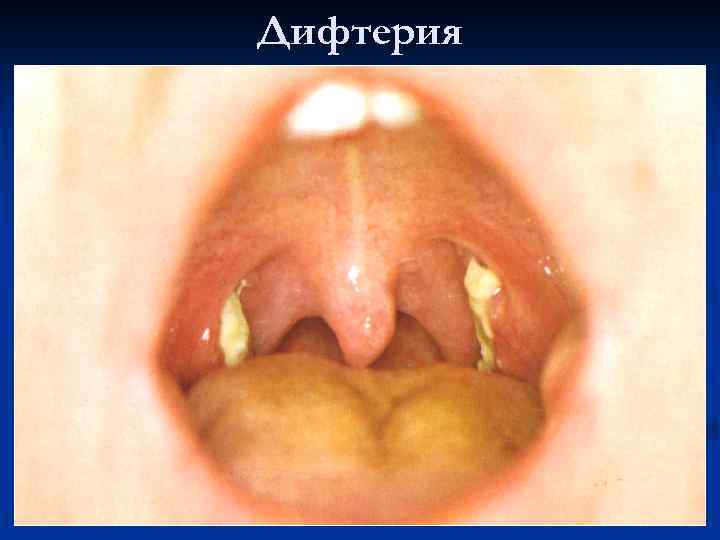
Дифтерия
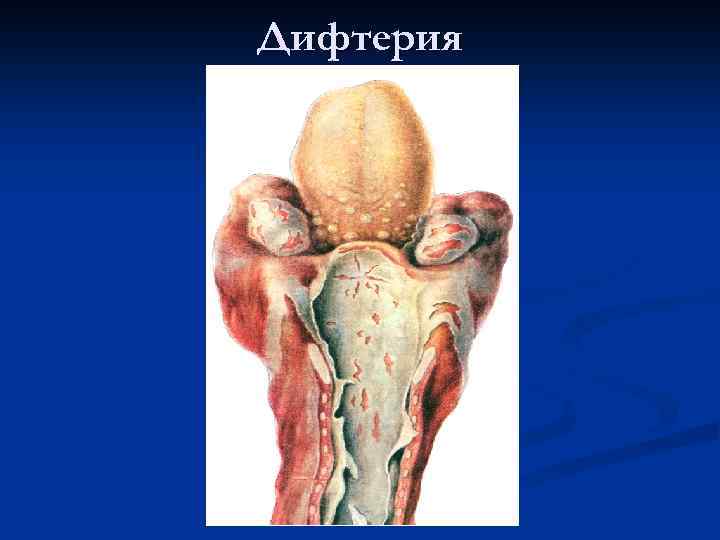
Дифтерия
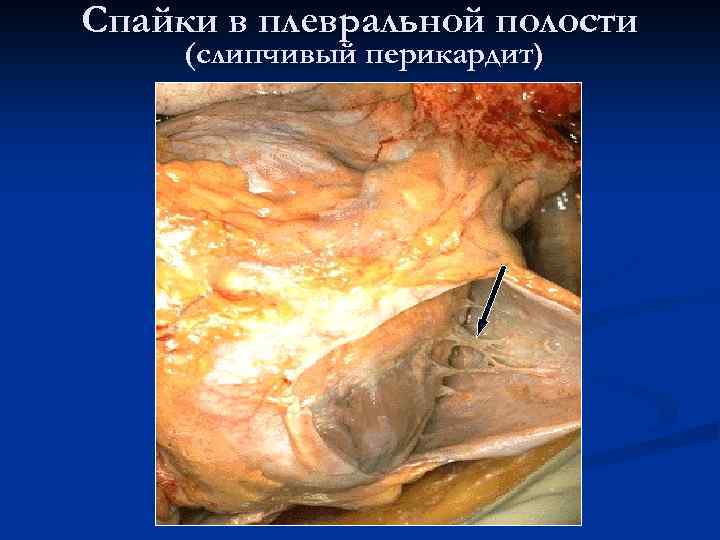
Спайки в плевральной полости (слипчивый перикардит)

Виды гнойного воспаления: n n n Фурункул Карбункул Абсцесс Флегмона Эмпиема Гнойная рана
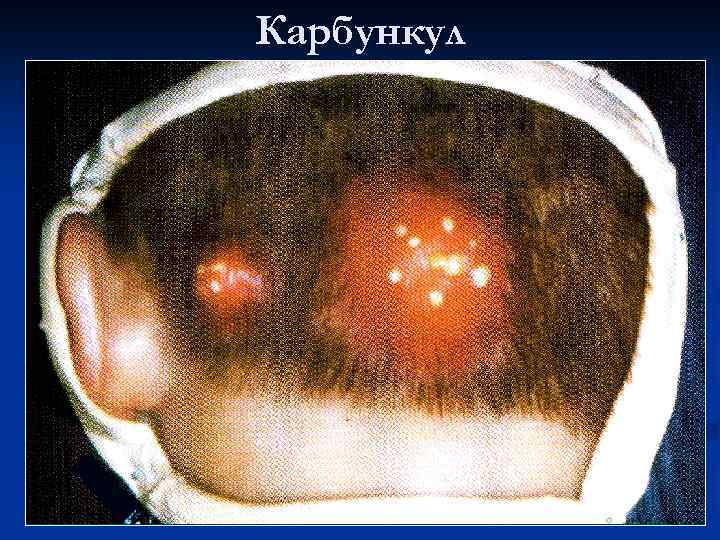
Карбункул
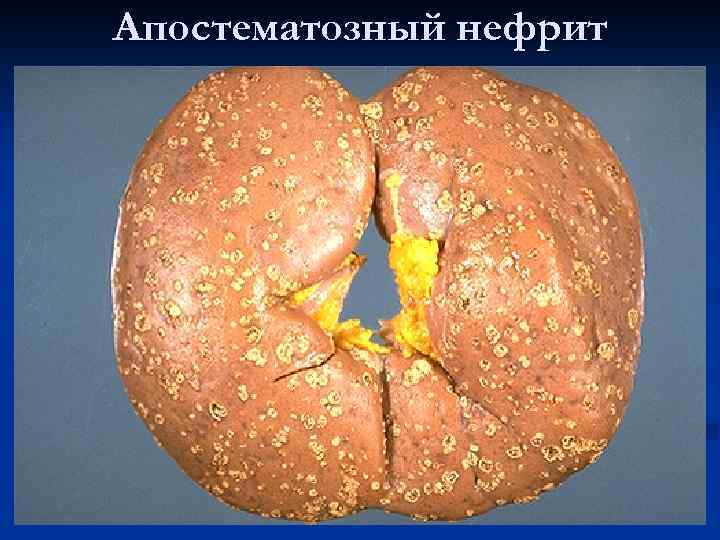
Апостематозный нефрит
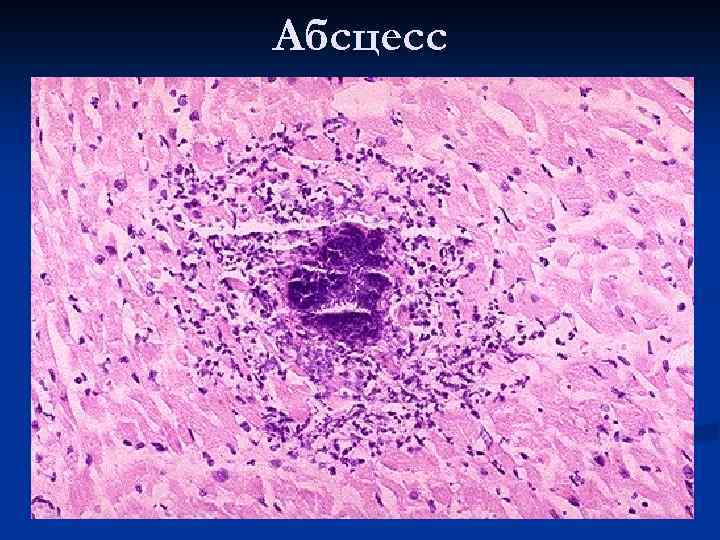
Абсцесс
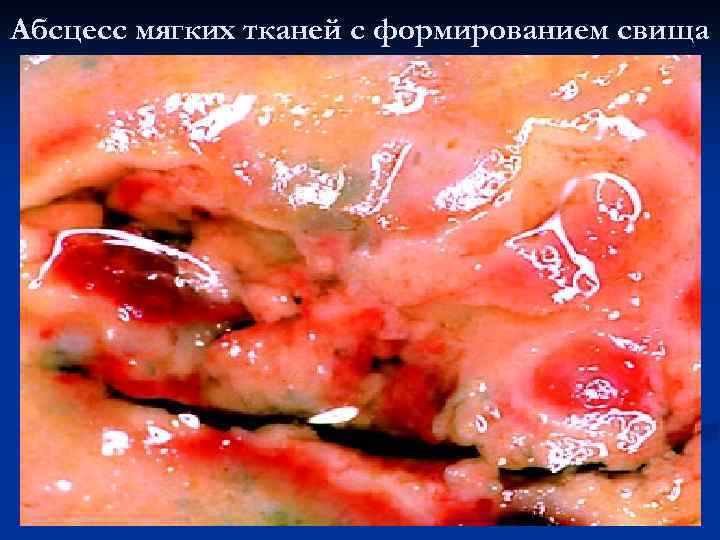
Абсцесс мягких тканей с формированием свища

Абсцесс легкого
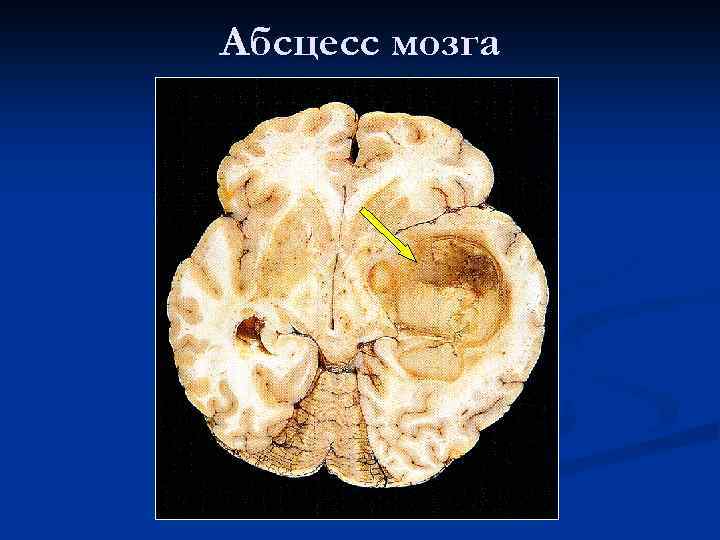
Абсцесс мозга
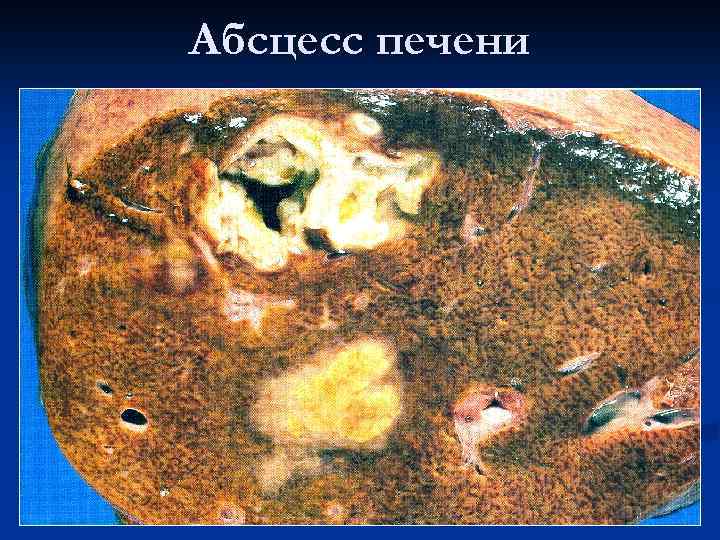
Абсцесс печени
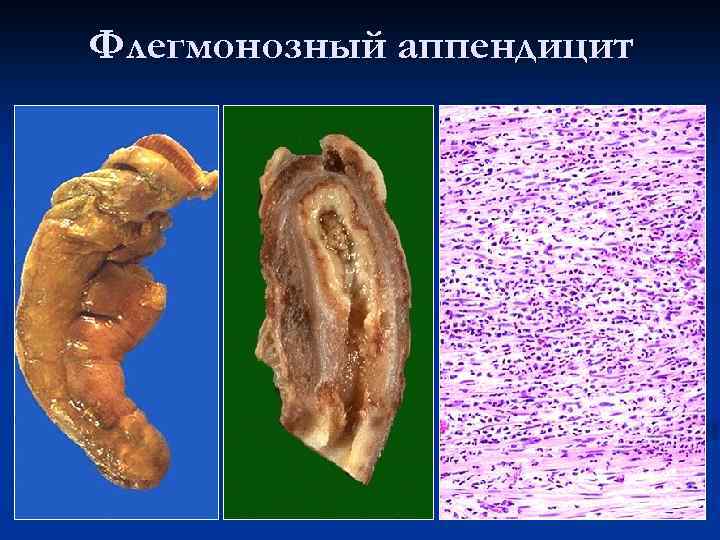
Флегмонозный аппендицит
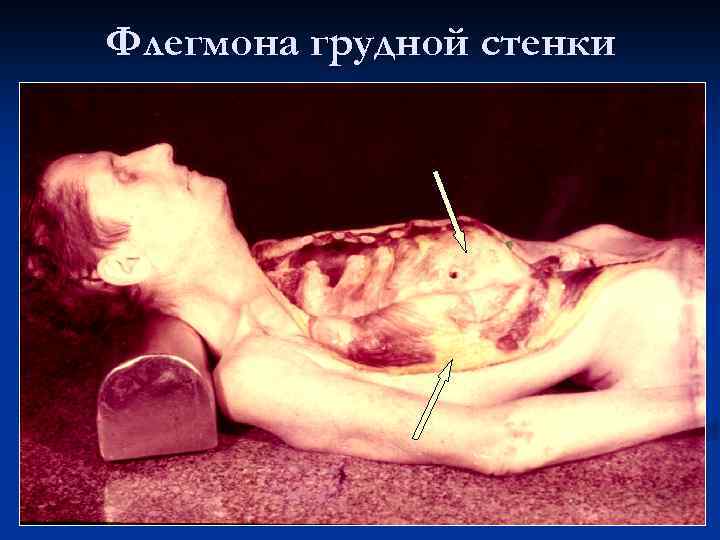
Флегмона грудной стенки

Примеры флегмон: n n n n Паронихий — острое гнойное воспаление околоногтевой клетчатки Панариций — острое гнойное воспаление подкожной клетчатки пальца Флегмона шеи — острое гнойное воспаление клетчатки шеи, развивается как осложнение гноеродных инфекций миндалин, челюстно-лицевой системы Медиастинит — острое гнойное воспаление клетчатки средостения Паранефрит — гнойное воспаление околопочечной клетчатки осложнение гнойного нефрита, септического инфаркта почек, распадающихся опухолей почек Параметрит — гнойное воспаление околоматочной клетчатки. Встречается при септических абортах, инфицированных родах, распаде злокачественных опухолей Парапроктит — воспаление клетчатки, окружающей прямую кишку. Причинами его могут быть дизентерийные язвы, язвенный колит, распадающиеся опухоли, трещины заднего прохода, геморрой
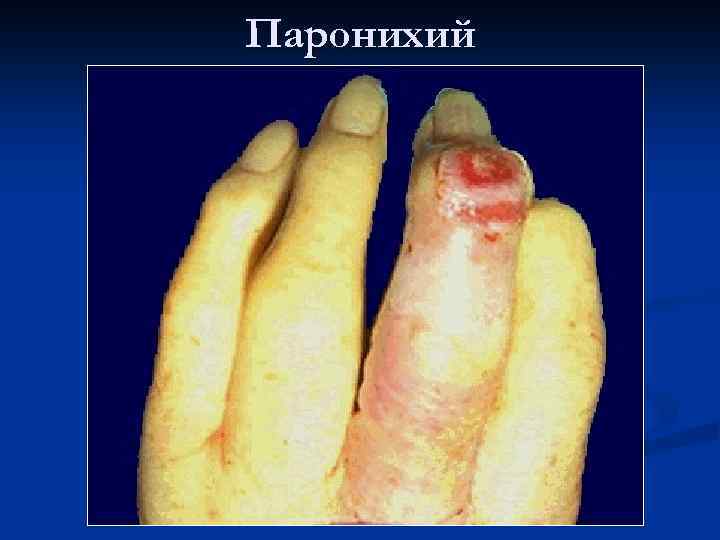
Паронихий
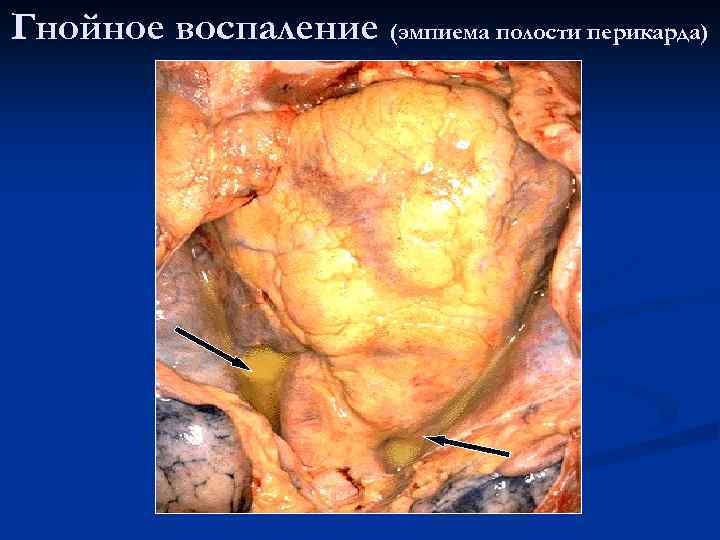
Гнойное воспаление (эмпиема полости перикарда)
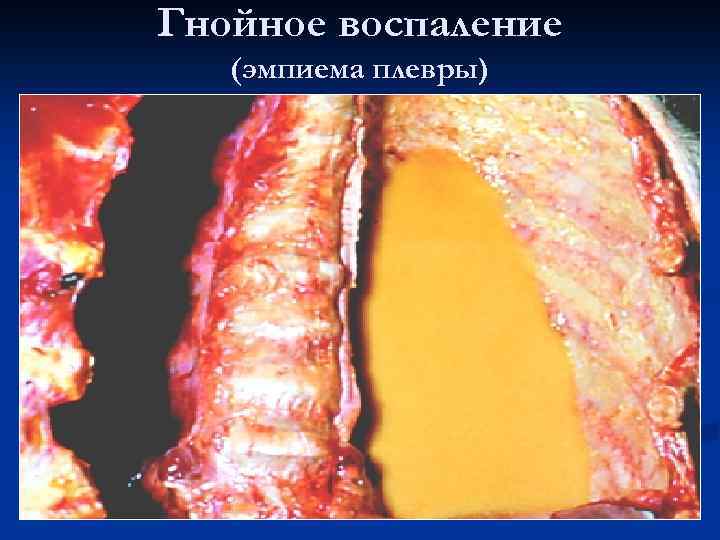
Гнойное воспаление (эмпиема плевры)
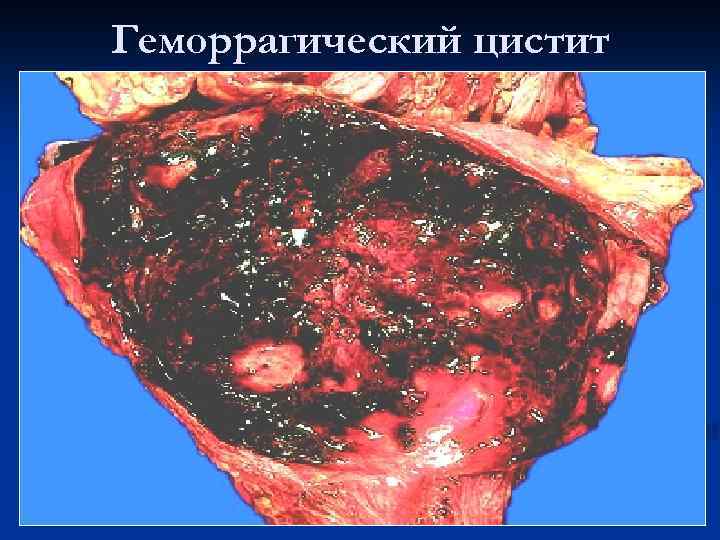
Геморрагический цистит
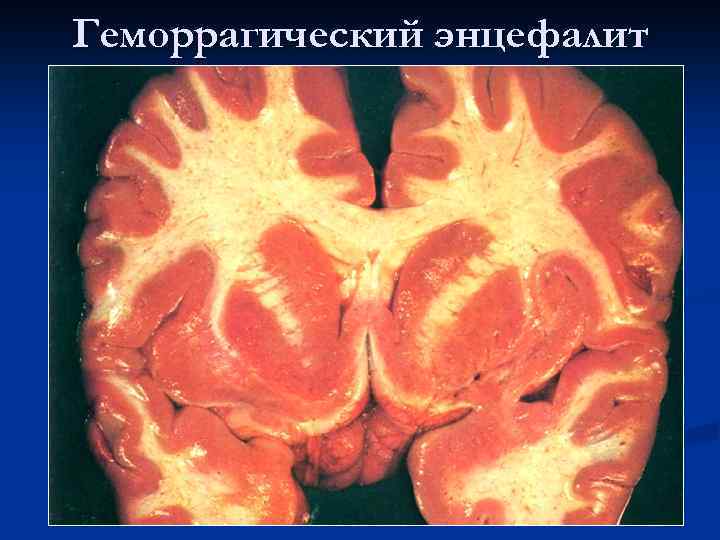
Геморрагический энцефалит

Геморрагическое воспаление (сибирская язва)
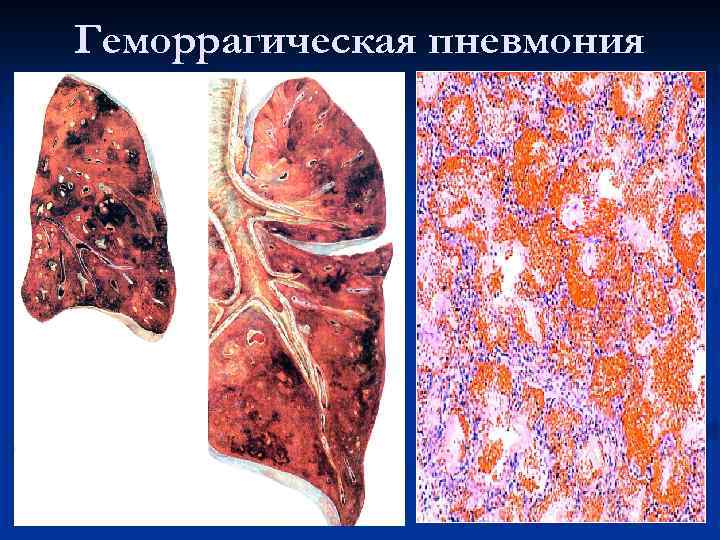
Геморрагическая пневмония
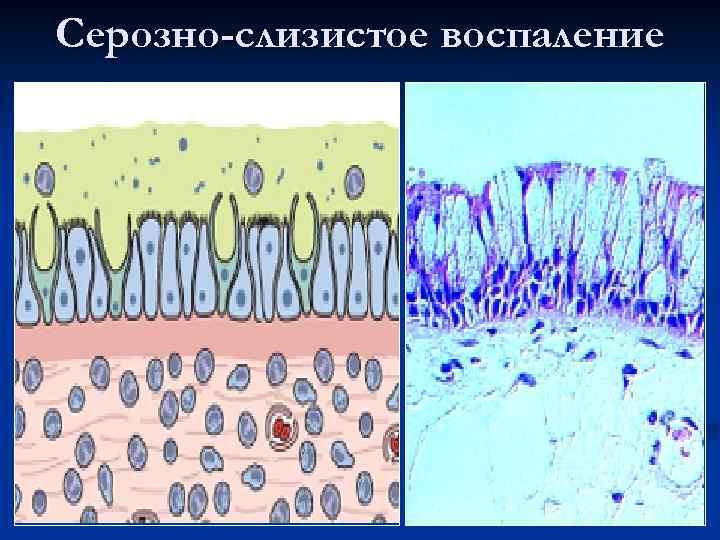
Серозно-слизистое воспаление
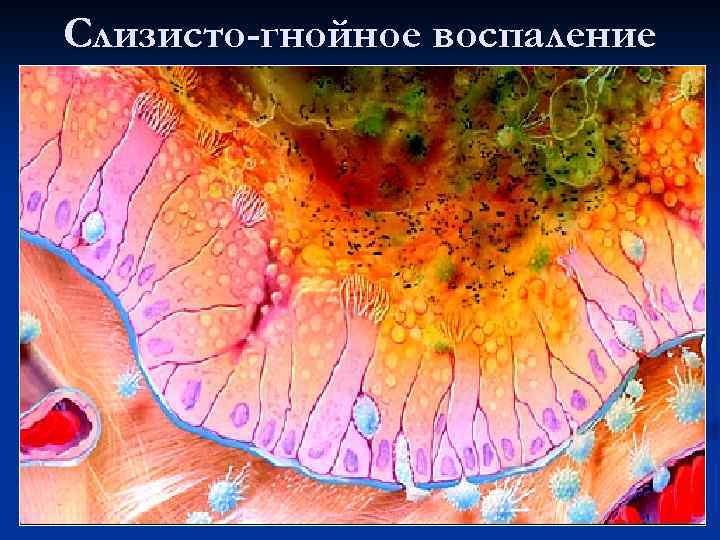
Слизисто-гнойное воспаление
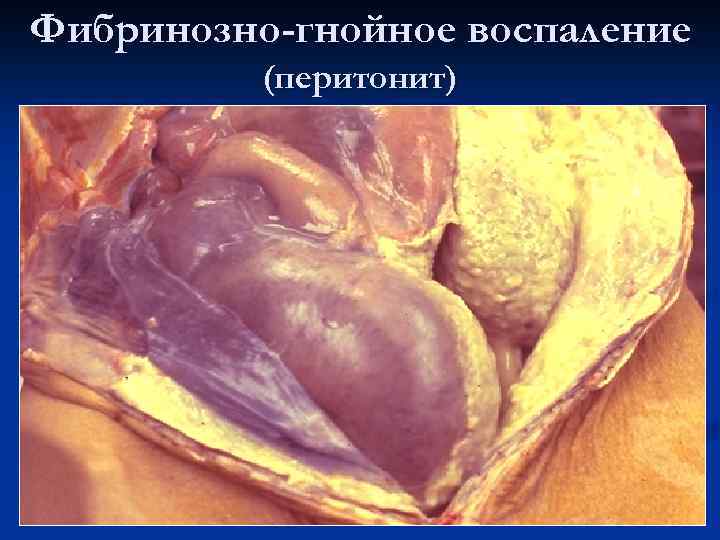
Фибринозно-гнойное воспаление (перитонит)

Исходы острого воспаления: n n n разрешение: при неосложненном остром воспалении ткань возвращается к нормальной жизнедеятельности путем разжижения и удаления экссудата и клеточного детрита макрофагами и лимфатической системой если при остром воспалении резко выражен некроз ткани, то восстановление ее происходит путем регенерации или замещения соединительной тканью с формированием рубца когда повреждающий агент не нейтрализуется при остром воспалительном ответе, развивается иммунный ответ, который приводит к развитию хронического воспаления

В тканях, поврежденных хроническим воспалением обнаруживаются: иммунный ответ: присутствие лимфоцитов, плазматических клеток и макрофагов n фагоцитоз: иммунный и неиммунный осуществляется макрофагами n некроз: затрагивает только рассеянные единичные клетки или может быть обширным n восстановление (регенерация): характеризуется формированием новых кровеносных сосудов и накоплением коллагена (фиброз) n

Виды пролиферативного воспаления: межуточное (интерстициальное) n гранулематозное n воспаление вокруг животных паразитов и инородных тел (как n разновидность гранулематозного) n гиперпластические (гиперрегенераторные) разрастания (воспаление с образованием полипов и остроконечных кондилом)
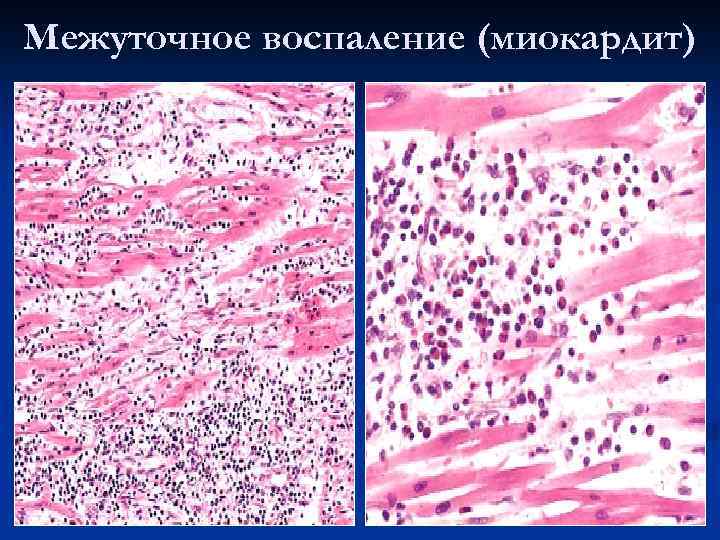
Межуточное воспаление (миокардит)

Морфогенез гранулем: накопление моноцитарных фагоцитов в очаге повреждения ткани n созревание моноцитов в макрофаги и образование макрофагальной гранулемы n созревание и трансформация моноцитарных фагоцитов и макрофагов в эпителиоидные клетки и образование эпителиоидно-клеточной гранулемы n трансформация эпителиоидных клеток в гигантские и формирование гигантоклеточной гранулемы n
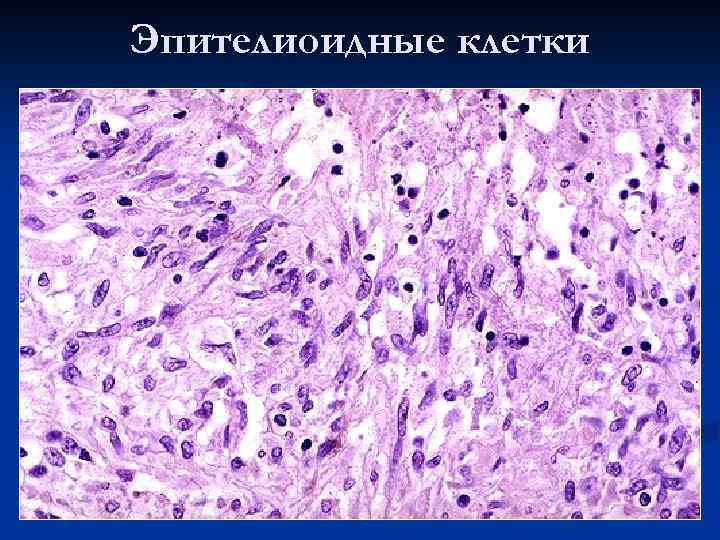
Эпителиоидные клетки
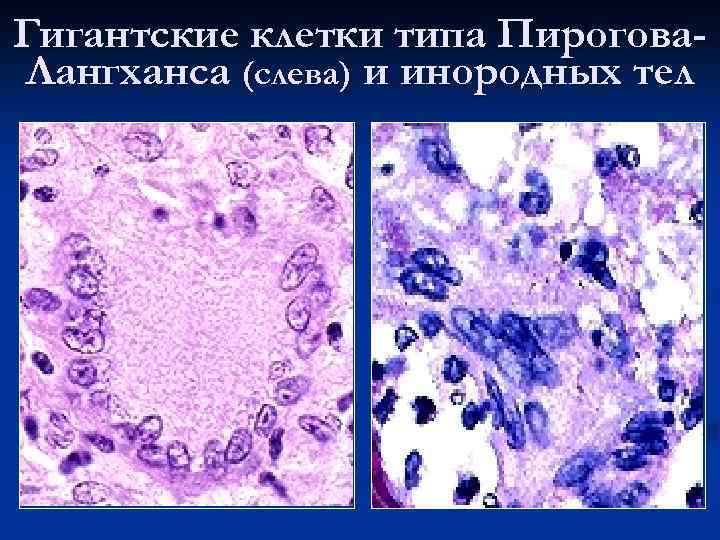
Гигантские клетки типа Пирогова. Лангханса (слева) и инородных тел

Виды гранулем: n n n инфекционные: микобактериальные (туберкулез, проказа и др. ), бруцеллезные, туляремические, хламидиозные (лимфогранулема), при болезни кошачьих царапин, при поражении грибами (кокцидоз, криптококкоз, гистоплазмоз), вызванные трепонемой (пинта, фрамбезия, сифилис), паразитические (шистоматоз) инородных тел: вызванные твердыми частицами (стекло, металл, песок), синтетическими материалами (хирургические швы), растительными веществами (целлюлоза) и при интоксикации бериллием идиопатические (причина неизвестна), нпример, саркоидоз с образованием эпителиоидноклеточных гранулем в легких, печени, селезенке, лимфоузлах, коже
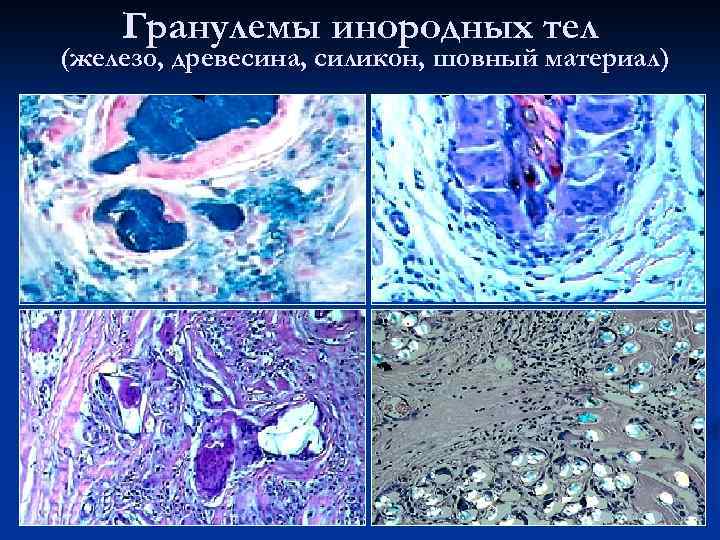
Гранулемы инородных тел (железо, древесина, силикон, шовный материал)
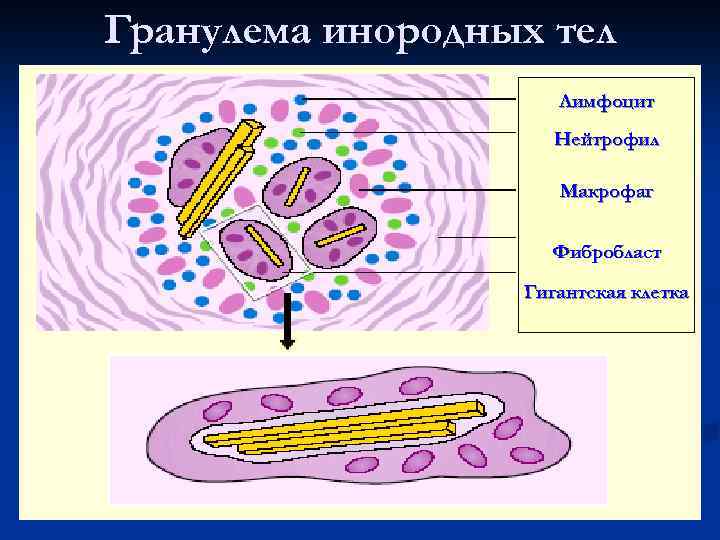
Гранулема инородных тел Лимфоцит Нейтрофил Макрофаг Фибробласт Гигантская клетка
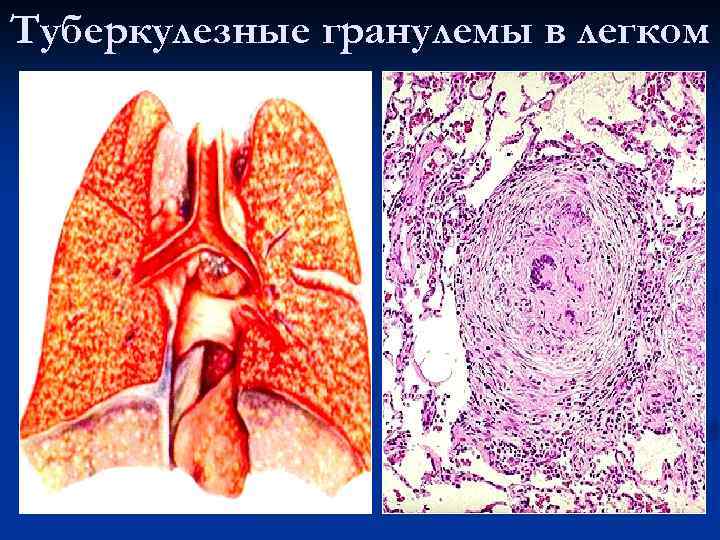
Туберкулезные гранулемы в легком
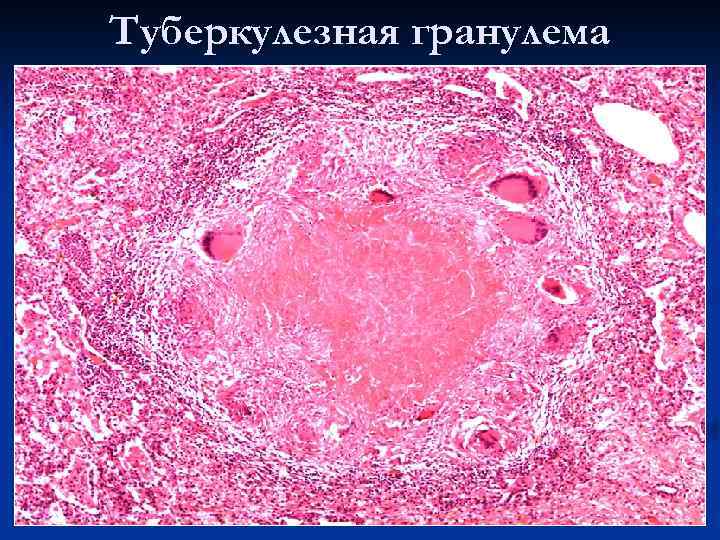
Туберкулезная гранулема
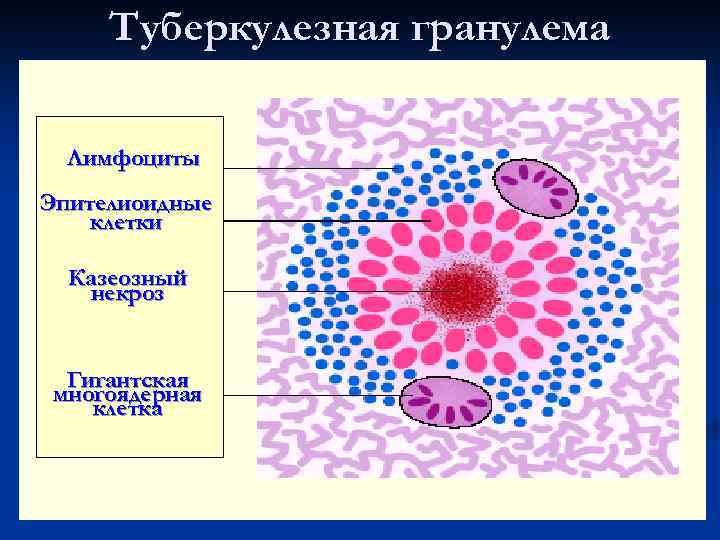
Туберкулезная гранулема Лимфоциты Эпителиоидные клетки Казеозный некроз Гигантская многоядерная клетка
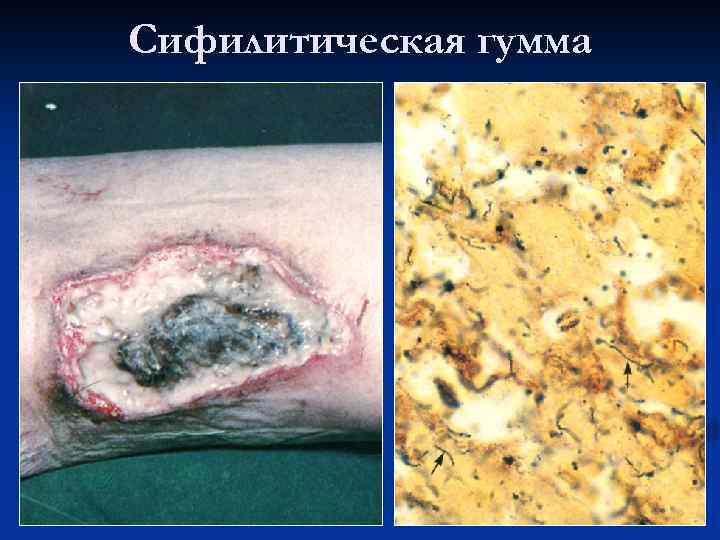
Сифилитическая гумма
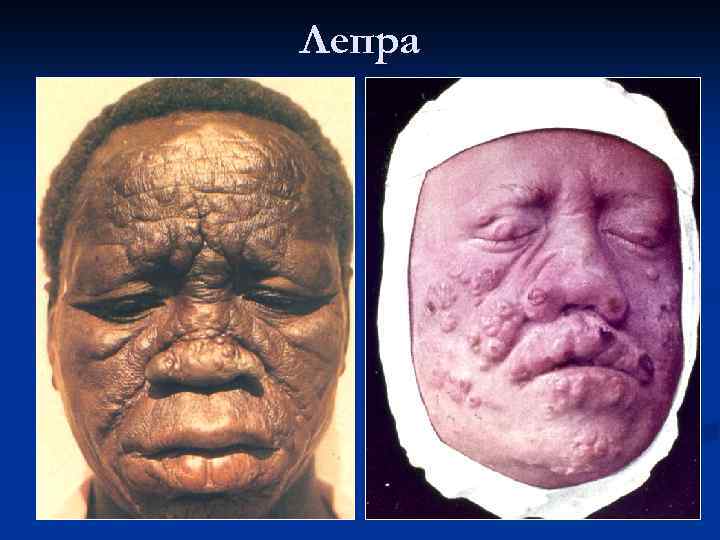
Лепра
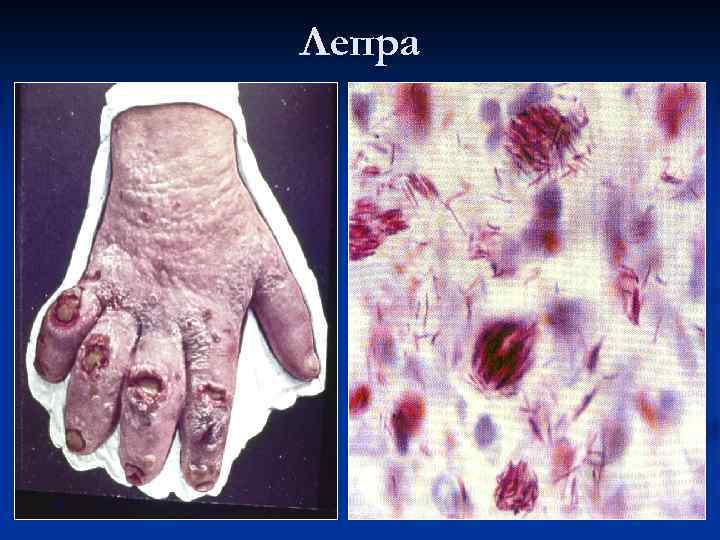
Лепра
Склерома

Продуктивное воспаление (трихинеллез)
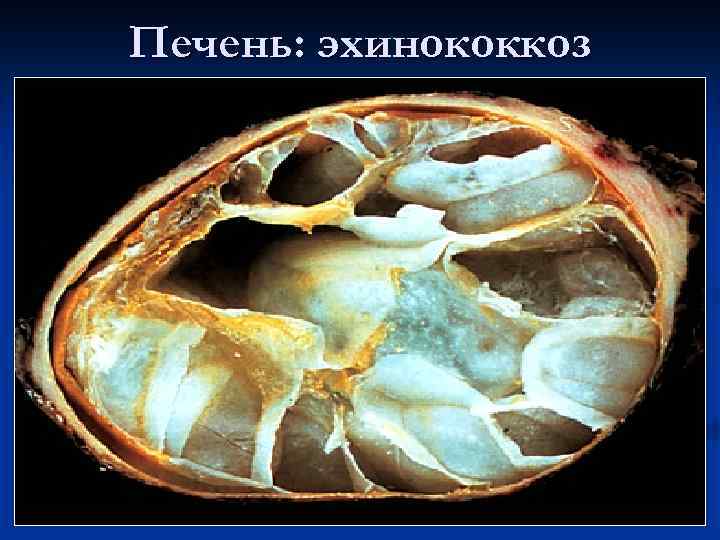
Печень: эхинококкоз

Продуктивное воспаление (эхинококкоз)
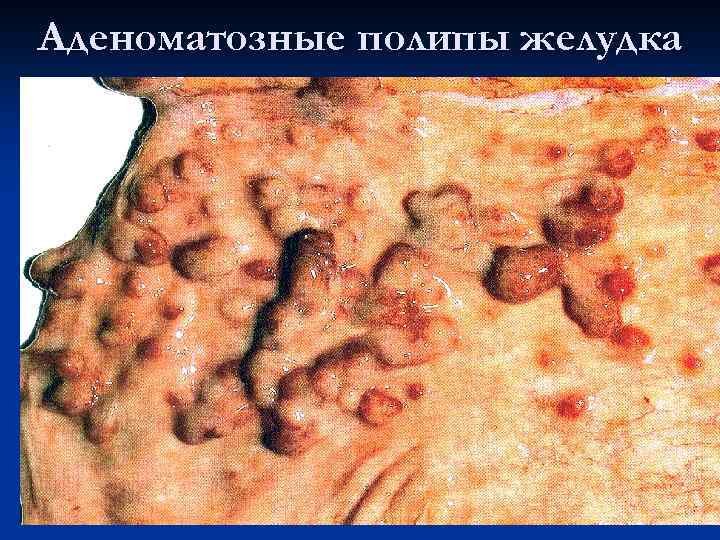
Аденоматозные полипы желудка
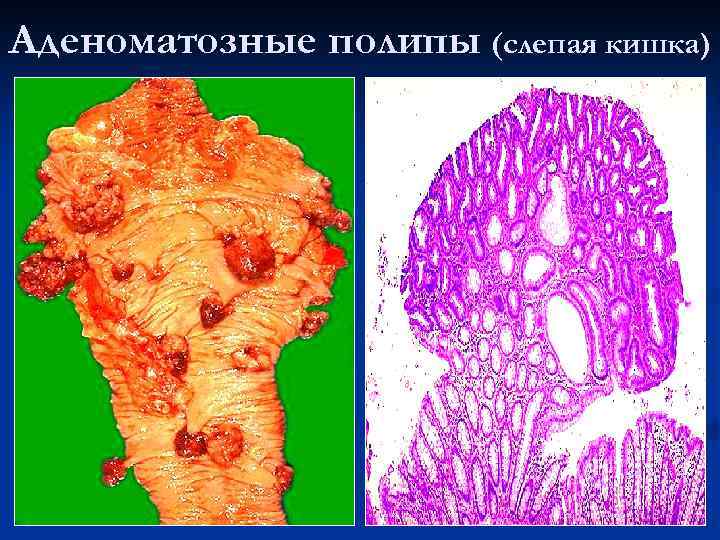
Аденоматозные полипы (слепая кишка)

Остроконечные кондиломы
РЕАКЦИЯ ВОСПАЛЕНИЯ — универсальная защитная реакция организма на действие различных патогенных факторов (механических, физических, химических, биологических и др.), благодаря которой происходит обезвреживание и уничтожение вызвавших повреждение факторов. Проникшие патогены индуцируют комплексную реакцию воспаления, которая обеспечивает привлечение лейкоцитов и растворимых компонентов плазмы в очаги инфекции, что приводит к локализации и уничтожению микрорганизмов в области их внедрения.
КЛИНИЧЕСКИЕ ПРИЗНАКИ ВОСПАЛЕНИЯ
· rubor (краснота),
· tumor (опухоль, припухлость),
· calor (жар),
· dolor (боль),
· functio laesa (нарушение функции).
СТАДИИ ВОСПАЛЕНИЯ
В классической патологии было принято выделять три стадии воспаления:
— альтерацию,
— экссудацию,
— пролиферацию.
Такое деление сохраняется и в настоящее время. Однако новые исследования и новые факты показали, что указанные стадии не монолитны, между ними нет четких границ (например, альтерация может быть максимально выражена на стадии гнойной экссудации, а нарушения микроциркуляции могут быть неодинаковыми в одно и то же время в различных участках очага воспаления). Поэтому в зависимости от процесса, преобладающего на определенном этапе воспаления, выделяют следующие стадии (рис.):
Стадия альтерации (повреждения):
· Первичная альтерация
· Вторичная альтерация
Стадия экссудации и эмиграции
Стадия пролиферации и репарации:
· Пролиферация
· Завершение воспаления
Первичная альтерация. Воспаление всегда начинается с повреждения ткани. После воздействия этиологического фактора в клетках происходят структурные, а также метаболические изменения.
Они бывают разными в зависимости от силы повреждения, от вида клеток (степени зрелости) и т.д.
Одни клетки гибнут, другие продолжают жить, третьи даже активируются.
Последние будут играть особую роль в дальнейшем.
Вторичная альтерация. Если первичная альтерация является результатом непосредственного действия воспалительного агента, то вторичная не зависит от него и может продолжаться и тогда, когда этот агент уже не оказывает влияния (например, при лучевом воздействии).
Этиологический фактор явился инициатором, пусковым механизмом процесса, а далее воспаление будет протекать по законам, свойственным ткани, органу, организму в целом.
Действие флогогенного агента проявляется, прежде всего, на клеточных мембранах, в том числе на лизосомах.
Это имеет далеко идущие последствия. Заключенные в лизосомах ферменты реактивны. Но как только лизосомы повреждаются и ферменты выходят наружу, они активируются и усугубляют, то разрушительное действие, которое оказал этиологический фактор. Можно сказать, что первичная альтерация — это повреждение, нанесенное со стороны, а вторичная альтерация — это самоповреждение.
Здесь следует отметить, что вторичная альтерация представляет собой не только повреждение и разрушение.
Некоторые клетки действительно гибнут, другие же не только продолжают жить, но и начинают вырабатывать биологически активные вещества, вовлекая в динамику воспаления иные клетки как в зоне воспаления, так и вне ее.
Клетки воспаления. Макрофаги. Установлено, что активированные макрофаги синтезируют особое вещество, получившее название интерлейкин-1 (ИЛ-1).
Оно выделяется макрофагами в среду и распространяется по всему организму, где оно находит свои мишени, которыми являются миоциты, синовиоциты, гепатоциты, костные клетки, лимфоциты, нейроциты.
По-видимому, на мембранах этих клеток имеются специфические рецепторы, благодаря которым ИЛ-1 действует именно на них, а не на другие клетки. Действие это стимулирующее и более всего изучено применительно к гепатоцитам и лимфоцитам.
Действие ИЛ-1 универсально, т.е. срабатывает при любом инфекционном (воспалительном) заболевании, причем в самом начале, и таким образом дает сигнал указанным органам включиться в воспалительный (инфекционный) процесс.
Есть основание предполагать, что характерные для ранних этапов заболевания симптомы (головная боль, боль в мышцах и суставах, сонливость, лихорадка, лейкоцитоз и увеличение содержания белков, в том числе иммуноглобулинов) объясняется именно действием ИЛ-1 (рис.).
Роль макрофагов не ограничивается секрецией ИЛ-1. В этих клетках синтезируется еще целый ряд биологически активных веществ, каждое из которых делает свой вклад в воспаление. К ним относятся: эстеразы, протеазы и антипротеазы; лизосомальные гидролазы — коллагеназа, аластаза, лизоцим, α-макроглобулин; монокины — ИЛ-1, колониестимулирующий фактор, фактор, стимулирующий рост фибробластов; антиинфекционные агенты — интерферон, трансферрин, транскобаламин; компоненты комплемента: С1, С2, СЗ, С4, С5, С6; дериваты арахидоновой кислоты: простагландин Е2, тромбоксан А2, лейкотриены. Не следует забывать также важнейшую функцию макрофагов — фагоцитоз.
Тучные клетки. Роль этих клеток в воспалении заключается в том, что они при повреждении выбрасывают содержащиеся в их гранулах гистамин и гепарин. А так как эти клетки в большом количестве располагаются по краям сосудов, то и действие указанных веществ проявится, прежде всего, на сосудах (гиперемия).
Макрофаги и лаброциты находятся в тканях постоянно (клетки-резиденты). Другие клетки воспаления проникают в зону воспаления со стороны (клетки-эмигранты). К ним относятся полиморфно-ядерные нейтрофилы, эозинофилы и лимфоциты.
Нейтрофилы. Главная функция этих клеток — фагоцитоз. Они выселяются из костного мозга в кровь, эмигрируют из сосудов и в больших количествах скапливаются в воспаленной ткани.
И активное их размножение, и миграция, и фагоцитоз подвержены регулирующему влиянию биологически активных веществ (тканевых, системных, организменных). Действие их проявляется, однако, только тогда, когда на клетках имеются рецепторы, специфически реагирующие с медиатором воспаления: гистамином, адреналином, глюкокортикоидами, гамма-глобулинами и т.д.
В цитоплазме нейтрофилов имеется два типа гранул: первичные азурофильные (более крупные) — обычные лизосомы, вторичные, или специфические гранулы мельче, а главное, они содержат другой набор ферментных и неферментных веществ. В первичных гранулах содержатся кислые гидролазы, а кроме того, лизоцим, миелопероксидаза и катионные белки. Вторичные гранулы специфические; содержат щелочную фосфатазу, лактоферрин и лизоцим. Все это важно для понимания участия нейтрофилов в воспалении (см. ниже).
Эозинофилы. Роль эозинофилов в воспалении определяется рецепторами, расположенными на поверхности, и ферментами, находящимися внутри. На наружных мембранах имеются рецепторы для комплемента, иммунных комплексов, содержащих IgE, IgG. Из ферментов следует упомянуть гистаминазу и арилсульфатазу В. Важную роль играет большой катионный белок, который способен нейтрализовать гепарин, повреждать личинки ряда паразитов. Миграция и активация эозинофилов происходит под влиянием комплемента (С5а и С5—С7), пептидов тучных клеток, ПГД, веществ, продуцируемых гельминтами.
Тромбоциты. Роль тромбоцитов (кровяных пластинок) в воспалении состоит главным образом в том, что они имеют ближайшее отношение к микроциркуляции. Наверное, это самые постоянные и самые универсальные участники воспаления. В них содержатся вещества, влияющие на проницаемость сосудов, на их сократимость, на рост и размножение клеток, а главное — на свертываемость крови.
Лимфоциты. Эти клетки играют роль при любом воспалении, но особенно при иммунном.
Фибробласты. Действие фибробластов проявляется в последней стадии процесса, когда в очаге воспаления увеличивается число этих клеток, оживляется синтез в них коллагена и гликозамингликанов.
В суммарном виде данные о клетках воспаления представлены в табл. 2.
Медиаторы воспаления. Медиаторами воспаления называются биологически активные вещества, которые синтезируются в клетках или в жидкостях организма и оказывают непосредственное влияние на воспалительный процесс. Клеточные медиаторы были рассмотрены выше (см. табл. 2). Гуморальные медиаторы воспаления синтезируются в плазме и в тканевой жидкости в результате действия соответствующих ферментов. Первоначальной причиной появления (или увеличения количества) этих веществ является альтерация. Именно в результате повреждения клеток освобождаются и активируются лизосомальные ферменты, которые активируют другие ферменты, в том числе содержащиеся в плазме, в результате чего возникает целый ряд биохимических реакций. Поначалу они носят хаотический характер («пожар обмена»), а продукты расщепления не имеют физиологического значения, нередко токсичны. Постепенно, однако, в этом процессе появляется определенный биологический смысл. Протеолитические ферменты расщепляют белки не до конца, а только до определенного этапа (ограниченный протеолиз), в результате чего образуются специфические вещества, действующие целенаправленно и ызывающие специфический патофизиологический эффект. Оказалось, что одни из них действуют преимущественно на сосуды, повышая их проницаемость, другие — на эмиграцию лейкоцитов, третьи — на размножение клеток. Первым обнаружил определенный «порядок» и закономерность в процессе воспаления В. Менкин. В воспалительном экссудате он выявил и индивидуализировал химические вещества и сопоставил с ними определенные слагаемые воспаления: гиперемию, лейкоцитоз, хемотаксис.
Одним из клеточных медиаторов воспаления является гистамин. Он содержится в гранулах тканевых базофилов (тучные клетки или лаброциты) в комплексе с гепарином и химазой в неактивной форме. В. свободном состоянии он оказывает расширяющее действие на мелкие сосуды (капилляры, венулы), увеличивая проницаемость их стенки. В малых дозах гистамин расширяет артериолы, в больших — суживает венулы. Выброс гистамина осуществляется вместе с выбросом в окружающую среду всех или части гранул тканевых базофилов при их дегрануляции. Этому может способствовать воздействие тепла, ионизирующего или ультрафиолетового излучения, растворов солей, кислот, белков, синтетических полимеров и мономеров, поверхностно-активных веществ. Дегрануляция всегда наблюдается при иммунных реакциях, т.е. при взаимодействии антигена с антителом на поверхности тканевых базофилов.
