Медиаторы воспаления при бронхиальной астме
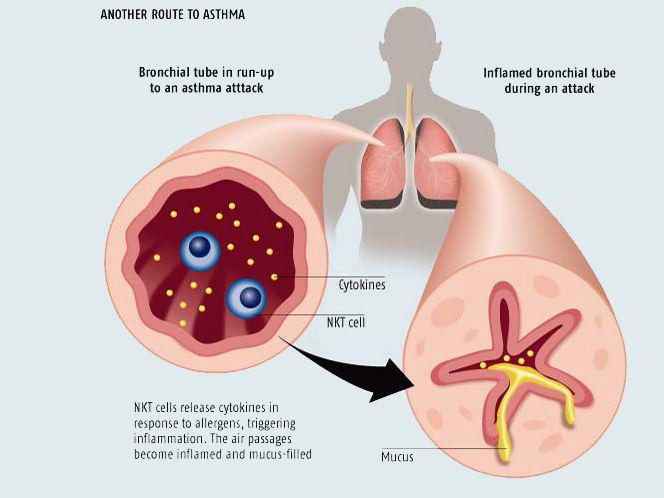
Медиаторы бронхиальной астмы. Тучные клетки и ответы типа I при астмеПодробное обсуждение неиммунологических факторов, вызывающих и поддерживающих астму, выходит за рамки наших статей. Однако необходимо остановиться вкратце на фармакологических и неврологических событиях, чтобы не потерять из виду все многочисленные факторы, связанные с индукцией астмы. Значение их особенно велико в настоящее время, когда вся область иммунофармакологии так быстро развивается. Многие исследователи подробно изучали медиаторы, высвобождающиеся из тучных клеток, и было опубликовано несколько интересных обзорных работ на эту тему за последнее время [Orange, 1971; Vane, 1971; Austen, Lichtenstein, 1973; Piper, 1974]. Медиаторы у человека изучались в периферических базофилах, в гомогенатах легочной ткани п в ее разделенных клеточных фракциях, и экспериментально на перфузируемых легких ин-тактных животных. Легочная ткань больных астмой выделяет как гистамин [Schild et al., 1951], так и медленно реагирующую субстанцию анафилаксии (МРС-А) [Brocklehurst, 1960, 1975] при воздействии соответствующих антигенов in vitro. Позднее был открыт фактор хемотаксиса эозинофилов (ФХЭ-А) [Кау, Austen, 1971]. При анафилактическом воздействии на легочную ткань in vitro было обнаружено также несколько типов простагландинов [Piper, Vane, 1969; Riper, Walker, 1973]. Простагландины E1 и Е2 обладают способностью воздействовать на гладкие мышцы, расширяя бронхи. Кроме того, после антигенного воздействия из сенсибилизированных легких человека был выделен фактор, активирующий тромбоциты [Siraganian, Osier, 1971]. При определении количества медиаторов в надосадоч-пой жидкости и в остаточной легочной ткани после антигенного воздействия на сенсибилизированные клетки легких человека или их фрагменты удалось установить, какие медиаторы образуются раньше и какие синтезируются после иммунологической стимуляции.
Гистамин образуется заранее и хранится в гранулах тучных клеток [Ishizaka et al., 1972]. При анафилаксии он высвобождается путем экзоцитоза — на этом биохимическом пути действуют диизопропилфиорофосфат (ДФФ), серинэстераза и ионы кальция [Austen, 1973]. ФХЭ-А также заранее образуется в легких [Wasserman et al., 1973]. Напротив, МРС-А и простагландины не образуются заранее и синтезируются вследствие анафилактической стимуляции. Интересно, что в отличие от образования простагландинов синтез МРС-А может быть заторможен гликатом натрия-хрома [Dawson, Tomlison, 1974]. Особенно важно то, что секреция этих веществ в гомогенатах легочной ткани, видимо, находится под влиянием стимуляции а- и бета-адренергических и холииергических рецепторов [Kaliner et al., 1972; Orange et al., 1971]. Такие адренергические агенты, как изопреналин, увеличивают внутриклеточное содержание циклического аденозин-3,5-монофосфата (циклический АМФ) и подавляют высвобождение гистамина и МРС-А. Такие а-адренергические агенты, как фенилэприн, снижают уровень циклического АМФ и оказывают обратное действие, повышая выделение гистамина и МРС-А [Lichtenstein, Margolis, 1968]. При холинергической стимуляции повышается уровень гуанозина-3,5-монофосфата (циклического ГНФ) и увеличивается высвобождение гистамина и других медиаторов [Orange, 1971]. — Также рекомендуем «Иммунофармакология реакций типа III при астме. Иммунонейрофармакология астмы» Оглавление темы «Виды и формы бронхиальной астмы»: |

Бронхиальная астма (БА) широко распространена в современном мире. Ею болеет каждый восьмой житель Европы. Для успешного лечения и профилактики заболевания необходимо знать его причины и особенности развития.
Именно поэтому изучению патогенеза бронхиальной астмы уделяется большое внимание. Подробнее об этом – далее в статье.
Что такое бронхиальная астма

Бронхиальная астма – это хроническая болезнь, которая характеризуется поражением дыхательных путей. Основное ее проявление – рецидивирующие приступы обструкции, то есть закупорки, бронхов. Во время приступа больному тяжело сделать выдох из-за того, что бронхи спазмируются на высоте вдоха.
У астматиков с продолжительным и тяжелым течением бронхиальной астмы развиваются необратимые изменения в дыхательной системе. Разрастается соединительная ткань в легких, развивается пневмосклероз, истончаются альвеолы (эта патология получила название «эмфизема»). Это еще больше усугубляет течение заболевания и усиливает дыхательную недостаточность.
В основе патофизиологии бронхиальной астмы лежит повышенная чувствительность бронхов к различным провоцирующим факторам, причем эти факторы индивидуальны для каждого.
Этиология и формы бронхиальной астмы

Важнейшую роль в этиологии бронхиальной астмы отводят аллергическому фактору. Провокаторы заболевания делятся на две большие группы: эндоаллергены (вырабатываются внутри организма) и экзоаллергены (поступают извне). Чаще причиной заболевания становится вторая группа провоцирующих факторов. К ним относятся:
- Инфекционные возбудители – вирусы, бактерии, грибки, простейшие.
- Раздражители растительного происхождения – пыльца растений, пух тополя.
- Аллергены животного происхождения – шерсть, перья, слюна, пух.
- Бытовые аллергены – пыль, бытовая химия.
- Пищевые продукты – чаще всего аллергическую реакцию вызывают орехи, мед, шоколад, помидоры.
- Медикаменты – ацетилсалициловая кислота, антибиотики.
У некоторых больных проявления астмы возникают при определенных погодных условиях. Особенно плохо переносят астматики дождь, высокую влажность, холод. В этом случае для БА характерно отсутствие приступов, если нет воздействия внешних раздражителей.
В ходе многочисленных исследований американские ученые установили, что стресс также может быть пусковым механизмом в развитии приступов. Он способен стать первопричиной болезни, а также усугубить уже имеющуюся бронхиальную астму.
В зависимости от природы и особенностей течения заболевания выделяют следующие формы БА:
- Атопическая – развивается вследствие воздействия аллергенов неинфекционной природы.
- Инфекционно-зависимая – приступ астмы возникает после перенесенных инфекций.
- Глюкокортикоидная – в ее основе лежит нарушение баланса кортикостероидных гормонов.
- Нервно-психическая – обструкция бронхов происходит вследствие длительного стресса.
- Аспириновая – прием лекарств, содержащих ацетилсалициловую кислоту, приводит к развитию приступа удушья.
- Астма физического напряжения – заболевание проявляется после физических нагрузок.
Общая схема патогенеза бронхиальной астмы
В основе патогенеза бронхиальной астмы лежит воспаление в стенке бронхов. Любое воспаление сопровождается повышенной проницаемостью стенок сосудов.
В результате этого плазма (жидкая часть крови) просачивается через них. Жидкость накапливается в слизистой бронха, развивается отек. Просвет органа сужается, затрудняется прохождение воздуха.
Но почему у одних людей при попадании аллергена развивается воспалительный процесс в дыхательной системе, а другие никак не реагируют на него? Ученые долго думали над этим вопросом и пришли к выводу, что все дело в наследственной предрасположенности.
У некоторых людей с рождения повышена активность особых клеток крови – Т-лимфоцитов-хелперов 2 типа. Из-за этого у них выделяется большое количество иммуноглобулина Е (IgE) – белка, провоцирующего аллергическую реакцию.
Активный синтез IgE приводит к дегрануляции (повреждению) тучных клеток, которые находятся на стенке бронхов. Они начинают высвобождать медиаторы воспаления. Именно из-за этих веществ повышается проницаемость стенок сосудов, и развивается воспалительный процесс.
Но воспаление – лишь один из механизмов развития бронхиальной астмы. Помимо него, в развитии приступа принимает участие спазм бронхов. Гладкая мускулатура этого трубчатого органа резко сокращается, что приводит к перекрытию его просвета.
Не менее важную роль в развитии приступа БА играет повышенная секреция слизи клетками эпителия бронхов, выстилающего внутреннюю поверхность его стенки. Таким образом, в патогенезе бронхиальной астмы и развитии удушья можно выделить три основных фактора:
- воспаление в стенке бронхов;
- повышенная реактивность бронхиального дерева, из-за чего спазмируются мышцы этого органа;
- увеличенная выработка слизи эпителиальными клетками.
В общем патогенез бронхиальной астмы можно разделить на три этапа:
- Иммунологический – возникает при первом контакте организма с аллергическим агентом. Характеризуется активацией клеток крови и выработкой IgE.
- Иммунохимический – развивается при последующих контактах с раздражителем. Уже выработанные иммуноглобулины запускают развитие реакции в бронхиальном дереве, которая сопровождается синтезом медиаторов воспаления.
- Патофизиологический – проявляется активными изменениями в стенке бронха, описанными ранее. У больного затрудняется дыхание, появляются свистящие хрипы.
У астматиков, как и у аллергиков, в крови повышается количество эозинофилов. Эти клетки относятся к группе лейкоцитов.
Они повреждают реснички на эпителии бронхов, ухудшая тем самым эвакуацию слизи, и провоцируют изменения в тканях. Их количество в общем анализе крови более 6% говорит в пользу диагноза бронхиальной астмы.
Особенности патогенеза разных форм астмы
Этиология и патогенез бронхиальной астмы тесно взаимосвязаны. Фактор, который привел к приступу, определяет механизм его развития. Далее мы подробно разберем механизмы развития разных форм БА.
Атопическая форма
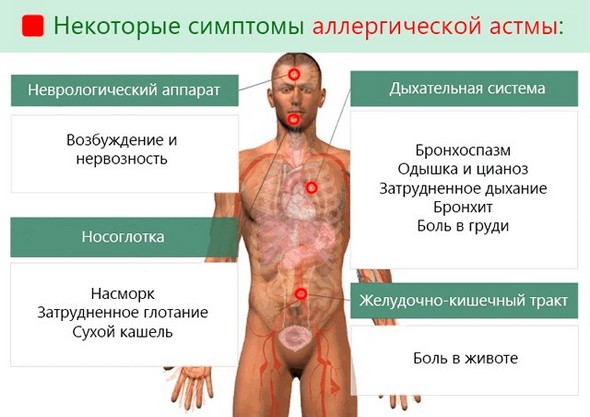
Это наиболее распространенная разновидность заболевания. Она развивается при повышенной чувствительности бронхов к аллергенам неинфекционной природы: бытовым, животным, растительным.
Особенность механизма развития бронхиальной астмы по атопическому типу заключается в его многоэтапности. Иммунологическая и иммунохимическая фазы проходят аналогично описанным в предыдущем разделе. А патофизиологический этап подразделяют еще на две стадии: раннюю и позднюю.
Ранняя реакция начинается в период от несколько минут до 2 часов после воздействия аллергенов. При этом слизистая стенки бронхов отекает, повышается выделение секрета, мускулатура спазмируется. Происходит закупорка просвета органа, прохождение воздуха затрудняется.
Поздняя стадия развивается примерно через 6 часов после действия раздражителя. Она характеризуется наличием стойкого воспаления в бронхах даже после спадания отека и прекращения спазма. Если не начать своевременное лечение, мышечная ткань органа заменяется соединительной. Данный процесс необратим.
Инфекционно-зависимая форма

Инфекционно-зависимая форма БА характерна для людей зрелого возраста. Она является осложнением перенесенных ранее острых респираторных вирусных инфекций, пневмонии, бронхита и других патологий органов дыхания.
Данная форма астмы характеризуется медленным развитием. Отек бронхов нарастает постепенно, состояние больного ухудшается на протяжении длительного времени. Пик заболевания наступает через две – три недели после перенесенной инфекции.
Течение инфекционно-зависимой формы более тяжелое. Отек, хоть и увеличивается медленно, не спадает на протяжении длительного времени. Эта форма БА тяжело поддается лечению при помощи традиционных медикаментов (бета-адреномиметиков, глюкокортикоидов).
Существует несколько механизмов развития бронхиальной астмы после воздействия инфекционных агентов:
- Аллергическая реакция медленного типа.
- Немедленная аллергическая реакция (аналогичная патогенезу атопической формы).
- Механизмы неиммунологического характера.
Реакция замедленного типа, соответственно названию, характеризуется длительным нарастанием отека. При этом для ее запуска требуется неоднократное воздействие аллергического агента. Клетки организма выделяют особые белки – медиаторы воспаления замедленного действия.
Эозинофилы также принимают участие в процессе. Они синтезируют белок, который повреждает реснитчатый эпителий бронхов. В результате его клетки не способны эвакуировать мокроту из просвета органа.
Неиммунологическая реакция развивается при непосредственном повреждении клеток бронхов инфекционными агентами.
Глюкокортикоидная форма
Глюкокортикоиды – это гормоны, вырабатываемые корой надпочечников. Они обладают мощным противовоспалительным действием, угнетают аллергическую реакцию. Поэтому нехватка этих гормонов в организме может как спровоцировать первый приступ, так и стать причиной постоянных рецидивов.
Патогенез влияния недостатка глюкокортикоидов при бронхиальной астме таков:
- Снижается концентрация бета-адренорецепторов на эпителии бронхов, что приводит к снижению восприимчивости к адреналину, расслабляющему мускулатуру бронхов.
- Активность медиаторов воспаления не уменьшается не регулируется гормонами.
- Увеличивается секреция провоспалительных белков и одновременно снижается активность противовоспалительных.
Эта форма бронхиальной астмы чаще всего развивается при длительном лечении глюкокортикоидами. Бесконтрольный прием гормонов влияет на надпочечники, угнетая их функцию.
У девушек гормональная БА может возникать при нарушении баланса половых гормонов. Приступ провоцируется снижением количества прогестерона в крови и повышением уровня эстрогена, что характерно для второй половины менструального цикла.
Нервно-психическая форма

Нервно-психическая форма бронхиальной астмы относится к группе психосоматических заболеваний. Это патологии, при которых длительные стрессы, депрессия, тревога проявляются в виде нарушения функции какого-либо органа и системы.
Для нервно-психической разновидности астмы характерно отсутствие органических изменений стенки бронхов на начальных этапах. Приступ развивается из-за спазма гладкой мускулатуры. Лишь при длительном течении заболевания возникают стойкие изменения в тканях органа.
В основе развития данной формы БА лежит гиперчувствительность эпителия бронхов к гистамину и ацетилхолину. Эти вещества являются нейромедиаторами, которые передают импульсы с периферии в центральную нервную систему.
Кроме того, приступ БА может провоцироваться любой нагрузкой, сопровождающейся глубоким вдохом.
Аспириновая форма
В основе патогенеза бронхиальной астмы аспиринового типа лежит повышенная чувствительность к препаратам, содержащим ацетилсалициловую кислоту. Вещество приводит к нарушению обмена арахидоновой кислоты.
Это, в свою очередь, стимулирует синтез лейкотриенов, которые вызывают спазм бронхиального дерева. Подобный эффект оказывает не только Аспирин, но и другие нестероидные противовоспалительные препараты.
Еще одно негативное свойство салицилатов – снижение активности тромбоцитов. Эти клетки играют важную роль в свертывании крови при травме сосуда и в питании стенок сосудов. Поэтому угнетение функции тромбоцитов повышает ее проницаемость, что провоцирует развитие отека.
Эту форму астмы чаще всего наблюдают у женщин в возрасте 30 – 40 лет. Часто больные аспириновой астмой принимают противовоспалительные препараты из-за болей в спине, суставах и прочее.
Астма физического напряжения

Приступ БА физического напряжения развивается при повышенной физической нагрузке, спустя 5 – 20 минут после ее начала. Некоторые больные отмечают удушье спустя 5 – 10 минут после окончания нагрузок.
В большинстве случаев приступ астмы физического усилия не очень интенсивный. Однако порой приходится прибегать к помощи ингалятора.
Большую часть времени человек дышит носом. Увлажненный, очищенный и теплый воздух благоприятно влияет на дыхательные пути и не раздражает их. При активных физических нагрузках дыхание сбивается, воздух поступает через рот. Он сушит и раздражает слизистую бронхов.
Эпителиальные клетки начинают активно выделять медиаторы воспаления, развивается отек слизистой. Спазм гладких мышц стенки бронхов также принимает участие в развитии приступа.
Патогенез астмы у детей

Патогенез бронхиальной астмы у детей преимущество основан на аллергической реакции. Инфекционно-зависимая форма встречается гораздо реже. Ею обычно страдают дети старшего школьного возраста.
У детей просвет бронхов уже, чем у взрослого, и мускулатура развита хуже. Потому основную роль в развитии приступа у них играет отек и гиперсекреция слизи. В то же время у взрослых на первом месте стоит бронхоспазм. Узким просветом дыхательных путей можно объяснить более тяжелое течение БА в детском возрасте.
Значительное место в этиопатогенезе бронхиальной астмы у детей играет генетическая предрасположенность. Наличие в анамнезе аллергического диатеза, поллинозов, БА у родителей повышают риск развития болезни у ребенка.
У многих детей в качестве аллергенов выступают пищевые продукты. Первый приступ удушья часто развивается в 5 – 6 месяцев, когда малышу начинают давать прикорм. Иногда искусственное питание становится провоцирующим фактором.
В заключение
При бронхиальной астме этиология и патогенез неразрывно связаны. Но вне зависимости от пускового фактора механизм развития приступа БА включат три процесса: отек слизистой, спазм гладких мышц, повышенная секреция слизи.
Заболевание часто предопределяется генетической предрасположенностью. Но нужно понимать, что человек не унаследует от родителей бронхиальную астму.
Ему передастся лишь повышенная чувствительность иммунной системы к определенным аллергенам. То есть наличие астмы у родителей еще не гарантирует ее развитие у ребенка.
Таким образом, патогенез БА сложен и многогранен. Надеемся, эта статья разъяснила особенности механизма развития этого заболевания.

В основе патогенеза бронхиальной астмы лежит повышенная чувствительность и гиперреактивность бронхов на специфические и неспецифические раздражители. Это обусловливает спазм бронхов, их отек, гиперсекрецию слизи и дискринию. При всех нормах бронхиальной астмы наблюдается нарушение нейрогуморальных механизмов регуляции тонуса бронхов. Следует заметить, что тонус бронхов регулируется множеством факторов. Функциональное состояние бронхов регулируется парасимпатической и симпатической нервной системой, через ?-, ?1 и ?2-адренорецепторы и холинергические структуры, расположенные в большом количестве в стенке бронхов. Также в регуляции сокращения гладких мышц бронхов участвуют кальций и АТФ-зависимый кальциевый насос, клические нуклеотиды –цАМФ и цГМФ, продукты метаболизма арахидоновой кислоты – простагландины и лейкотриены, нейропептиды (тахикинины), которые обладают бронхоконстрикторными и бронходилатационными свойствами, цитокины, продуцируемые тучными клетками и лимфоцитами.
При анализе патофизиологических нарушений у больных бронхиальной астмой обнаружен дефект в биохимической структуре ?2-адренорецепторов, сводящийся к недостаточности аденилциклазы, снижение функции которой приводит к бронхоспазму, выявлены гиперчувствительность ?-адренорецепторов, и нарушения в холинергических структурах бронхов (повышение уровня ацетилхолина и снижение холинестеразы). Полагают, что нарушение равновесия между возбуждающими (?-адренергическая и холинергическая система) и ингибирующими (?-адренергическая система) механизмами тонуса бронхов является фактором их длительного спазма. У больных бронхиальной астмой также выявлена повышенная чувствительность ирритантных рецепторов, расположенных в слизистой оболочке верхних дыхательных путей, ответственных за бронхоспазм. У больных бронхиальной астмой, кроме того, повышена продукция ПГF2, обладающего бронхоконстрикторным действием. Нарушения в системе регуляции тонуса бронхов могут быть вызваны самыми различными факторами.
При аллергической бронхиальной астме развитие бронхоспазма и других проявлений заболевания вызывается аллергическими реакциями, развивающимися в тканях бронхиального дерева. В основе патогенеза неинфекционно-аллергической бронхиальной астмы лежат реакции гиперчувствительности I типа. В результате аллергизации организма у больных формируются IgЕ-специфические антитела, которые фиксируются на тучных клетках и базофилах крови. При повторном попадании аллергена в организм происходит его взаимодействие с фиксированными IgЕ, что приводит к выбросу из тучных клеток медиаторов воспаления (гистамина, ацетилхолина, серотонина, протеаз, фактора хемотаксиса эозинофилов, нейтрофилов) и стимуляция метаболизма мембранных фосфолипидов. Первичные медиаторы воспаления и продукты метаболизма арахидоновой кислоты – простагландины (РGD2) и лейкотриены (LTC4) вызывают повышение проницаемости сосудистого русла, отек слизистой оболочки дыхательных путей, спазм гладкой мускулатуры бронхов, инфильтрацию ткани эозинофилами, нейтрофилами, усиливают секрецию бронхиальных желез. Перечисленные процессы развиваются в течение первых 5-20 минут после контакта организма с аллергеном и могут самостоятельно угаснуть через 1-2 часа.
У части больных через 4-6 часов наблюдается повторный бронхоспазм, который может продолжаться сутки и более. Он опосредуется вторичными медиаторами тучных клеток: фактором активации тромбоцитов, лейкотриенами (LTC4), а также хемотаксинами эозинофилов и нейтрофилов. Медиаторы поздней реакции индуцируют хемотаксис клеток в зону воспаления, вызывают активацию клеток воспаления в слизистой оболочке бронхов и стимулируют синтез лейкотриенов. Кроме перечисленных медиаторов, в развитии воспалительной реакции в бронхах участвуют активные формы кислорода, кинины, тромбоксаны, протеазы, цитокины (ИЛ-1, ИЛ-6, ФНО?).
В основе патогенеза инфекционно-аллергической бронхиальной астмы лежат аллергические реакции немедленного и замедленного типов. В результате сенсибилизации организма микробными антигенами появляются специфические антитела (IgЕ и IgG) и сенсибилизированные лимфоциты. У больных этой формы бронхиальной астмы из содержимого бронхов высеваются около 14 видов условно-патогенных и сапрофитных микроорганизмов. Чаще определяются Neisseria perflava, staphylococcus aureus, Klebsiella pneumoniae, которые, как установлено, имеют общие антигенные детерминанты с тканями легких человека. Бронхоспазм при бронхиальной астме индуцируется медиаторами, высвобождаемыми из тучных клеток (гистамин, серотонин, ацетилхолин, лейкотриены и др.) в результате взаимодействия на их поверхности антигена с фиксированными антителами и медиаторами, выделяемыми антигенактивированными сенсибилизированными лимфоцитами (цитокины, HRF-histamine releasing factor). HRF, продуцируемый лимфоцитами, стимулирует высвобождение из тучных клеток гистамина и других биологически активных веществ. Кроме того, бактериальные антигены способны самостоятельно индуцировать сокращение гладких мышц бронхов в результате прямого воздействия на них.
При приступах бронхиальной астмы сужение бронхов развивается в результате спазма гладких мышц, образования слизистых пробок, отека и воспаления слизистой оболочки. Обструкция усиливается во время выдоха, поскольку при этом происходит динамическое сужение дыхательных путей. Из-за сужения бронхов часть воздуха задерживается в альвеолах, что приводит к перерастяжению легких и удлинению выдоха. Избыточное сопротивление дыхательных путей приводит к напряжению в легких, в акт дыхания включаются дополнительные мышцы, появляется одышка. Образующаяся при бронхиальной астме густая, вязкая слизь содержит слущенный эпителий бронхов, эозинофилы, кристаллы Шарко-Лейдена. Слизь способна частично и полностью закупоривать бронхи. Чем длиннее и тяжелее приступ, тем более вязкой становится слизь из-за дегидратации. При бронхиальной астме активно протекает процесс морфологической перестройки стенки бронхов. Происходит уменьшение количества клеток мерцательного эпителия, увеличивается число клеток, секретирующих слизь, возникает эозинофильная, лимфоцитарная и макрофагальная инфильтрации ткани бронхов, отек и утолщение базальной мембраны, гипертрофия мышечной оболочки бронхов.
При бронхиальной астме в патологический процесс вовлекаются крупные, средние и мелкие бронхи. Шумное свистящее дыхание наблюдается при обструкции крупных бронхов, а приступы одышки и кашля развиваются при обструкции мелких бронхов.
Обструкция бронхов во время приступа бронхиальной астмы приводит к увеличению остаточного объема (ОО), уменьшению жизненной емкости легких (ЖЕЛ) и повышению общей емкости легких (ОЕЛ). Выраженность этих изменений зависит от тяжести приступа. Остаточный объем легких во время приступа может превышать значение общей емкости легких в межприступный период. Обструкция бронхов во время приступа неравномерна, поэтому одни участки легких могут вентилироваться лучше, а другие – хуже. Перфузия плохо вентилируемых участков резко снижается, нарушается равновесие между вентиляцией и перфузией, что приводит к снижению парциального давления O2 в артериях (раO2). В легких случаях это может быть единственным отклонением от нормы в газовом составе крови. Уровень парциального давления CO2 в артериях (раCO2) зависит от вентиляции альвеол. При легких и среднетяжелых приступах бронхиальной астмы возникает гипервентиляция, которая приводит к уменьшению раCO2 и дыхательному алкалозу. При тяжелых и длительных приступах, напротив, развивается гиповентиляция, повышается раCO2 и возникает дыхательный ацидоз. Перерастяжение легких и снижение парциального давления O2 в альвеолах (раO2) вызывают сужение капилляров альвеол и повышение давления в легочной артерии. Чем тяжелее приступ бронхиальной астмы, тем более выражена легочная гипертензия.

