Незавершенный фагоцитоз при воспалении
Фагоцитоз – это способность определенных клеток (фагоцитов) удерживать и переваривать плотные частицы. Это явление было открыто И. Мечниковым.
Фагоцитоз осуществляется микрофагами (нейтрофилами) и системой мононуклеарных макрофагов.
Мононуклеарные макрофаги
Система (MMS) включает следующие элементы:
- промоноциты (костный мозг);
- моноциты (кровь);
- тканевые макрофаги;
- гистиоциты соединительной ткани;
- печеночные клетки Куппера;
- легочные альвеолярные макрофаги;
- свободные и фиксированные макрофаги лимфатической ткани;
- плевру и перитонеальные макрофаги.
Клетки мононуклеарной системы объединяет общее происхождение гемопоэтических клеток и саморегуляция.
Моноцитопоэз
Моноцитопоэз – это стимулирующий фактор колонии фибробластов и фактор роста макрофагов, но он же подавляет (отрицательная саморегуляция) интерферон фибробластов и лейкоцитов и т. д.
Процесс фагоцитоза делится на четыре стадии:
- Приближение.
- Адгезия.
- Оседание;
- Стадия пищеварения.
Фаза приближения
Фагоцит приближается к объекту – бактериям, мервому клеточному элементу, инородному объекту. При движении под действием хемотаксиса цитоплазма фагоцита образует удлинения (псевдоподии).
Адгезия
Способствует образованию аминополисахаридов на поверхности фагоцитов и перекрытию фагоцитарного объекта белками сыворотки, особенно иммуноглобулинами. Последний механизм по сути является опсонизацией – бактерии и поврежденные клетки перекрываются с IgM, IgG и компонентами комплемента (C3, C5 и др.), что облегчает адгезию к фагоциту.
Адгезия
Поверхность фагоцита заряжена отрицательно, поэтому адгезия лучше, если объект, подлежащий фагоцитозу, заряжен положительно. Менее фагоцитарны отрицательно заряженные объекты, такие как опухолевые клетки.
Оседание
Этап фагоцитации объекта – путь инвагинации. Сначала фагоцит образует углубление, а затем фагосому – вакуоль, содержащую объект, подлежащий фагоцитозу. НАДН-зависимая оксидаза в мембране фагоцитов активируется до образования фагосом; в результате O2 превращается в O 2 ~ (супероксид-анион) и образуется H 2 O 2.
Эти продукты обладают бактерицидным действием, а также вызывают образование свободных радикалов. Под действием пероксидаз и каталаз H 2 O 2 расщепляется и высвобождается молекулярный O 2. Свободные радикалы и активный молекулярный O 2 действуют на мембрану фагоцита и объект, подлежащий фагоцитозу, активируя перекисное окисление липидов.
Липопероксиды и свободные радикалы неустойчивы к лизосомным мембранам и способствуют высвобождению лизосомальных ферментов.
Стадия пищеварения
Лизосомы присоединяются к фагосоме, содержащей фагоцитарный объект. Эти органеллы содержат все ферменты, необходимые для расщепления углеводов, белков, жиров и нуклеиновых кислот. В еще неактивной форме они попадают в вакуоль фагоцитов.
Пищеварительная вакуоль образуется при pH около 5,0, близком к оптимальному для лизосомальных ферментов. Активируются лизосомальные ферменты, и фагоцитарный объект постепенно переваривается. Во время стадии пищеварения проницаемость мембраны фагосомы увеличивается, содержимое фагосомы ускользает в цитоплазму, и микрофаг умирает (этому процессу способствует ацидоз). В этом случае фагоцитарный микроорганизм также может сохранять жизнеспособность.
Роль макрофагов в воспалительном процессе
Макрофаги начинают участвовать в фагоцитозе позже микрофагов. Макрофаги также более устойчивы к гипоксии и ацидозу, например, моноциты жизнеспособны даже при pH 5,5.
В очаге воспаления макрофаги выполняют несколько функций:
- Фагоцитируют бактериальные остатки, оставшиеся после эвакуации гноя и продуктов распада тканей – очищающая функция;
- Высвобождают лизосомальные ферменты – гиалуронидазу, аминопептидазу и др;
- Синтезируют компоненты системы комплемента и простагландины.
Взаимодействие макрофагов и лимфоцитов при хроническом воспалении
В то же время воспаленная тканевая среда также стимулирует образование фибробластов и фиброцитов. Постепенно появляется новая, богатая сосудами грануляционная ткань.
Фагоцитоз стимулируется продуктами повреждения тканей – внутриклеточные белки, ферменты, полипептиды, аминокислоты, электролиты и т. д., биологически активными веществами, половыми гормонами, тироксином, адреналином, лихорадкой. Но подавляется недостатком стимулирующих факторов, глюкокортикоидов, гликолортикоидов, ацетилхолина, ацетилхолина.
Фагоцитоз
Считается, что клетки плаценты и злокачественные опухоли способны секретировать вещество, которое подавляет функцию макрофагов, иммунологические реакции лимфоцитов и эмиграцию лейкоцитов, что приводит к значительному ослаблению или даже прекращению воспаления.
Объекты, которые фагоциты не могут переваривать, остаются в этих клетках в течение длительного времени и покрываются тонкой пленкой аминополисахаридов. После гибели фагоцитов они повторно фагоцитируются или выводятся из организма. Процесс, при котором фагоцит после переваривания высвобождает часть продуктов своего фагоцитоза в окружающую среду, называется экструзией.
Фагоцитоз – не единственный в организме механизм борьбы с воспалением. Большинство микроорганизмов погибают в условиях ацидоза, а также от ферментов, высвобождаемых во время гибели клеток и функционирования иммунокомпетентной системы.
Нейтрофилы во внеклеточном пространстве секретируют катионные белки, которые могут убивать ферменты без ферментов и фагоцитоза. Таким образом, воспалительные очаги постепенно избавляются от микроорганизмов и мертвых клеток.
Асептическое и острое воспаление
Дальнейшее течение воспаления зависит от того, является ли воспаление асептическим или бактериальным.
В асептических воспалительных условиях, например, вокруг хирургического шва, инородного тела, стенка микрофагов (нейтрофилов) начинает формироваться в течение нескольких часов, достигая максимума в течение дня.
Позже появляется следующий вал макрофагов, который достигает максимума через 2-3 раза. в день. Эмигрировавшие лейкоциты постепенно становятся неподвижными, больше не могут делиться и погибают в течение 3-5 дней. 2-3. на 5 сутки начинает формироваться стенка фибробластов, а на 5 сутки – соединительнотканная капсула.
Таким образом, в случае острого воспаления патогенный агент в организме преобразует белки, которые участвуют в реакции антиген-антитело, медиаторы и модуляторы воспаления, систему фагоцитов и миграцию клеток. В результате заканчивается острое воспаление. Однако, если инфекционные агенты попадают в участок асептического воспаления, например, в результате травмы, это воспаление становится септическим (бактериальным) воспалением.
Бактериальные воспалительные состояния бактерий и токсинов, не вызывающие гиперемии, экссудации и эмиграции лейкоцитов. Между клетками воспаленных тканей и особенно вокруг кровеносных сосудов накапливается все больше и больше микрофагов. Лизосомы микрофагов содержат множество активных ферментов, и эти клетки также начинают процесс фагоцитоза. При пальпации воспаленная ткань в это время кажется плотной, поэтому это называется стадией воспалительной инфильтрации.
По мере прогрессирования воспаления лейкоциты и те тканевые клетки, которые претерпели необратимые изменения во время воспаления, погибают. В этих клетках высвобождаются лизосомальные ферменты, которые расщепляют тканевые белки, белковые и липидные комплексы и другие структуры. Это стадия гнойного размягчения воспаления.
Эти стадии наблюдаются, например, у пациентов с гнойным воспалением перикарда (фурункул), гнойным воспалением апокринных потовых желез (гидраденит) и гнойным воспалением соединительной ткани (флегмона). При вдыхании воспаленная ткань выглядит мягкой, с характерным раскачиванием – флюктуацией. Образуется замкнутое скопление гноя – абсцесс.
Гнойное воспаление перикарда
Гной разрывается в направлении наименьшего сопротивления (либо наружу, либо внутри тела). Если гной попадает в кровоток (пемия), в организме может развиться множество очагов гноя, но под действием микроорганизмов и токсических веществ – угрожающее общее заболевание (сепсис, септикопиемия). Поэтому важно диагностировать накопление гноя и обеспечить хирургический дренаж гноя наружу.
Продолжение статьи
- Часть 1. Этиология и патогенез воспаления. Классификация.
- Часть 2. Особенности обмена веществ при воспалении.
- Часть 3. Физико – химические изменения. Роль нервной и эндокринной систем в развитии воспаления.
- Часть 4. Изменения в периферическом кровообращении при воспалении.
- Часть 5. Экссудация. Экссудат и транссудат.
- Часть 6. Эмиграция лейкоцитов. Хемотаксис.
- Часть 7. Фагоцитоз. Асептическое и острое воспаление.
- Часть 8. Распространение. Последствия. Принципы лечения воспаления.
Поделиться ссылкой:
Поглощённые фагоцитами бактерии обычно погибают и разрушаются, но некоторые микроорганизмы, снабжённые капсулами или плотными гидрофобными клеточными стенками, захваченные фагоцитом, могут быть устойчивы к действию лизосомальных ферментов или способны блокировать слияние фаго-сом и лизосом. В силу этого обстоятельства они на длительное время остаются в фагоцитах в жизнеспособном состоянии. Такая разновидность фагоцитоза получила название незавершённого. Существует множество причин незавершённого фагоцитоза, основные из них перечислены на рисунке.
Многие факультативные и облигатные внутриклеточные паразиты не только сохраняют жизнеспособность внутри клеток, но и способны размножаться. Персистирование патогенов опосредуют три основных механизма.
• Блокада фагосомо-лизосомального слияния. Этот феномен обнаружен у вирусов (например, у вируса гриппа), бактерий (например, у микобактерий) и простейших (например, у токсоплазм).
• Резистентность к лизосомальным ферментам (например, гонококки и стафилококки).
• Способность патогенных микроорганизмов быстро покидать фагосомы после поглощения и длительно пребывать в цитоплазме (например, риккетсии).
Фагоцитоз сопряжен с процессом передачи информации об Аг лимфоцитам. Это происходит тогда, когда объектом фагоцитоза являлся носитель чужеродной антигенной информации (клетки, микроорганизмы, опухолевые и вируссодержащие клетки, белковые неклеточные структуры и др.). В этом случае Аг после его модификации в фагоците (процессинг) экспрессируется на поверхности клетки. Такой Аг значительно более иммуногенен, чем интактный Аг. Фагоцитирующие клетки, осуществляющие процессинг, называют антигенпред-ставляющими клетками. При этом фагоцит представляет (презентирует) клеткам иммунной системы двоякую информацию: о чужеродном Аг и о собственных Аг, кодируемых генами HLA и необходимых для сравнения их с чужими Аг.
Фагоциты также продуцируют и выделяют в межклеточную жидкость ряд БАВ, регулирующих развитие либо иммунитета, либо аллергии, либо состояния толерантности. Таким образом, воспаление непосредственно связано с формированием иммунитета или иммунопатологических реакций в организме.
Основные причины незавершённого фагоцитоза.
Пролиферация
Пролиферация — компонент воспалительного процесса и завершающая его стадия — характеризуется увеличением числа стромальных и, как правило, паренхиматозных клеток, а также образованием межклеточного вещества в очаге воспаления. Эти процессы направлены на регенерацию альтерированных и/или замещение разрушенных тканевых элементов. Существенное значение на этой стадии воспаления имеют различные БАВ, в особенности стимулирующие пролиферацию клеток (митогены).
Пролиферативные процессы при остром воспалении начинаются вскоре после воздействия флогогенного фактора на ткань и более выражены по периферии зоны воспаления. Одним из условий оптимального течения пролиферации является затухание процессов альтерации и экссудации.
Формы и степень пролиферации органоспецифических клеток различны и определяются характером клеточных популяций.
• У части органов и тканей (например, печени, кожи, ЖКТ, дыхательных путей) клетки обладают высокой пролиферативной способностью, достаточной для ликвидации дефекта структур в очаге воспаления.
• У других органов и тканей эта способность весьма ограничена (например, у тканей сухожилий, хрящей, связок, почек и др.).
• У ряда органов и тканей паренхиматозные клетки практически не обладают пролиферативной активностью (например, миоциты сердечной мышцы, нейроны). В связи с этим при завершении воспалительного процесса в тканях миокарда и нервной системы на месте очага воспаления пролифе-рируют клетки стромы, в основном фибробласты, которые образуют и неклеточные структуры. В результате этого формируется соединительнотканный рубец. Вместе с тем известно, что паренхиматозные клетки указанных тканей обладают высокой способностью к гипертрофии и гиперплазии субклеточных структур.
Активация пролиферативных процессов коррелирует с образованием БАВ, обладающих антивоспалительным эффектом (своеобразных противовоспалительных медиаторов). К числу наиболее действенных среди них относятся:
• ингибиторы гидролаз, в частности протеаз (например, антитрипсина), р-микроглобулина, плазмина или факторов комплемента;
• антиоксиданты (например, церулоплазмин, гаптоглобин, пероксидазы, СОД);
• полиамины (например, путресцин, спермин, кадаверин);
• глюкокортикоиды;
• гепарин (подавляющий адгезию и агрегацию лейкоцитов, активность кининов, биогенных аминов, факторов комплемента).
Замещение погибших и повреждённых при воспалении тканевых элементов отмечается после деструкции и элиминации их (этот процесс получил название раневого очищения).
— Читать далее «Регуляция пролиферации. Острое воспаление.»
Дефицит
белка.Дефицит
витаминов.Наследственные
ферментопатии.Иммунодефициты.
Особенности
возбудителя (его размеры значительно
превышают размеры самого фагоцита).Объектом
фагоцитоза являются комплексы
антиген-антитело, находящиеся на
плоской поверхности сосудистого
эндотелия.
Как
следствие, раздраженные мононуклеары
выделяют монокины, лимфокины, которые
стимулируют хемотаксис, соседние клетки
соединительной ткани и др. Активированные
хемоаттрактантами фагоциты способны
высвобождать содержимое своих гранул
не только внутрь фагосомы, но и во
внеклеточное пространство. При этом
содержимое гранул и продуцируемые
фагоцитами активные метаболиты кислорода
воздействуют
и на объект атаки, и на ткани организма
хозяина.
Дистантно развивается лейкоцитоз.
При
затяжных воспалительных процессах
(сопровождающихся незавершенным
фагоцитозом)
целесообразно применять
Стимуляторы
иммунитета, в частности, фагоцитоза
путем
искусственного обострения воспаления,
вводя, например, искусственно получаемые
эндотоксины бактерий (продигиозан);через
активацию лимфоцитов иммуностимуляторами
(см. тему «Патология иммунитета»).
Создание
гипертермии (положительный эффект на
активность ферментов, диссоциацию
оксигемоглобина).
Витаминотерапию.
Специфическую
антибиотикотерапию.
Механизмы пролиферации.
Пролиферация
— репаративная стадия воспаления, это
размножение клеток. Нейтрофилы погибают,
макрофаги расчищают поле для регенерации.
Фибробласты
— главные эффекторы репарации. Механизм
— стимуляция пролиферации через
синтез ДНК и митотическую активность.
Начинается с 1
стадии воспаления, а ее пик приходит к
3 стадии.
Медиаторы пролиферации (трефоны)
Полиамины
— путресцин, спермидин (продукты
орнитиндекарбоксилазы).Факторы
роста фибробластов
— тромбоцитарный и гипофизарный.Эндотелиальный
хемотаксический фактор
(из макрофагов) — для врастания сосудов
в грануляционную ткань.Тканеспецифические
стимуляторы
— иммуноглобулины G
и M.Лимфокины
(из Т-лимфоцитов) участвуют в пролиферации
лимфоцитов и макрофагов.Монокины
(из макрофагов).Эндотелиальный
фактор роста.Кейлоны
(ингибиторы пролиферации).
Их
эффекты ослабляет: адреналин,
глюкокортикоиды, цАМФ. Усиливает
альдостерон, цГМФ.
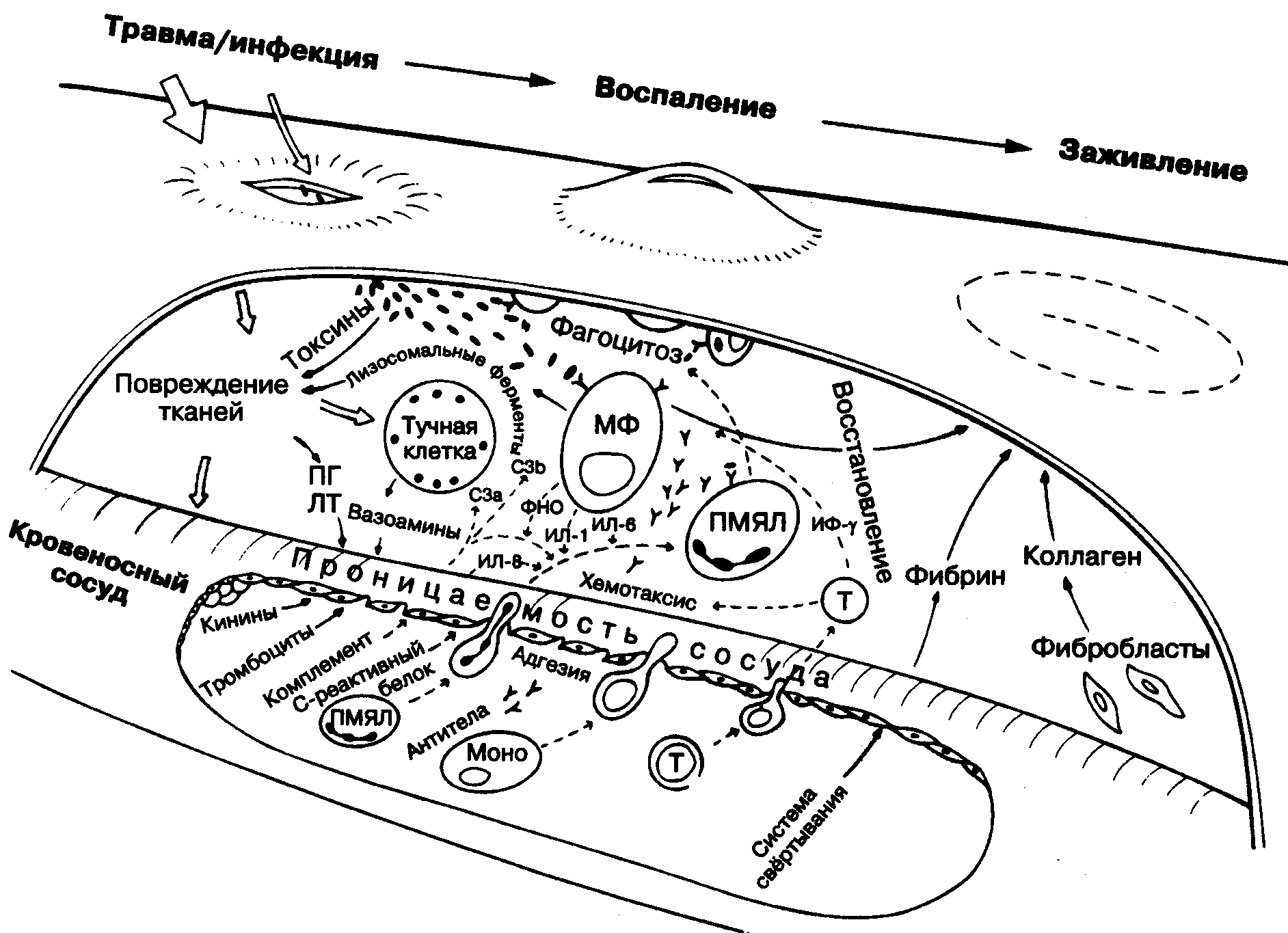
Рис. 10.5. Общая схема
острого воспаления.
Хроническое воспаление. Гранулема.
Хроническое
воспаление
развивается, когда повреждающий агент
действует длительное время, или первично
(при аллергических и аутоиммунных
болезнях), и характеризуется преобладанием
процессов пролиферации.
Причины хронического
воспаления
Слабая реактивность,
чаще у детей и стариков.Слабые сосудистые
реакции.Незавершённый
фагоцитоз.Устойчивые
микроорганизмы (при туберкулёзе,
проказе, листериозе, токсикоплазмозе).Неперевариваемые
объекты — инородные тела (металл,
древесина).
Активация
лимфоцитов как хронический аутоиммунный
процесс бывает при ревматоидном артрите,
системной красной волчанке (СКВ). Этому
способствует изменение антигенной
структуры клеток в очаге воспаления.

Рис. 10.6. Схема
хронического и клеточно-опосредованного
(гранулематозного) воспаления.
Гранулематозное
воспаление
— хроническое
воспаление, вызванное нерастворимыми
или медленно разрушающимися
(персистирующими) раздражителями и
сопровождающееся образованием гранулем,
возникающих в результате пролиферации
и трансформации способных к фагоцитозу
клеток.
Этиологические
факторы гранулематозного воспаления
Эндогенные
труднорастворимые
продукты повреждения тканей, в первую
очередь жировой ткани (например, мыла),продукты нарушенного
обмена, такие, как ураты.
Экзогенные
биологические
факторы (бактерии, грибы, простейшие,
гельминты и т. д.),органические
и неорганические вещества (при пылевых
болезнях — силикоз, талькоз, асбестоз,
биссиноз и др., крахмальные и тальковые
гранулемы, шовные гранулемы, вызванные
экзогенными жирами, сульфатом бария,
ртутью и т. д.), в том числе лекарственные
средства (гранулематозный гепатит,
олеогранулематозная болезнь).

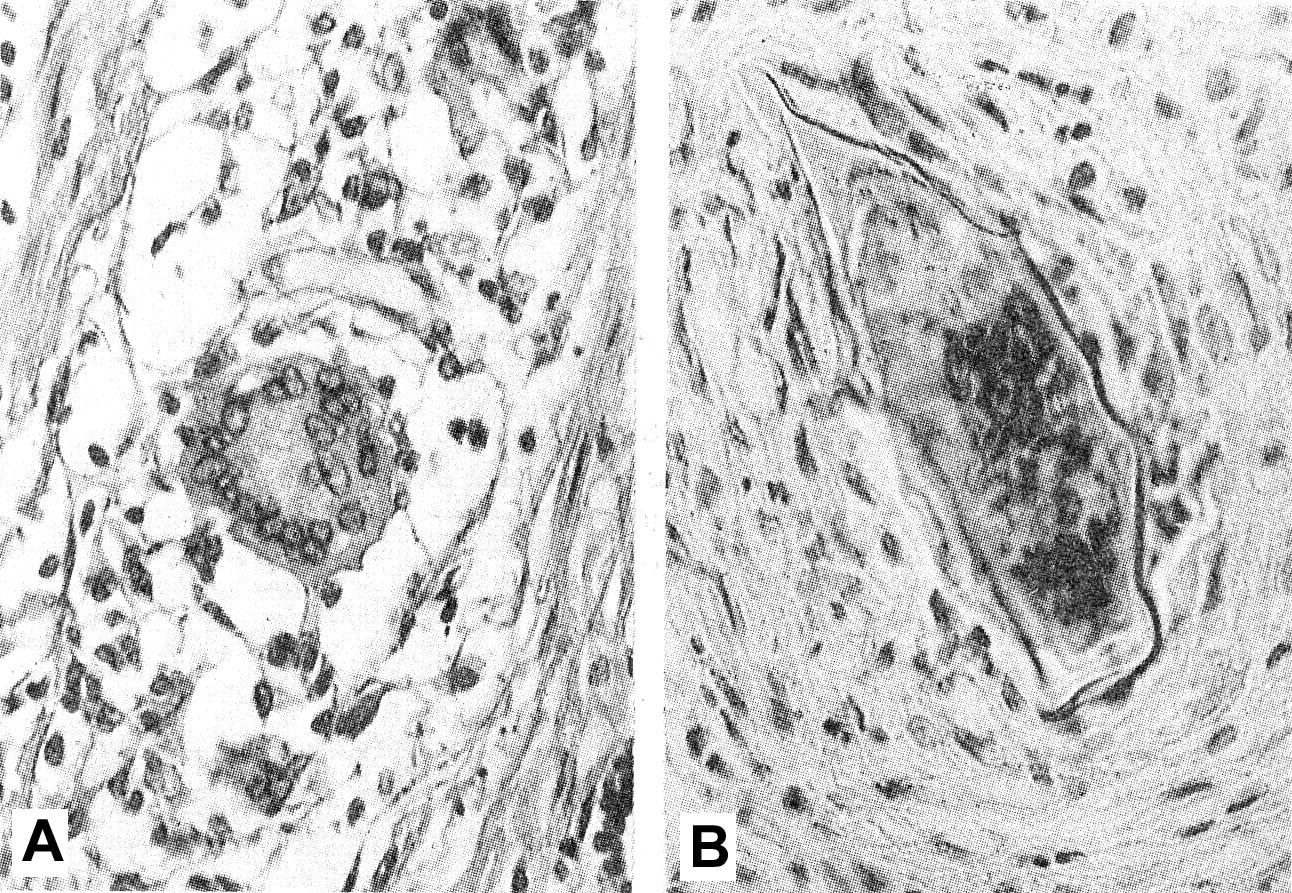
Рис.
10.7. Эпителиоидно-клеточные
гранулемы саркоидного типа.
Примечание.
А — гранулема саркоидного типа в стенке
тонкой кишки при болезни Крона, в центре
гранулемы — гигантская многоядерная
клетка Пирогова-Лангханса (увеличение
в 400 раз); В — гранулема саркоидного типа
вокруг яиц паразита при шистосомозе в
подслизистом слое тонкой кишки (увеличение
в 250 раз).
Длительно
раздражённые макрофаги выделяют
монокины, которые и формируют гранулёму.
Гранулемы
представляют собой компактное скопление
Макрофагов.
Эпителиоидных
клеток.Дополнительные
признаки (могут не быть)
инфильтрация
другими клетками (лимфоцитами,
плазматическими клетками, нейтрофильными
или эозинофильными гранулоцитами);наличием
фибробластов и развитием склероза;развитием
деструктивных изменений и некроза.
Соседние файлы в предмете [НЕСОРТИРОВАННОЕ]
- #
- #
- #
- #
- #
- #
- #
- #
- #
- #
- #
