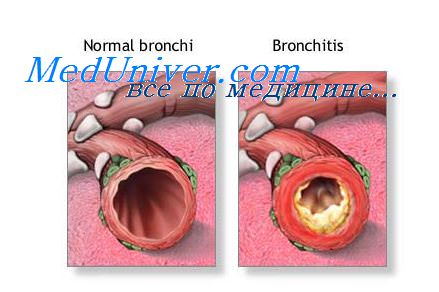
Последовательность клеточных реакций при остром воспалении
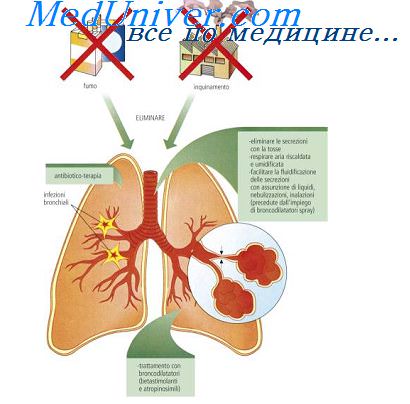
Клеточные механизмы защитных реакций организма при воспалении.Основные закономерности развития необратимых патологических изменений в клетках при первичной и вторичной альтерации Рассматривая воспаление как типовой патологический процесс, протекающий в виде последовательно сменяющих друг друга, а в ряде случаев развивающихся параллельно стадий альтерации, экссудации и пролиферации, необходимо отметить, что при определенных условиях течение воспалительных реакций может иметь как преимущественно защитно-приспособительный, так и разрушительный характер. Воздействие на ткани различных по своей природе факторов (химических, физических, бактериальных), как правило, приводит к развитию первичной альтерации. Степень выраженности и распространенность альтеративных изменений определяется интенсивностью действующего фактора, устойчивостью клеток к этому воздействию и способностью клеточных механизмов компенсировать патологические изменения. Повреждение ткани сопровождается выделением биологически активных веществ, способных еще в большей степени увеличивать альтеративные процессы — вызывать вторичную альтерацию. Независимо от особенностей воздействующего фактора, индуцирующего воспалительный процесс, все изменения в клетках можно свести к следующим типам:
Деструктивные процессы в тканях, возникающие в альтернативной стадии (фазе) воспаления, имеют преимущественно патологический характер. Их выраженностью в значительной степени определяется возможная степень неблагоприятного течения воспалительного процесса в целом. При обратимых сублетальных изменениях клетка способна адаптироваться и восстанавливать свою структуру и функцию. В этом случае, как правило, происходит снижение интенсивности метаболических процессов, ограничение потребления кислорода, угнетение процессов окислительного фосфорилирования, активирование гликолиза, уменьшение запасов макроэргических фосфорных соединений, падение уровня активности K-Na-АТФ-азы, ингибирование внутриклеточных ферментов, активирующих анаболические процессы. В процессе необратимого повреждения клетки наблюдается постепенное увеличение объема внутриклеточных структур (расширение эндоплазматической сети, набухание митохондрий, увеличение объема лизосом). Летальные изменения в клетках сопровождаются повреждением наружной и внутриклеточных мембран, в результате чего повышается их пассивная проницаемость для ионов. Одним из кардинальных признаков повреждения клетки является увеличение содержания натрия в цитозоле и выход во внеклеточную среду калия. Тяжелые метаболические расстройства клеточных функций сопровождаются увеличением содержания кальция в цитозоле. В нормальных условиях в цитоплазме регистрируется низкая концентрация кальция, не превышающая 10″‘ моль/л, которая обеспечивается непрерывной работой Са-АТФаз. Основные запасы кальция содержатся в эндоплазматическом ретикулуме, большая часть мембраны которого плотно покрыта белком с молекулярной массой 110 кДа, являющегося Са-насосом. Концентрация кальция в эндоплазматическом ретикулуме в 10 000-100 000 раз выше чем в цитозоле. Деполяризация клеточной мембраны и гидролиз мембранных липидов сопровождаются раскрытием кальциевых каналов, по которым кальций из внутриклеточных депо (цистерн эндоплазматического ретикулума, митохондрий) или интерстициального пространства устремляется в цитозоль. Возникающие в ходе воспаления метаболические нарушения энергообеспечения работы транспортных систем клеток изменяют нормальное протекание процессов реабсорбции кальция, который устремляется из кальцийсодержащих структур и внеклеточной среды в цитозоль по механизмам пассивного транспорта. — Также рекомендуем «Изменения клеток при альтеративной стадии воспаления.» Оглавление темы «Ключевые механизмы воспаления легких.»: |
Воспаление (лат. inflammatio) – это сложный процесс реакции организма на внешний или внутренний повреждающий (болезненный) фактор. Воспаление направлено на устранение этого фактора, восстановление поврежденных тканей и защиту от развития заболеваний.
Таким образом, воспаление выполняет защитную функцию в организме, но только тогда, когда оно острое. Хроническое воспаление перестает быть физиологическим фактором и становится патогеном, ведущим к аутоиммунным заболеваниям и раку.
Воспаление – это естественный процесс, который происходит на определенных этапах. Без воспалительной реакции, которая активирует иммунную систему для борьбы с патогеном, например, вирусом, бактериями, травмированными участками, мы не смогли бы пережить даже самую маленькую инфекцию.
Сложность воспалительного процесса отражается в часто используемых терминах – состояние, процесс или воспалительная реакция.
Симптомы воспаления
Симптомы острого воспаления были впервые описаны римским ученым и энциклопедистом Аврелием Цельсом (25 г. до н.э. – 50 г. н.э.). в единственной работе «Медицина», которая сохранилась до наших дней, он описал четыре основных симптома острого воспаления, которые иногда называют тетрадой Цельса:
- боль (лат. dolor);
- повышенная температура (лат. calor);
- покраснение (лат. rubor);
- отек (лат. tumor).
Пятый признак воспаления – потеря функции и повреждение органов (лат. Functiolaesa) был добавлен немного позже, возможно, греческим врачом и философом Галеном (129-200 н.э).
Покраснение кожи является результатом увеличения кровотока в области, пораженной патогенными микроорганизмами, отек – это результат проникновения белка и клеток из сосудов в ткани – все это вызывает боль. Температура также является следствием увеличения кровотока. В свою очередь, «потеря функции» означает, что орган не функционирует должным образом.
В развитии воспалительной реакции участвуют многие физиологические механизмы, связанные как с клетками – гранулоцитами, моноцитами, тромбоцитами, лимфоцитами Т и В, тучными клетками, эндотелиальными клетками кровеносных сосудов, макрофагами, фибробластами, так и с веществами, выделяемыми ими – медиаторами воспаления. Со временем могут быть поражены целые органы и могут возникнуть системные симптомы – повышение температуры тела, потеря веса, мышечная атрофия, чувство общей слабости.
Воспаление при ларингите
Как возникает воспаление?
Чаще всего повреждающий фактор, который инициирует воспалительный процесс, приходит извне. Это может быть:
- физическое повреждение – химическое, тепло или холод, механическая травма;
- биологический агент – бактерии, вирус, чужеродный белок.
Также бывает, что причиной воспаления является процесс, происходящий внутри организма – эмболия артерии, сердечный приступ или развитие рака.
Изменения в кровеносных сосудах всегда являются корнем воспалительной реакции. Сосуды расширяются, и их проницаемость увеличивается. Это приводит к проникновению медиаторов и воспалительных клеток в окружающие ткани.
Составляющие воспаления
Острое воспаление выполняет важную защитную функцию – оно удаляет возбудителя и восстанавливает нормальную функцию органа. Переход острой фазы в хроническую фазу часто связан с потерей контроля организма над воспалительными механизмами и, следовательно, с функциональными нарушениями и даже повреждением пораженной ткани. Этот процесс можно сравнить с превращением острой боли (защитной функции) в хроническую боль, которая становится самой болезнью.
Патогенез воспалительного процесса
Воспалительная реакция неразрывно связана с иммунным ответом. Начинается с контакта патогена со специализированными клетками иммунной системы, так называемыми антигенпрезентирующие клетки. Когда клетки стимулируются, они продуцируют и высвобождают медиаторы воспаления, которые имеют решающее значение для инициации и поддержания воспалительного процесса.
Медиаторы оказывают про-и противовоспалительное действие на клетки-мишени, модулируя течение воспаления. Со временем адаптивная иммунная система (специфическая реакция) также участвует в борьбе с повреждающим фактором. Работа этой системы чрезвычайно точна – взаимодействие лимфоцитов Т и В приводит к выработке специфических антител, которые селективно нейтрализуют возбудителя.
Правильно функционирующая иммунная система эффективно распознает патогены и эффективно уничтожает их, не повреждая свои собственные клетки и ткани. Однако в определенных ситуациях иммунорегуляторные механизмы могут работать с дефектом – возникает воспалительная реакция на аутоантигены.
Это состояние встречается при многих аутоиммунных заболеваниях (диабет 1 типа, ревматоидный артрит, красная волчанка, целиакия, болезнь Хашимото).
Поделиться ссылкой:
Своеобразие вирусного воспаления на клеточном уровне.Особенности вирусного воспаления на клеточном уровне, также как и на субклеточном, обусловлены морфологическими и функциональными особенностями вирусных частиц. Аналогично воспалению, обусловленному другими инфекционными агентами, возможно развитие двух основных форм воспаления: острого и хронического. Принципиальная схема острого воспаления также сходна: повреждение клеток — выход гидролитических ферментов — нарушение проницаемости сосудистой стенки эндотелия и его базальной мембраны под влиянием продуктов деградации тучных клеток и активированных фагоцитов — диапедез форменных элементов крови и появление экссудата. И все-таки существуют принципиальные различия. Бактерии, за редким исключением (гонококки, менингококки), воздействуют на клетки-мишени извне с помощью различных ферментов и токсинов, которые нередко ведут к полному расплавлению наружнрой мембраны. Вирусы осуществляют процесс воспаления как снаружи, так и изнутри клетки. Основой защитной воспалительной реакции при бактериальной инфекции служат нейтрофилы, заглатывающие и переваривающие их, а также выделяющие ряд высокоактивных веществ. При этом возникает целый ряд кислородозависимых и кислородонезависимых защитных реакций, продукты которых (супероксид О2, Н202, ОН и др.) обладают мощным бактерицидным действием и в то же время способны повреждать собственные клетки хозяина. Кроме того, полиморфноядерные лейкоциты (ПМЛ) выделяют лизосомальные гидролазы, катепсины и эластазу, которая отслаивает эндотелиоциты от базальной мембраны. Биоокислители (02, Н202) разрушают ингибиторы протеаз и провоцируют образование медиаторов проницаемости, которые, наряду с системой комплемента, способствуют фокусированию нейтрофилов в очаге воспаления. Значительные скопления ПМЛ в сочетании с тромбоцитами способствуют не только повышению проницаемости стенок сосудов, но и их разрушению, что, чаще всего, имеет место при аллергических процессах в легких, бронхиальной астме, острых сливных пневмониях и респираторном дистресс-синдроме. Сравнительно недавно участие нейтрофилов в развитии воспалительного процесса при респираторных вирусных инфекциях практически отрицалось. Полагали, что это исключительная прерогатива бактерий. Тем не менее, в последние годы представлены убедительные данные о значительном вкладе нейтрофилов в процессы образования активных форм кислорода (АФК) при гриппе. Доказано, что одним из основных механизмов воспалительного процесса при гриппе является образование свободных радикалов кислорода. С генерированием этих форм связаны мутагенез, протеолитическая активация вируса гриппа, цитопатический эффект вирусной инфекции, деструкция капиллярной сети и стенок капилляров, развитие сливных пневмоний с отеком легких. Установлено также, что липидная пероксидация (ЛП), активируемая вирусом гриппа в клетках легкого, является одним из узловых метаболических процессов наряду с генерацией АФК. Именно эти процессы определяют тяжесть и распространенность воспалительной реакции. При резкой активации АФК и ЛП ферментная защита от них в виде супероксиддисмутазы (СОД), каталазы, глютатион-пероксидазы и аскорбиновой кислоты становится недостаточной. Преимущественная генерация при гриппе гипохлорида, который является мощным неспецифическим окислителем, способным окислять не только липиды, но и белки, безусловно, требует переоценки стратегии антиоксидантной терапии при гриппе, с подключением не только токоферола, ионола, но и более эффективной супероксиддисмутазы.
Несмотря на явное участие нейтрофилов в развитии воспаления при вирусных инфекциях, по мнению многочисленных авторов, основой фагоцитарной защитной реакции при вирусной инвазии являются моноциты и их зрелые формы — макрофаги. В чем сходство и отличие фагоцитоза, осуществляемого нейтрофилами и макрофагами? Сходство в наличии ряда аналогичных по функциональной направленности этапов при взаимодействии с чужеродными агентами: хемотаксис, активация, выброс активных веществ, адсорбция, захват, переваривание. Однако много принципиальных отличий. В противоположность нейтрофилам макрофаги — долгоживущие клетки и рассеяны по всему организму, они входят в состав соединительной ткани, содержатся в базальной мембране кровеносных сосудов. Соответствующую фокусировку макрофагов можно обнаружить как в ткани, так и в полостях и экссудатах. При хронической бронхолегочной патологии альвеолярные макрофаги нередко содержат вирусные антигены. Набор выделяемых активированным макрофагом веществ значительно больше и многообразнее, чем у ПМЛ. Соответственно этому спектр выбрасываемых активных веществ при вирусном воспалении значительно шире. К числу секретируемых им веществ следует отнести гидролазные ферменты (лизоцим, кислые гидролазы, нейтральные протеазы, липазы), ингибиторы протеолитических ферментов, факторы, меняющие клеточную пролиферацию и функцию (интерлейкин 1, фактор созревания тимоцитов, ангиогенный фактор, интерферон и фибронектин), производные липидов (простагландины, лейкотриены, фактор активации тромбоцитов), факторы, меняющие процесс свертывания крови (тромбопластин, активатор плазминогена), вирусоцидные агенты (супероксид — радикал О2, Н202, интерфероны), компоненты комплемента и их ингибиторы. Обилие секретируемых макрофагами веществ определяет и большую сложность и многообразие их функций. Активные МФ из очага воспаления участвуют во всех процессах по обеспечению гомеостаза, являясь главными его эффекторами. В отличие от нейтрофилов макрофаги способны фагоцитировать крупные, более 1 мкм объекты, именно они поглощают фрагменты клеток с содержащимися в них вирусами. В силу многообразия секретируемых веществ и выполняемых функций макрофаг активно вступает в контакт с другими клетками, осуществляющими более высокий уровень клеточной защиты организма. Именно макрофаг представляет Т-хелперам вирусный антиген, который находится на поверхности МФ в комплексе с клеточными маркерами главного комплекса гистосовместимости. Макрофаги запускают и регулируют деятельность всех видов лимфоцитов (В, Т с хелперной и супрессорной активностью). Под влиянием активированных МФ Т-лимфоциты продуцируют разнообразные растворимые факторы — лимфокины, которые, в свою очередь, оказывают активирующее воздействие на макрофаги. Макрофаги в значительно большей степени участвуют в развитии наиболее сложных и актуальных в настоящее время хронических форм воспаления. Причин для возникновения хронического воспаления при активации макрофагов значительно больше в силу их более длительного жизненного цикла, полифункциональности и значительной связи с элементами, контролирующими клеточный иммунитет, который при вирусных инфекциях, в отличие от бактериальных, имеет доминирующее значение. Функциональная недостаточность МФ, в том числе альвеолярных, нередко возникает именно под влиянием респираторных вирусов, встраивающихся в мембрану макрофага, повреждающих их рецепторный аппарат и внутренние структуры. Известно также, что для вирусов характерен незавершенный механизм фагоцитоза, при котором сами фагоциты способствуют диссеминации вирусного агента на значительные расстояния от первичного очага воспаления. — Также рекомендуем «Фагоцитоз при вирусной инфекции. Хроническое вирусное воспаление.» Оглавление темы «Воспаление в легких.»: |
Лекция 13
ВОСПАЛЕНИЕ
• Воспаление — один из самых распространенных общепатологических процессов и лежит в основе многих заболеваний (воспалительные заболевания). Неудивительно поэтому, что со времен Гиппократа взгляды на воспаление исторически отражали взгляды на сущность болезни вообще. Поэтому воспаление испытало груз всех течений в медицине — гуморализма, целлюляризма, нервизма, физиологизма, а в конце XX столетия — влияние достижений иммунологии, генетики и молекулярной биологии.
ИСТОРИЧЕСКАЯСПРАВКА
Клинические признаки воспаления были впервые описаны римским энциклопедистом Цельсом 2000 лет назад. Он относил к ним красноту (rabor), припухлость ткани — опухоль (tumor), жар (calor) и боль (dolor). В начале нашей эры греческий врач Гален дополнил эти четыре признака пятым — нарушением функции (functio laesa).
В довирховский период все многочисленные исследования воспаления проводились путем визуальных наблюдений, хотя и предпринимались попытки выделения различных его форм — катаральное, флегмонозное, гнойное, острое, хроническое воспаление (К.Рокитанский, 1846). Р.Вирхов в «целлюлярной патологии» (1858) смог раскрыть механизмы каждого из классических признаков воспаления: краснота и жар связаны с воспалительной гиперемией, припухлость — со скоплением в ткани экссудата, боль — с повреждением (альтерацией) ткани. Отстаивая свою нутритивную (питательную) теорию воспаления, Р.Вирхов противопоставляет паренхиматозный тип воспаления отделительному (экссудативному).
Важным этапом изучения воспаления в XIX веке явились исследования Ю.Конгеймом (1878) сосудистого компонента воспалительной реакции, позволившие выдвинуть сосудистую теорию воспаления. Подтверждением этой теории послужило открытие А.С.Шкляревским краевого стояния лейкоцитов и В.В.Подвысоцким (1899) межэндотелиальной миграции лейкоцитов в очаге воспаления.
К концу прошлого столетия сущность воспалительной реакции стала достаточно ясной: это защитно-приспособительная реакция, а назначение ее заключается как в уничтожении агента, вызвавшего повреждение, так и в восстановлении поврежденной ткани. Такое толкование воспаления определяет необходимость изучения его в филогенезе. Этот труд взял на себя Л.И.Мечников, показавший, что основой воспалительной реакции является фагоцитоз, осуществляющийся с помощью клеточных «цитаз», названных впоследствии лизосомами. Появляется фагоцитарная теория воспаления И.И.Мечникова (1892), наиболее аргументированная в «Сравнительной патологии воспаления» (1917). Теория Мечникова убеждает в совершенствовании механизмов воспаления по мере эволюции организмов, но она касается лишь фагоцитоза, направленного на уничтожение повреждающего агента; репаративная функция воспаления, ее эволюционное совершенствование оказались вне поля зрения исследователя. Репаративный компонент воспаления был раскрыт лишь в середине нашего столетия исследователями, показавшими роль медиации и клеточной рецепции в кинетике воспалительного процесса.
H.Dale и P.Laidow (1909) первыми открыли первый медиатор воспаления гистамин, a V.Menkin (1948) выделяет из экссудата вещество — лейкотаксин, влияющий на состояние сосудистой стенки и движение лейкоцитов в очаг воспаления. В дальнейшем среди медиаторов воспаления были выделены биогенные амины, плазменные системы, производные арахидоновой кислоты, кислородные радикалы и гидропероксидазы липидов, а также многочисленные медиаторы нейтрофилов, моноцитов, лимфоцитов и фибробластов [Серов В.В., Пауков B.C., 1995].
Эти исследования позволили дать наиболее полное, раскрывающее сущность процесса, определение воспаления.
СУЩНОСТЬИЭТИОЛОГИЯВОСПАЛЕНИЯ
• Воспаление — наиболее древняя и сложная сосудисто-мезенхимальная реакция на повреждение, направленная не только на ликвидацию повреждающего агента, но и на восстановление поврежденной ткани.
Уникальность воспаления в его многоликости. Биологическое его назначение — сохранение вида. Как категория медицинская, воспаление — это и проявление болезни, и патологический процесс, направленный на устранение повреждающего начала и репарацию, т.е. на исцеление от болезни.
Этиология воспаления многообразна. Оно может быть вызвано разнообразными эндогенными и экзогенными биологическими (вирусы, бактерии, грибы, животные-паразиты, антитела и иммунные комплексы), физическими (лучевая и электрическая энергия, высокие и низкие температуры, пыли и аэрозоли, различные травмы) и химическими (химические вещества, в том числе лекарства, токсины, яды) факторами.
Определение воспаления предусматривает тесную его связь как с иммунитетом (становление иммунитета осуществляется «посредством воспаления» — достаточно вспомнить постинфекционный иммунитет), так и с регенерацией (третья фаза воспаления — фаза репарации). Связь воспаления с иммунитетом и регенерацией хорошо объясняет ставшее аксиомой положение: иммунологический гомеостаз — это структурный гомеостаз.
ВОСПАЛЕНИЕИИММУНИТЕТ —
КИНЕТИКАВОСПАЛИТЕЛЬНОГОПРОЦЕССА
Сопряжение воспаления с иммунитетом для репарации обеспечивается участием всех систем защиты организма в уникальной реакции терминальных сосудов и соединительной ткани, которая составляет сущность воспаления.
Как известно, защиту организма определяют неспецифические факторы и иммунологическая реактивность, или иммунный ответ.
Неспецифическиефакторызащитыииммунологическая реактивность [поПетровуР.В., 1982]
| Неспецифические факторы защиты | Иммунологическая реактивность (иммунный ответ) |
| Фагоцитоз Система комплемента Интерферон Лизоцим Пропердин Гидролитические фрагменты Бактерицидные субстанции тканей Непроницаемость покровов | Антитела Гиперчувствительность немедленного типа(ГНТ) Гиперчувствительность замедленного типа(ГЗТ) Иммунологическая память Иммунологическая толерантность Идиотипы — антиидиотипы Фагоцитоз Система комплемента |
В становлении иммунитета при воспалении велика роль как фагоцитоза, так и системы комплемента. Место фагоцитоза, осуществляемого полиморфно-ядерными лейкоцитами (ПЯЛ) и моноцитарными фагоцитами (макрофаги), в системе иммунитета определяется тем, что, несмотря на неспецифичность самого акта фагоцитоза, фагоциты, особенно макрофаги, принимают участие в очищении антигенов, переработке их в иммуногенную форму, которую воспринимает Т-хелпер. Место макрофагов в
системе иммунитета определяется и участием в кооперации Т- и В-лимфоцитов, необходимой для становления иммунного ответа. Поэтому фагоцитоз дополняет формы реакций иммунологической реактивности. Система комплемента участвует в специфических реакциях, присоединяя свои компоненты к молекулам антител, что обеспечивает лизис антигенных субстанций, против которых выработаны антитела. Из этого следует, что комплемент как один из неспецифических факторов защиты принимает участие в иммунном ответе, поэтому он, как и фагоцитоз, дополняет формы иммунологической реактивности. Как видно, включение иммунного ответа при воспалении обеспечивается двумя клеточными системами неспецифической защиты: системой моноцитарных фагоцитов, а также плазменной системой — системой комплемента.
Кинетика воспалительной реакции для достижения конечной цели — элиминации повреждающего агента и репарации ткани — характеризуется сменой взаимоотношений клеточных систем защиты между собой и с системой соединительной ткани, что определяется медиаторной регуляцией. Из этого, однако, не следует, что в воспалительной реакции участвуют лишь ПЯЛ, макрофаги, лимфоциты и фибробласты. Клетки — носители вазоактивных аминов (лаброциты, базофилы, тромбоциты), как и сдерживающие их функциональную активность эозинофилы, имеют огромное значение для развития собственно сосудистой реакции воспаления. Но они непричастны к основному назначению воспалительной реакции — элиминации повреждающего начала и репарации повреждения. Как цепная, в значительной мере саморегулирующаяся, воспалительная реакция укладывается в универсальную схему: повреждение → медиация → рецепция → клеточная кооперация → клеточные трансформации → репарация (схема 16). Воспалительная реакция определяет и последовательно развивающиеся фазы: 1) повреждения, или альтерации, 2) экссудации, 3) пролиферации и дифференцировки клеток.
Схема 16. Клеточныесистемызащитыикинетика воспалительнойреакции
Повреждение (альтерация) — обязательный компонент воспаления. Это изначально то, на что возникает сосудисто-мезенхимальная реакция, составляющая сущность воспаления. Можно ли считать альтерацию фазой воспаления? Вопрос этот не решается однозначно. Одни современные патологи [Robbins S. et al., 1981] не выделяют альтерацию как таковую, подменяя ее нарушениями микроциркуляции и реологических свойств крови. А.М.Чернух в монографии «Воспаление» (1979) первой стадией воспаления называет сосудистую, выделяя в ней Две фазы. Д.С.Саркисов и В.Н.Галанкин (1988) рассматривают альтерацию как неспецифический компонент воспаления, причем не всегда обязательный (В.Н.Галанкин) для развития последующей экссудации и пролиферации. Иными словами, допускается возможность развития воспаления без повреждения, причем альтерация в такой ситуации подменяется функциональной недостаточностью полиморфно-ядерных лейкоцитов. Эта позиция, даже условно допускаемая, исключает понимание воспаления как сосудисто-мезенхимальной реакции на повреждение.
Многие патологи [Огруков А.И., 1972; Серов В.В., Пауков B.C., 1995; Cottier H., 1980] отстаивают необходимость выделения альтеративной фазы воспаления, характеризующей инициальные процессы (дистрофия, некроз) и выделение медиаторов. Вероятно, у патологоанатома есть все основания для сохранения этой фазы, имеющей конкретное морфологическое и биохимическое выражение.
■ Следует заметить, что сохранение альтеративной фазы воспалительной реакции не оправдывает выделения альтеративной формы воспаления, при которой сама сосудисто-мезенхимальная реакция на повреждение практически отсутствует. Поэтому необходимо согласиться с большинством современных патологов в том, что признание альтеративного воспаления, выделяемого классической патологией прошлого, противоречит сути воспалительной реакции в ее современном толковании.
Повреждение и медиация — неразрывные компоненты морфогенеза воспаления, поскольку медиаторы «рождаются» в самом повреждении (альтерации).
Принято выделять плазменные (циркулирующие) медиаторы, представленные прежде всего калликреин-кининовой системой, системой комплемента и системой свертывания крови, а также клеточные (локальные) медиаторы, связанные со многими клетками: лаброцитами, тромбоцитами, базофилами, ПЯЛ, макрофагами, лимфоцитами, фибробластами и др. Однако и плазменные, и клеточные медиаторы тесно взаимосвязаны и работают при воспалении как аутокаталитическая система, использующая принципы «обратной связи», «дублирования», «необходимого разнообразия» и «антагонизма».
Эти принципы системы позволяют циркулирующим медиаторам обеспечить повышение сосудистой проницаемости и активацию хемотаксиса ПЯЛ для фагоцитоза, а внутрисосудистую коагуляцию в отводящих из очага воспаления сосудах — для отграничения возбудителя и самого очага воспаления (барьерная функция очага воспаления). При этом основные этапы сосудистой реакции — повышение проницаемости, активация хемотаксиса ПЯЛ и фактора Хагемана — дублируются несколькими медиаторами. Те же принципы системы в аутокаталитической реакции клеточных медиаторов обеспечивают не только повышение сосудистой проницаемости, фагоцитоз и вторичную деструкцию, но и включение иммунного ответа для элиминации повреждающего агента и продуктов повреждения и, наконец, репарацию ткани путем пролиферации и дифференцировки клеток в очаге воспаления.
Наиболее ярко принцип дублирования выражен среди клеток — носителей вазоактивных веществ — лаброцитов, базофилов, тромбоцитов, а антагонистические начала — между этими клетками и эозинофильными лейкоцитами: медиаторы лаброцитов и базофилов стимулируют хемотаксис эозинофилов, последние же способны инактивировать эти медиаторы и фагоцитировать гранулы лаброцитов (схема 17). Среди клеток, несущих медиаторы сосудистой проницаемости, возникает «антагонистическое равновесие», определяющее своеобразие морфологии сосудистой фазы воспаления, особенно при аллергических реакциях.
Клеточные медиаторы — лейкокины, монокины (интерлейкин-1), лимфокины (интерлейкин-2) и фиброкины — являются локальными регуляторами кооперации клеток на «поле» воспаления — ПЯЛ, макрофага, лимфоцита и фибробласта [Серов ВВ., Шехтер А.Б., 1981]. Другими словами, клеточные медиаторы определяют последовательность и долю участия в воспалении фагоцитарной и иммунной систем, с одной стороны, и системы соединительной ткани — с другой.
«Дирижером» ансамбля клеточных медиаторов следует считать монокины макрофагов (схема 18). Макрофаги, поддерживаемые медиаторной ауторегуляцией, способны управлять с помощью монокинов дифференцировкой гранулоцитов и моноцитов из стволовой клетки, пролиферацией этих клеток, т.е. являются регуляторами фагоцитоза. Макрофаги не только влияют на функциональную активность Т- и В-лимфоцитов, принимают участие в их кооперации, но и секретируют 6 первых компонентов комплемента, т.е. являются посредниками привлечения иммунной системы в воспалительную реакцию. Макрофаги индуцируют рост фибробластов и синтез коллагена, т.е. являются стимуляторами завершающей фазы репаративной реакции при воспалении. Вместе с тем сами макрофаги испытывают регулярное влияние лимфокинов и фиброкинов, т.е. теснейшим образом связаны в локальной клеточной регуляции с лимфоцитом и фибробластом [Серов В.В., Шехтер А.Б., 1981; Маянский А.Н., Маянский Д.Н., 1983].
Клеточная рецепция играет огромную роль в локальной клеточной регуляции при воспалении. С нею связаны межклеточное взаимодействие и привлечение в очаг воспаления компонентов иммунных реакций, так как у всех эффекторных клеток воспаления обнаружены Fc-рецепторы иммуноглобулинов и С-рецепторы комплемента. Становятся понятными неразрывная связь и неравнозначное во времени сопряжение фагоцитарной системы, иммунной системы и системы соединительной ткани в реализации конечной цели воспалительной реакции (схема 19).
Схема 19. Межклеточноевзаимодействиепривоспалении
Варианты этого сопряжения, зависящие от особенностей как повреждающего агента, так и организма, реагирующего на повреждение, должны, вероятнее всего, определять развитие той или иной формы воспаления. Так, гнойное воспаление (вид экссудативного воспаления) отражает, вероятно, особую форму сопряжения функционально несостоятельной системы ПЯЛ с макрофагами. При этом макрофаги, усиленно фагоцитирующие распадающиеся ПЯЛ, становятся устойчивыми к возбудителю. В.Е.Пигаревский (1978), изучающий это особое взаимоотношение двух систем фагоцитоза, называет его резорбтивной клеточной резистенцией. Как видно, оно отражает вторичную несостоятельность фагоцитарной функции макрофагов при первичной несостоятельности фагоцитоза ПЯЛ.
Первичная и избирательная несостоятельность системы моноцитарных фагоцитов, разобщение ее с системой ПЯЛ лежат в основе гранулематозного воспаления (вид продуктивного воспаления). Фагоцитарная недостаточность макрофагов определяет образование из них эпителиоидных и гигантских клеток, теряющих фагоцитарные функции. Фагоцитоз подменяется отграничением, персистенцией возбудителя. Незавершенный фагоцитоз делает незавершенной и несовершенной саму воспалительную реакцию. Она становится выражением реакции гиперчувствительности замедленного типа (ГЗТ).
Очевидно также, что наследственные дефекты каждой из систем защиты, как и системы самой соединительной ткани, делают дефектной и воспалительную реакцию как по форме ее проявления и течению, так и по возможности реализации конечной цели. Достаточно вспомнить наследственную недостаточность бактерицидных систем ПЯЛ и моноцитов, наиболее ярко представленную при хронической гранулематозной болезни детей, наследственные и врожденные иммунные дефициты и фатальность развивающейся при них гнойной инфекции, врожденную несостоятельность соединительной ткани и упорство хронического воспаления. Нельзя не сказать и о наследственных дефицитах системы комплемента, особенно СЗ- и С5-компонентов ее. Э?