Последствия ацидоза в очаге воспаления
Оглавление темы «Изменения клеток при воспалении.»:
1. Изменение клеток при воспалении. Изменение морфологии и обмена веществ при воспалении.
2. Метаболизм углеводов при воспалении. Нарушение обмена углеводов при воспалении.
3. Метаболизм липидов при воспалении. Нарушение обмена липидов при воспалении.
4. Метаболизм белков при воспалении. Нарушение обмена белков при воспалении.
5. Метаболизм ионов и воды при воспалении. Нарушение обмена ионов и воды при воспалении.
6. Физико-химические изменения в очаге воспаления. Ацидоз.
7. Гиперосмия в очаге воспаления. Гиперонкия в очаге воспаления.
8. Изменение поверхностного натяжения мембран в очаге воспаления. Изменения коллоидного состояния цитозоля в очаге воспаления.
9. Медиаторы воспаления. Виды медиаторов воспаления.
10. Биогенные амины. Серотонин. Адреналин. Норадреналин.
Основные физико-химические изменения в очаге воспаления перечислены на рисунке.
Физико-химические изменения в очаге воспаления.
Ацидоз в очаге воспаления
Воспалительная реакция характеризуется увеличением [Н+] и, соответственно, снижением рН в клетках и межклеточной жидкости — развитием ацидоза.
Причина ацидоза
Причина метаболического ацидоза — накопление в очаге воспаления избытка недоокисленных соединений.
Механизмы развития метаболического ацидоза
• Образование большого количества «кислых» продуктов изменённого метаболизма вследствие:
— активации гликолиза, что сопровождается накоплением избытка молочной и пировиноградной кислот;
— усиления протеолиза и липолиза с накоплением аминокислот, ВЖК и КТ.
• Нарушение оттока из очага воспаления продуктов как нормального, так и нарушенного обмена веществ. Последнее особенно выражено в связи с замедлением оттока венозной крови и развитием стаза в очаге воспаления.
• Истощение щелочных буферных систем (бикарбонатной, фосфатной, белковой и др.) клеток и межклеточной жидкости, которые на начальном этапе воспаления нейтрализуют избыток кислых соединений.
Особенности изменения [Н+] в очаге воспаления
• Чем острее протекает воспаление, тем более выражен ацидоз: из компенсированного он быстро трансформируется в некомпенсированный.
• Как правило, [Н+] наибольшая в зоне первичной альтерации, она меньше в прилегающей к ней зоне вторичной альтерации и постепенно снижается по направлению к неповреждённой ткани.
• В отдельных участках интенсивной деструкции и аутолиза тканей, где накапливаются восстановленные органические и неорганические соединения, продукты промежуточного белкового распада (аммиак и его производные), может развиваться более или менее выраженный преходящий алкалоз. Однако в целом для очага воспаления характерен ацидоз.

Эффекты ацидоза в очаге воспаления
Последствия ацидоза
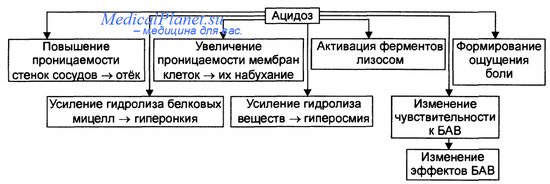
Последствия метаболического ацидоза в очаге воспаления приведены на рисунке.
• Повышение проницаемости клеточных мембран, в том числе плазмо-леммы и лизосом, приводит к выходу гидролаз в цитозоль и межклеточное вещество.
• Активация лизосомальных ферментов сопровождается усилением деструкции клеточных и неклеточных структур в очаге воспаления.
• Повышение проницаемости стенок сосудов за счёт усиления неферментного и ферментного гидролиза компонентов межклеточного матрикса, включая базальные мембраны.
• Формирование ощущения боли в очаге воспаления в связи с раздражением и повреждением чувствительных нервных окончаний в условиях избытка Н+.
• Усиление гидролиза солей и органических соединений ведёт к повышению осмотического и онкотического давления, изменяет коллоидное состояние цитозоля.
• Изменения чувствительности рецепторных структур клеток (в том числе стенок микрососудов) к регуляторным факторам (гормонам, нейромеди-аторам, другим БАВ) сопровождаются нарушениями регуляции тонуса сосудистой стенки. Так, на стадии альтерации в очаге воспаления, как правило, снижается чувствительность рецепторов к адреномиметикам (в частности, к норадреналину) и повышается к холиномиметическим агентам.
— Читать далее «Гиперосмия в очаге воспаления. Гиперонкия в очаге воспаления.»
Альтерационные процессы, нарушение обмена веществ и кровообращения в очагах воспаления вызывают ряд физико-химических изменений – ацидоз, гипертонию, дистонию, гиперосмию, гиперонкию и гипертермию.
Ацидоз
Ацидоз (H hiperjonija) очаг воспаления, возникающий в результате увеличения количества молочной и кетоновых кислот, плохо насыщенных кислородом промежуточных продуктов цикла Кребса (яблочная, янтарная и т. д.) и аминокислот. Первоначально буферная система ткани и воспалительный экссудат нейтрализуют кислотные соединения, образующиеся в тканевом метаболизме, и pH ткани не снижается – ацидоз компенсируется. Декомпенсированный ацидоз возникает при истощении буферной системы. PH экссудата снижается.
Ацидоз и алкалоз
Чем острее воспаление, тем сильнее выражен ацидоз. Особенно тяжелый ацидоз возникает при гнойном воспалении. В условиях хронического воспаления pH ткани обычно не опускается ниже 6,5 единиц, в то время как pH при остром гнойном абсцессе может упасть до 5,3. Наиболее выражен ацидоз в центре воспалительного очага, где он усиливает повреждение (альтерацию).
Альтерация
До выделения биологически активных веществ изменения связаны только с ацидозом. Слабый ацидоз на периферии очага воспаления стимулирует пролиферацию. Следовательно, разрастание ткани происходит в направлении от периферии очага воспаления к центру. Этот пример показывает, что один и тот же фактор может работать двумя способами.
Гипериония и дизиония
Наряду с разрастанием ионов водорода в воспалительных очагах увеличивается количество ионов натрия, кальция и хлора, а в результате повреждения клеток – количество ионов калия и анионов фосфорной кислоты. В нормальных тканях концентрация ионов К не превышает 20 мг%, но в гнойном экссудате может достигать 100-200 мг%. Отношение K:Na к K:Ca увеличивается. Дизион в основном проявляется увеличением количества ионов К в воспалительной жидкости и крови, оттекающей от места воспаления.
Гиперосмия (осмотическая гипертензия)
Концентрация ионов в очаге воспаления увеличивается, в том числе при усилении диссоциации солей. Кроме того, в результате активных ферментативных процессов большие молекулы распадаются на более мелкие и концентрация молекул увеличивается. В процессе интенсивного гликолиза, липолиза и главным образом протеолиза выделяется:
- много аминокислот;
- органических кислот цикла Кребса;
- жирных кислот;
- молочной кислоты.
Концентрация молекул увеличивается в основном за счет аминокислот – когда одна молекула белка (аминокислотного полимера) разрушается, высвобождается много молекул аминокислот. В результате осмотическое давление в очагах воспаления резко повышается – в нормальных тканях оно составляет 7-8 атмосфер, но очаги воспаления могут увеличиваться вдвое и более.
Кроме того, наибольшее осмотическое давление находится в центре воспалительного процесса. Гиперосмии тканей играют важную роль в развитии экссудации и боли.
Гиперонкия
Повышение коллоидосмотического давления вызывается увеличением количества мелкодисперсных белков в тканях. В то же время белки плазмы, в основном альбумины, попадают в ткани из сосудов с повышенной проницаемостью стенки.
Онкотическое давление низкое (всего около 1% от осмотического), но оно играет важную роль в обмене жидкости между кровеносными сосудами и тканями – обычно белки плазмы не проходят через стенку сосудов и удерживают жидкость в крови.
При ацидозе гидрофильность белков тканей увеличивается, и они набухают. Экссудация вызывает местный воспалительный отек. Развивается один из основных местных признаков воспаления – опухоль. Отек опухших тканей вызывает боль.
Отек и боль
Гипертермия
Вызывает один из характерных признаков воспаления – жар. Если воспаление развивается на поверхности тела, например на коже, повышение температуры происходит главным образом из-за артериальной гиперемии. Гораздо более теплая артериальная кровь поступает в относительно низкотемпературную область тела. Однако температура тканей также повышается, когда воспаление локализуется на большой глубине, например, во внутренних органах.
Причиной локальной гипертермии считается разделение процессов биологического окисления и окислительного фосфорилирования. В результате энергия не накапливается в АТФ, а выделяется в виде тепла.
Роль нервной и эндокринной систем в развитии воспаления
Регуляторная роль нервной системы проявляется на всех стадиях воспаления. Например, воспалительная гиперемия и экссудация могут быть вызваны у человека, при убеждении, что монета, помещенная на кожу, горячая, хотя на самом деле монета холодная.
Анестезия тормозит развитие воспаления, но местная анестезия способствует созреванию очагов гноя. Состояние вегетативной нервной системы считается важным в развитии воспаления, однако воспаление также возникает в полностью денервированных тканях. Нарушения микроциркуляции в очаге воспаления возникают в результате локальных нервных процессов (аксональный рефлекс) и гуморальных влияний.
На развитие воспаления значительное влияние оказывают гормоны коры надпочечников. Поэтому кортикоиды дезоксикортикостерон и альдостерон также называют воспалительными гормонами. В фазе воспалительной гипергидратации они увеличивают проницаемость сосудистой стенки и более позднюю пролиферацию. Во время фазы гипогидратации обычно увеличивается выработка адренокортикотропного гормона и глюкокортикоидов.
Глюкокортикоиды (кортизон, гидрокортизон) – это так называемые противовоспалительные гормоны. Кортизон снижает активность гистидиндекарбоксилазы и увеличивает активность гистамина, тем самым снижая уровень гистамина. Одновременно снижается активность 5-окситриптаминдекарбоксилазы и, как следствие, продукция серотонина. В результате снижается проницаемость сосудистой стенки, подавляется гиперемия и экссудация.
Глюкокортикоиды
Из-за ингибирующего действия глюкокортикоидов на ферментные системы снижается энергетический потенциал клеток, деление и подвижность клеток (эмиграция лейкоцитов и фагоцитоз). Глюкокортикоиды стабилизируют лизосомные мембраны и инактивируют кислую фосфатазу, рибонуклеазу и другие ферменты. Глюкокортикоиды подавляют не только воспаление, но и защитные реакции организма – экссудацию, эмиграцию лейкоцитов, фагоцитоз, пролиферацию и образование антител.
Другие гормоны также влияют на течение воспаления. Давно известно, что воспаление активно у пациентов с гипертиреозом и инертно у пациентов с микседемой.
Инсулин регулирует не только углеводный обмен, но и метаболизм белков. При отсутствии инсулина сопротивляемость организма инфекционным агентам снижается, и воспаление протекает гораздо тяжелее. Фурункулез часто встречается у диабетиков.
Эстрогенные половые гормоны подавляют активность гиалуронидазы и течение воспаления.
Продолжение статьи
- Часть 1. Этиология и патогенез воспаления. Классификация.
- Часть 2. Особенности обмена веществ при воспалении.
- Часть 3. Физико – химические изменения. Роль нервной и эндокринной систем в развитии воспаления.
- Часть 4. Изменения в периферическом кровообращении при воспалении.
- Часть 5. Экссудация. Экссудат и транссудат.
- Часть 6. Эмиграция лейкоцитов. Хемотаксис.
- Часть 7. Фагоцитоз. Асептическое и острое воспаление.
- Часть 8. Распространение. Последствия. Принципы лечения воспаления.
Поделиться ссылкой:
Воспаление всегда начинается с изменения. Через некоторое время процессы инфильтрации, протеолиза, некроза и синяков уменьшаются или прекращаются, и на первый план выходит регенерация тканей.
Наибольшее повреждение тканей вызывает гнойное воспаление. После эвакуации гноя в тканях остается полость (тканевой дефект), которая постепенно заполняется соединительнотканными элементами – происходит разрастание соединительной ткани.
Разрастанию соединительной ткани в месте воспаления способствует особый материал, присутствующий в повышенных количествах в воспаленных тканях и экссудате, активаторы роста, возникающие в результате процессов изменения, снижение хилона (ингибиторы пролиферации), пролиферация cAMF и слабый ацидоз.
В условиях слабого ацидоза для диссоциации оксигемоглобина на ткани требуется более высокое парциальное давление кислорода, чем обычно – кривая диссоциации Hb02 смещается вправо. Это уже начало следующей фазы – регенерации. Все интенсивно пролиферирующие ткани нуждаются в большом количестве воды, и регенерация соединительной ткани также начинается в гипергидратационных условиях (фаза гипергидратации).
Микрофаги в очаге воспаления постепенно погибают, и начинают преобладать макрофаги. Повышается фагоцитарная активность этих клеток, они фагоцитируют мертвые клетки и другие продукты изменения. В очаге воспаления один тип клеток заменяет другой (микрофаги – макрофаги – фибробласты), каждый из которых выполняет свою функцию, а затем отдает свое место другому типу клеток.
Таким образом, основные изменения соединительной ткани в очаге воспаления – это разрастание макрофагов, фибробластов и гистиоцитов, образование капилляров (2-3 дня) и развитие волокон соединительной ткани (3-6 дней). Дефект ткани постепенно заполняется грануляционной тканью – новой, энергично растущей и богатой сосудами тканью, которая окружает очаг воспаления.
В условиях повышенной активности фагоцитоза, ацидоза, протеолитических и липолитических ферментов уничтожаются микроорганизмы и элементы омертвевшей ткани, ограничивается воспаление, уменьшается экссудация и площадь гиперемии.
После заполнения дефекта ткани кровеносные сосуды и лимфатические сосуды начинают опорожняться (лимфатические сосуды выполняют дренажную функцию для устранения воспалительного отека). Воспалительный отек исчезает, наступает фаза гипогидратации. Происходит регенерация не только соединительной ткани, но и клеток органов и тканей. Однако по мере увеличения числа дифференцированных клеток, интенсивность регенерации снижается.
Если повреждение ткани невелико, регенерация часто бывает полной, тогда как при большом повреждении возникает рубцевание. Клетки высокодифференцированной паренхимы органов (головной мозг, миокард) неспособны к регенерации после травмы. Соединительная ткань часто перерастает в некротическую массу, например, после инфаркта миокарда, плеврита, операций на брюшной полости. Особенно интенсивно разрастается соединительная ткань вокруг инородного тела – вокруг него образуется плотная капсула.
Асептическая рана, края которой соприкасаются, заживает в первую очередь. В этом случае происходит выраженное разрастание макрофагов и интенсивное образование соединительнотканных волокон, которые вместе с эпителиальными клетками замещают фибрин тромба в ране.
Иногда поврежденные клеточные элементы, такие как слизистые оболочки, кожа, способны регенерировать и заполнить дефект определенными тканями, и тогда рана заживает без рубца. Напротив, инфицированные раны, а также асептические раны, если их края не совпадают, заживают вторично, и образуется рубец.
Последствия воспаления
Если регенерация ткани, поврежденной при воспалении, завершена, то функции также полностью восстанавливаются (restitutio ad integrum). Когда определенные ткани заменяются соединительной тканью, функции восстанавливаются только частично (restitutio incpleta). В результате такого воспаления образуется рубец, а функции тканей остаются ограниченными (замещение).
Рубец
Большой рубец часто негативно влияет на организм. По мере сокращения рубцовой ткани развивается значительная дисфункция органа или конечности. Спайки и рубцы, например, в брюшной полости после перитонита или хирургического вмешательства, стеноз пищевода и желудка после ожога кислотой или щелочью, деформируют органы и нарушают их функцию. Распространены нарушения движений конечностей из-за воспаления нервов, сухожилий и суставов. Также в паренхиматозных органах (легких, печени, поджелудочной железе, почках) часто возникают тяжелые функциональные нарушения после воспаления.
Процессы изменения, которые убивают высокодифференцированные клетки жизненно важных органов, могут угрожать существованию организма. Очень опасны рубцы, например, после воспаления сердечных клапанов или мозговых оболочек.
Биологическое значение воспаления в организме
Уже И. Мечников доказал, что воспаление, усложняющееся в ходе эволюции, является одним из неспецифических механизмов защиты всех организмов от действия патогенного агента. Даже сегодня воспаление считается типичным патологическим процессом, при котором компоненты повреждения и защиты связаны в неразрывное целое, а также во взаимной борьбе.
Вредные для организма процессы – это ухудшение функции и интоксикация, когда нарушаются функции воспаленного органа (ткани). Например, при воспалении сустава движения в нем болезненны и ограничены или даже невозможны.
Воспаление как защитная реакция организма проявляется по-разному. Уже во время смены высвобождаются биологически активные вещества, которые участвуют в сосудистых реакциях и процессах пролиферации. Спазм сосудов предотвращает дальнейшее распространение инфекционного агента в организме. В условиях венозной гиперемии уменьшается кровоток и лимфоток, поэтому токсические и пирогенные вещества дольше задерживаются в очаге воспаления.
Также важен для защиты воспалительный экссудат.
- Из-за кислой среды экссудат является бактерицидным. Его белки связывают бактериальные токсины.
- Экссудат разжижает и ферментативно расщепляет, препятствуя абсорбции и дальнейшему распространению токсинов в организме.
- Экссудат используется для доставки антител к специфическим антигенам в месте воспаления.
Особое значение имеет фагоцитарная и пролиферативная функция клеток соединительной ткани. Грануляционная ткань, образующаяся в процессе пролиферации, и соединительнотканный барьер изолируют воспаление от окружающих тканей. Благодаря этим защитным механизмам подопытному животному можно вводить токсины в очаге воспаления, но заметной реакции организма не происходит. С другой стороны, в здоровых тканях токсины вызывают у животного значительную реакцию или даже гибель.
Грануляционная ткань
Как и другие типичные патологические процессы в организме, защитная функция воспаления не безгранична. Если действие вредного агента сильное, защитные реакции могут стать ненормальными, вредными для организма. Например, тяжелый фурункулез, разлитой гнойный перитонит, септическое состояние и т. д. нельзя считать положительной защитной реакцией.
Способность реагировать на действие болезнетворных агентов воспалением – очень важный типичный патологический процесс в организме, нарушение которого может иметь опасные последствия. Эти нарушения могут быть связаны с уменьшением количества нейтрофилов (нейтропения) и проблемами с их функцией.
В свою очередь, наиболее частыми причинами тяжелой нейтропении являются лекарственный агранулоцитоз и лейкоз. В редких случаях возникает так называемая циклическая (периодическая) нейтропения, когда каждые 21 день наблюдается значительное снижение количества нейтрофилов. Эта нейтропения чаще встречается у пациентов с инфекционными кожными заболеваниями, отитом и артритом.
Дисфункция лейкоцитов может включать хемотаксис, эмиграцию и фагоцитоз. Например, нарушения хемотаксиса и эмиграции лейкоцитов возникают при диабете, пародонтите, терапии кортикостероидами и других.
Также описаны многие наследственные дефекты фагоцитарной системы. Некоторые дефекты – это нарушения бактерицидной активности фагоцитов, другие – нарушения подвижности фагоцитов.
- К первой группе относится хронический гранулематоз у детей, в основе которого лежит снижение активности НАДН2-зависимой оксидазы. В результате в клетке не образуется H 2 O 2 и не повреждается мембрана фагоцитирующего объекта. Процесс фагоцитоза не завершается, и из гистиоцитов развиваются гранулемы (чаще всего в легких). Гранулемы разрушаются, лейкоциты и микроорганизмы оставляют очаги воспаления, развивается сепсис.
- Вторая группа наследственных дефектов включает синдром Чедиака-Хигаси. Признаки включают лейкоцитарные аномалии и нарушения пигментации кожи, склонность к рецидивам, гнойные инфекции, анемию, лейкоцитопению, тромбоцитопению и т. д.
Воспаление развивается плохо из-за нарушения фагоцитоза. Снижается сопротивляемость организма инфекции, и ухудшается состояние больного. Например, в случае пониженной реактивности смертность больных пневмонией намного выше.
Принципы противовоспалительной терапии
Поскольку воспаление и часто связанная с ним лихорадка являются защитными, с ними не всегда нужно бороться. Иногда эти типичные патологические процессы изолируют возбудителя болезни, иногда – благотворно влияют на течение некоторых хронических заболеваний. Однако при многих острых воспалительных заболеваниях (фурункулез, тромбофлебит, острый аппендицит, острый панкреатит и т. д.) Необходимо бороться с воспалением, чтобы избежать опасных для организма осложнений.
Воспалительная терапия бывает этиологической и патогенетической.
- Цель этиологической терапии – устранить биологический агент воспаления (антибиотики, противотуберкулезные препараты, терапевтические сыворотки и т. д.) Или подавить действие аллергена.
- Задача патогенетического лечения – предотвратить или полностью заблокировать один из этапов воспалительного патогенеза.
Например:
- Противовоспалительные препараты (салицилаты, глюкокортикоиды) стабилизируют лизосомальную мембрану, снижают активность ферментов (трансаминаз, дегидрогеназ, эстераз, протеаз) и тем самым уменьшают образование биологически активных веществ.
- Индометацин подавляет синтез простагландинов. Гиперосмолярные растворы (как местные, так и внутривенные) используются для уменьшения воспалительного отека.
- Глюкокортикоиды подавляют фагоцитоз, пролиферацию клеток и иммунологические процессы. В результате течение воспаления ослабевает и замедляется. Эти препараты широко используются при лечении аллергических воспалений.
Противовоспалительная терапия
Чтобы создать наиболее благоприятные условия для развития воспаления как защитного процесса организма, воспаленным тканям нужен покой. В случае острого воспаления механические движения могут помешать локализации воспаления и способствовать распространению инфекции.
В лечении воспалений играют роль различные тепловые процедуры: они улучшают кровообращение и циркуляцию лимфы в воспаленных тканях и стимулируют экссудацию, тем самым усиливая и ускоряя воспалительные процессы. Холод снижает интенсивность этих процессов.
Основная задача хирургических методов лечения – удаление внутренних ограниченных инфекционных очагов воспаления (флегмонозный отросток, желчный пузырь), а также вскрытие и дренирование гнойной полости (абсцесс, флегмона).
В современной медицине, в том числе при лечении воспалений, успешно применяются каликреин и препараты ингибиторов каликреина.
Ингибиторы протеаз, обладающие широким спектром действия, участвуют в регуляции хининов и фибринолитической системы. Эти ингибиторы играют защитную роль при различных заболеваниях, включая панкреатит. Они препятствуют образованию калькреина и прогрессированию воспаления. Многие ингибиторы каликреина содержатся в бычьей печени, слюнных железах, поджелудочной железе. Препараты-ингибиторы (трасилол, калол, контральтик) используются при лечении острого панкреатита.
Препараты каликреина (падутин, депокаликреин, дилминал D, ангиотропин) расширяют кровеносные сосуды и играют важную роль в лечении облитерирующего эндартериита.
В период разрастания соединительной ткани для борьбы с негативными последствиями рубцевания, особенно контрактур, движения следует выполнять постепенно, увеличивая их амплитуду до максимума.
Продолжение статьи
- Часть 1. Этиология и патогенез воспаления. Классификация.
- Часть 2. Особенности обмена веществ при воспалении.
- Часть 3. Физико – химические изменения. Роль нервной и эндокринной систем в развитии воспаления.
- Часть 4. Изменения в периферическом кровообращении при воспалении.
- Часть 5. Экссудация. Экссудат и транссудат.
- Часть 6. Эмиграция лейкоцитов. Хемотаксис.
- Часть 7. Фагоцитоз. Асептическое и острое воспаление.
- Часть 8. Распространение. Последствия. Принципы лечения воспаления.
