Роль клеток крови при воспалении
Эффекты воспаления. Макрофаги и нейтрофилы при воспалении
а) Воспаление. При повреждении ткани независимо от его причины (бактерии, травма, химические агенты, тепло или любое другое явление) выделяется множество веществ, вызывающих существенные вторичные изменения в окружающих неповрежденных тканях. Весь комплекс этих тканевых изменений называют воспалением.
Воспаление характеризуется:
(1) расширением местных кровеносных сосудов с последующим избыточным местным кровотоком;
(2) увеличением проницаемости капилляров, что способствует утечке большого количества жидкости в интерстициальное пространство;
(3) часто — свертыванием жидкости в интерстициальном пространстве в связи с избытком фибриногена и других белков, вытекающих из капилляров;
(4) миграцией большого числа гранулоцитов и моноцитов в ткани;
(5) отеком тканевых клеток.
К тканевым продуктам, вызывающим эти реакции, относятся гистамин, брадикинин, серотонин, простагландины, несколько разных продуктов реакции системы комплемента, продукты реакции свертывающей системы крови и множество веществ, называемых лимфокинами, которые выделяются активированными Т-клетками (частью иммунной системы). Некоторые из этих веществ мощно активируют макрофагальную систему, и в течение нескольких часов макрофаги начинают уничтожать поврежденные ткани. Но иногда макрофаги повреждают еще живые тканевые клетки.
б) «Ограждающий» эффект воспаления. Одним из первых результатов воспаления является «ограждение» области повреждения от остальных тканей. Тканевые пространства и лимфатические сосуды в воспаленной области блокируются сгустками фибрина, поэтому через небольшой промежуток времени жидкость с трудом протекает через интерстиций. Этот процесс отгораживания задерживает распространение бактерий или токсических продуктов.
Интенсивность воспалительного процесса обычно пропорциональна степени повреждения ткани. Например, когда стафилококки проникают в ткани, они выделяют смертельно опасные клеточные токсины. В результате воспаление развивается быстро, гораздо быстрее, чем сами стафилококки могут размножиться и распространиться. Следовательно, для локальной стафилококковой инфекции характерно быстрое отгораживание, предохраняющее от распространения ее по телу.
Стрептококки, напротив, не вызывают такого интенсивного локального разрушения тканей. Следовательно, процесс отгораживания развивается медленно, на протяжении многих часов, в течение которых стрептококки успевают размножиться и мигрировать. В результате стрептококки часто проявляют гораздо более выраженную тенденцию к распространению в организме и развитию смертельных состояний, чем стафилококки, несмотря на то, что стафилококки гораздо более губительны для тканей.

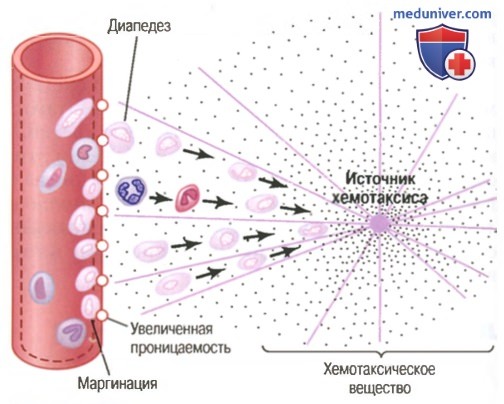
Движение нейтрофилов путем диапедеза через поры капилляров и путем хемотаксиса по направлению к области повреждения ткани
Реакции макрофагов и нейтрофилов во время воспаления
а) Тканевые макрофаги — первая «линия обороны» против инфекции. Тканевые макрофаги — первая «линия обороны» против инфекции. В течение нескольких минут после начала воспаления макрофаги, уже присутствующие в тканях, немедленно начинают свое фагоцитарное действие, будь то гистиоциты в подкожных тканях, альвеолярные макрофаги в легких, микроглия в мозге или др. При активации продуктами инфицирования и воспаления первым эффектом является быстрое увеличение каждого из макрофагов.
Затем многие из ранее неподвижных макрофагов отделяются от мест их прикрепления и становятся мобильными, формируя первую «линию обороны» против инфекции в течение примерно первого часа. Количество этих рано мобилизуемых макрофагов часто незначительно, но они спасают жизнь.
б) Вторжение нейтрофилов в воспаленную область является второй «линией обороны». В течение примерно первого часа после начала воспаления большое число нейтрофилов начинает внедряться в воспаленную область из крови. Этот процесс вызывается продуктами воспаленных тканей, которые инициируют следующие реакции:
(1) изменяют внутреннюю поверхность эндотелия капилляров, способствуя прилипанию нейтрофилов к стенкам капилляров в воспаленной области. Этот эффект, показанный на рисунке выше, называют маргинацией (или краевым стоянием лейкоцитов),
(2) ведут к разрыхлению сцеплений между эндотелиальными клетками капилляров и небольших венул, обеспечивая появление достаточно больших отверстий для прохождения нейтрофилов путем диапедеза непосредственно из крови в тканевые пространства;
(3) другие продукты воспаления вызывают хемотаксис нейтрофилов в направлении поврежденных тканей, как объяснялось ранее.
Таким образом, в течение нескольких часов после начала повреждения тканей область обильно заполняется нейтрофилами. Поскольку нейтрофилы крови — уже зрелые клетки, они готовы немедленно начать свои очистительные функции для уничтожения бактерий и удаления инородного материала.
— Также рекомендуем «Нейтрофилия. Защитные механизмы воспаления»
Оглавление темы «Клетки иммунитета. Виды иммунитета»:
1. Ретикулоэндотелиальная система. Макрофаги в лимфатических узлах
2. Альвеолярные макрофаги в легких. Клетки Купфера печени
3. Эффекты воспаления. Макрофаги и нейтрофилы при воспалении
4. Нейтрофилия. Защитные механизмы воспаления
5. Образование гноя. Эозинофилы и базофилы
6. Лейкопения. Лейкемии и его типы
7. Врожденный иммунитет. Приобретенный или адаптивный иммунитет
8. Типы приобретенного иммунитета. Лимфоциты в приобретенном иммунитете
9. Длительность жизни белых клеток крови. Нейтрофилы и макрофаги
10. Роль лимфоцитарных клонов. Происхождение клонов лимфоцитов
Небольшое перемещение лейкоцитов из кровеносных сосудов в ткани – диапедез или так называемая эмиграция лейкоцитов – нормальное явление. Однако при воспалительных условиях этот процесс идет интенсивно и активно – лейкоциты используют в процессе эмиграции АТФ. И этот процесс уже выходит за пределы нормы.
Почему происходит эмиграция лейкоцитов
Основной фактор, вызывающий эмиграцию лейкоцитов, – положительная гемотаксия в очаге воспаления. Эмиграции способствует повышенная проницаемость сосудистой стенки, замедление кровообращения и экссудации.
Эмиграция лейкоцитов следует за экссудацией, она начинается при артериальной гиперемии, но достигает пика при венозной гиперемии и застое. Экссудация происходит в основном из капилляров и вен, тогда как эмиграция лейкоцитов происходит из капилляров, вен и мелких вен.
Венозный застой
Эндотелиальные клетки сосудов прикрепляются к непрерывной базальной мембране, состоящей из коллагеновых волокон и гомогенного вещества, богатого комплексами белковых полисахаридов. В нормальных условиях эндотелиальная поверхность покрыта тонким слоем фибринового вещества, примыкающего к фиксированному слою плазмы крови, который, в свою очередь, граничит с движущейся частью плазмы.
Как протекает эмиграция лейкоцитов в очаг воспаления
Эмиграцию лейкоцитов в очаг воспаления можно разделить на три периода:
- Адгезия лейкоцитов. Так называемое крайнее положение. Которая длится от нескольких минут до одного часа,
- Прохождение лейкоцитов через эндотелий сосудов – длится несколько минут.
- Лейкоциты перемещаются к очагу воспаления и в тканях очага воспаления – длится много часов и даже дней.
Миграция лейкоцитов к месту повреждения
С адгезией лейкоцитов меняется расположение этих элементов на поверхности венозного эндотелия. В нормальных условиях лейкоциты не касаются слоя фибрина, но в случае воспаления структура фибринового цемента изменяется, и внутренняя поверхность сосуда выстлана чешуйчатым материалом, содержащим кислые мукополисахариды, мукопротеины и соляную кислоту. Нити фибрилл могут пересекать просвет даже мелких кровеносных сосудов.
Когда скорость кровообращения снижается, эти нити захватывают белые кровяные тельца, и они контактируют с измененным слоем фибринового цемента. Прежде чем прикрепиться к эндотелию сосудов, лейкоциты часто совершают очень сложные траектории движения – даже против кровотока.
Считается, что адгезия лейкоцитов к эндотелию определяется электрохимическими силами – потерей отрицательного заряда лейкоцитов и специфических химических связей между мембранами контактирующих клеток.
После адгезии к эндотелию сосудов нейтрофил развивает цитоплазматическое расширение, которое проникает между эндотелиальными клетками и образует отверстие в базальной мембране. Важную роль в изменении молекулярной структуры базальной мембраны и повышении ее проницаемости играют ферменты лейкоцитарных гранул (эластаза, коллагеназа).
Гранулы лейкоцитов также содержат катионные белки, которые также действуют на стенку кровеносных сосудов и способствуют эмиграции.
Первоначально в изгнании эмигрирующей клетки органелл нет. Затем за удлинением следует остальная масса гранулоцитов с ядром и гранулами. Эти клетки перемещаются к месту воспаления со скоростью от 6 до 12 микрон в минуту.
Разновидности гранулоцитов
На эмиграцию гранулоцитов влияет тип воспаления. Например, в случае бактериального воспаления эмигрируют в основном нейтрофилы, но в экссудате аллергического воспаления много лимфоцитов и эозинофилов. Гранулы этих лейкоцитов содержат вещества, инактивирующие гистамин, серотонин и, возможно, хинины, которых много в тканях в условиях гиперчувствительности.
Эмиграция моноцитов и лимфоцитов немного отличается от эмиграции нейтрофилов. Нейтрофилы мигрируют через эндотелиальную щель, а моноциты и лимфоциты мигрируют через эндотелий. После попадания в эндотелиальную клетку вокруг них образуется большая вакуоль. Попадая в него, моноцит и гимфоцит проходят через эндотелиальную клетку.
Эмиграция лимфоцитов и моноцитов – более медленный процесс, эти клетки позже появляются в воспаленных тканях и образуют второй слой или лейкоциты.
Хемотаксис
Хемотаксис – это активное движение лейкоцитов либо в направлении определенных химических раздражителей, либо от них.
В первом случае речь идет о положительной хемотаксии, а во втором – об отрицательной. Положительный хемотаксис играет роль на всех стадиях эмиграции лейкоцитов, особенно когда эти клетки уже покинули кровеносный сосуд и мигрируют во внесосудистое пространство.
И. Мечников первым наблюдал активное движение лейкоцитов к очагу воспаления и описал так называемый закон эмиграции лейкоцитов. Согласно ему, гранулоциты очень чувствительны к раздражителям хемотаксиса – так называемым гемоаттрактантам, поэтому они первыми эмигрируют к очагу воспаления. Хемотаксис моноцитов и лимфоцитов против этих раздражителей ниже. За гранулоцитами следуют моноциты и, наконец, лимфоциты.
Химические раздражители, вызывающие положительный гемотаксис, изучены достаточно подробно. Они делятся на две группы – хемотаксины и хемотаксигены.
- Хемотаксины – это вещества, которые могут привлекать лейкоциты.
- Хемотаксигены сами по себе не вызывают хемотаксии, но способствуют образованию хемотаксинов.
Примерами нейтрофильных хемотаксинов являются денатурированные белки, калихреин, компоненты комплемента (C3, C5), бактериальные токсины и гемотаксигены – трипсин, плазмин, коллагеназа, крахмал, гликоген, комплексы антиген-антитело. Хемотаксис подавляется гидрокортизоном. простагландины Ei и E2, цАМФ, колхицин.
Хемотаксины макрофагов представляют собой бактериальные культуры (Streptococcus pneumoniae, Corynebacteria) фильтрат белковых фракций, компонента С5а комплемента и др., кроме хемотаксигенов – липополисахаридов кишечных микробов, микобактерий, фракций лизосом лейкоцитов, протеиназ макрофагов.
Лейкоциты эозинофилов являются факторами хемотаксиса эозинофилов (высвобождаемых аллергеном и IgE из легких и гладких мышц), лимфокинов и других, но хемотаксигены представляют собой различные иммунные комплексы, а также продукты агрегации IgG и IgM.
Хемотаксис и активация лейкоцитов
В настоящее время считается, что реципиенты различных хемоаттрактантов присутствуют на поверхности эмигрирующих клеток (макрофагов). Например, были изучены рецепторы на поверхности макрофагов на Fc-фрагменте иммуноглобулинов, компоненте C3 комплемента и лимфокинах. Контакт клеточной мембраны с хемоаттрактантом изменяет мембранный потенциал, увеличивает проницаемость мембраны, увеличивает транспорт ионов Ca и Mg в клетке. Эти ионы контролируют функцию сокращения актомиозина. Активация микрофибрилл и внутриклеточной канальцевой системы способствует гематокриту и эмиграции лейкоцитов.
Отток экссудата способствует прохождению лейкоцитов через эндотелиальную щель. Кроме того, движение лейкоцитов также связано с некоторыми физико-химическими факторами. Воспалительные сурфактанты (аминокислоты, полипептиды) уменьшают поверхностное натяжение поверхности лейкоцитов и образование цитоплазматического объема на их поверхности, но положительно заряженные тканевые макромолекулы снижают отрицательный заряд лейкоцитов, нарушая электростатическую стабильность лейкоцитарной мембраны. Однако основную роль играют активные движения лейкоцитов, использующие энергию мацергических соединений.
Эмигрантские лейкоциты играют важную роль в дальнейшем развитии воспаления. Эти клетки являются источником биологически активных веществ. Однако главная из них – фагоцитарная функция лейкоцитов.
Продолжение статьи
- Часть 1. Этиология и патогенез воспаления. Классификация.
- Часть 2. Особенности обмена веществ при воспалении.
- Часть 3. Физико – химические изменения. Роль нервной и эндокринной систем в развитии воспаления.
- Часть 4. Изменения в периферическом кровообращении при воспалении.
- Часть 5. Экссудация. Экссудат и транссудат.
- Часть 6. Эмиграция лейкоцитов. Хемотаксис.
- Часть 7. Фагоцитоз. Асептическое и острое воспаление.
- Часть 8. Распространение. Последствия. Принципы лечения воспаления.
Поделиться ссылкой:
Фагоцитоз – это способность определенных клеток (фагоцитов) удерживать и переваривать плотные частицы. Это явление было открыто И. Мечниковым.
Фагоцитоз осуществляется микрофагами (нейтрофилами) и системой мононуклеарных макрофагов.
Мононуклеарные макрофаги
Система (MMS) включает следующие элементы:
- промоноциты (костный мозг);
- моноциты (кровь);
- тканевые макрофаги;
- гистиоциты соединительной ткани;
- печеночные клетки Куппера;
- легочные альвеолярные макрофаги;
- свободные и фиксированные макрофаги лимфатической ткани;
- плевру и перитонеальные макрофаги.
Клетки мононуклеарной системы объединяет общее происхождение гемопоэтических клеток и саморегуляция.
Моноцитопоэз
Моноцитопоэз – это стимулирующий фактор колонии фибробластов и фактор роста макрофагов, но он же подавляет (отрицательная саморегуляция) интерферон фибробластов и лейкоцитов и т. д.
Процесс фагоцитоза делится на четыре стадии:
- Приближение.
- Адгезия.
- Оседание;
- Стадия пищеварения.
Фаза приближения
Фагоцит приближается к объекту – бактериям, мервому клеточному элементу, инородному объекту. При движении под действием хемотаксиса цитоплазма фагоцита образует удлинения (псевдоподии).
Адгезия
Способствует образованию аминополисахаридов на поверхности фагоцитов и перекрытию фагоцитарного объекта белками сыворотки, особенно иммуноглобулинами. Последний механизм по сути является опсонизацией – бактерии и поврежденные клетки перекрываются с IgM, IgG и компонентами комплемента (C3, C5 и др.), что облегчает адгезию к фагоциту.
Адгезия
Поверхность фагоцита заряжена отрицательно, поэтому адгезия лучше, если объект, подлежащий фагоцитозу, заряжен положительно. Менее фагоцитарны отрицательно заряженные объекты, такие как опухолевые клетки.
Оседание
Этап фагоцитации объекта – путь инвагинации. Сначала фагоцит образует углубление, а затем фагосому – вакуоль, содержащую объект, подлежащий фагоцитозу. НАДН-зависимая оксидаза в мембране фагоцитов активируется до образования фагосом; в результате O2 превращается в O 2 ~ (супероксид-анион) и образуется H 2 O 2.
Эти продукты обладают бактерицидным действием, а также вызывают образование свободных радикалов. Под действием пероксидаз и каталаз H 2 O 2 расщепляется и высвобождается молекулярный O 2. Свободные радикалы и активный молекулярный O 2 действуют на мембрану фагоцита и объект, подлежащий фагоцитозу, активируя перекисное окисление липидов.
Липопероксиды и свободные радикалы неустойчивы к лизосомным мембранам и способствуют высвобождению лизосомальных ферментов.
Стадия пищеварения
Лизосомы присоединяются к фагосоме, содержащей фагоцитарный объект. Эти органеллы содержат все ферменты, необходимые для расщепления углеводов, белков, жиров и нуклеиновых кислот. В еще неактивной форме они попадают в вакуоль фагоцитов.
Пищеварительная вакуоль образуется при pH около 5,0, близком к оптимальному для лизосомальных ферментов. Активируются лизосомальные ферменты, и фагоцитарный объект постепенно переваривается. Во время стадии пищеварения проницаемость мембраны фагосомы увеличивается, содержимое фагосомы ускользает в цитоплазму, и микрофаг умирает (этому процессу способствует ацидоз). В этом случае фагоцитарный микроорганизм также может сохранять жизнеспособность.
Роль макрофагов в воспалительном процессе
Макрофаги начинают участвовать в фагоцитозе позже микрофагов. Макрофаги также более устойчивы к гипоксии и ацидозу, например, моноциты жизнеспособны даже при pH 5,5.
В очаге воспаления макрофаги выполняют несколько функций:
- Фагоцитируют бактериальные остатки, оставшиеся после эвакуации гноя и продуктов распада тканей – очищающая функция;
- Высвобождают лизосомальные ферменты – гиалуронидазу, аминопептидазу и др;
- Синтезируют компоненты системы комплемента и простагландины.
Взаимодействие макрофагов и лимфоцитов при хроническом воспалении
В то же время воспаленная тканевая среда также стимулирует образование фибробластов и фиброцитов. Постепенно появляется новая, богатая сосудами грануляционная ткань.
Фагоцитоз стимулируется продуктами повреждения тканей – внутриклеточные белки, ферменты, полипептиды, аминокислоты, электролиты и т. д., биологически активными веществами, половыми гормонами, тироксином, адреналином, лихорадкой. Но подавляется недостатком стимулирующих факторов, глюкокортикоидов, гликолортикоидов, ацетилхолина, ацетилхолина.
Фагоцитоз
Считается, что клетки плаценты и злокачественные опухоли способны секретировать вещество, которое подавляет функцию макрофагов, иммунологические реакции лимфоцитов и эмиграцию лейкоцитов, что приводит к значительному ослаблению или даже прекращению воспаления.
Объекты, которые фагоциты не могут переваривать, остаются в этих клетках в течение длительного времени и покрываются тонкой пленкой аминополисахаридов. После гибели фагоцитов они повторно фагоцитируются или выводятся из организма. Процесс, при котором фагоцит после переваривания высвобождает часть продуктов своего фагоцитоза в окружающую среду, называется экструзией.
Фагоцитоз – не единственный в организме механизм борьбы с воспалением. Большинство микроорганизмов погибают в условиях ацидоза, а также от ферментов, высвобождаемых во время гибели клеток и функционирования иммунокомпетентной системы.
Нейтрофилы во внеклеточном пространстве секретируют катионные белки, которые могут убивать ферменты без ферментов и фагоцитоза. Таким образом, воспалительные очаги постепенно избавляются от микроорганизмов и мертвых клеток.
Асептическое и острое воспаление
Дальнейшее течение воспаления зависит от того, является ли воспаление асептическим или бактериальным.
В асептических воспалительных условиях, например, вокруг хирургического шва, инородного тела, стенка микрофагов (нейтрофилов) начинает формироваться в течение нескольких часов, достигая максимума в течение дня.
Позже появляется следующий вал макрофагов, который достигает максимума через 2-3 раза. в день. Эмигрировавшие лейкоциты постепенно становятся неподвижными, больше не могут делиться и погибают в течение 3-5 дней. 2-3. на 5 сутки начинает формироваться стенка фибробластов, а на 5 сутки – соединительнотканная капсула.
Таким образом, в случае острого воспаления патогенный агент в организме преобразует белки, которые участвуют в реакции антиген-антитело, медиаторы и модуляторы воспаления, систему фагоцитов и миграцию клеток. В результате заканчивается острое воспаление. Однако, если инфекционные агенты попадают в участок асептического воспаления, например, в результате травмы, это воспаление становится септическим (бактериальным) воспалением.
Бактериальные воспалительные состояния бактерий и токсинов, не вызывающие гиперемии, экссудации и эмиграции лейкоцитов. Между клетками воспаленных тканей и особенно вокруг кровеносных сосудов накапливается все больше и больше микрофагов. Лизосомы микрофагов содержат множество активных ферментов, и эти клетки также начинают процесс фагоцитоза. При пальпации воспаленная ткань в это время кажется плотной, поэтому это называется стадией воспалительной инфильтрации.
По мере прогрессирования воспаления лейкоциты и те тканевые клетки, которые претерпели необратимые изменения во время воспаления, погибают. В этих клетках высвобождаются лизосомальные ферменты, которые расщепляют тканевые белки, белковые и липидные комплексы и другие структуры. Это стадия гнойного размягчения воспаления.
Эти стадии наблюдаются, например, у пациентов с гнойным воспалением перикарда (фурункул), гнойным воспалением апокринных потовых желез (гидраденит) и гнойным воспалением соединительной ткани (флегмона). При вдыхании воспаленная ткань выглядит мягкой, с характерным раскачиванием – флюктуацией. Образуется замкнутое скопление гноя – абсцесс.
Гнойное воспаление перикарда
Гной разрывается в направлении наименьшего сопротивления (либо наружу, либо внутри тела). Если гной попадает в кровоток (пемия), в организме может развиться множество очагов гноя, но под действием микроорганизмов и токсических веществ – угрожающее общее заболевание (сепсис, септикопиемия). Поэтому важно диагностировать накопление гноя и обеспечить хирургический дренаж гноя наружу.
Продолжение статьи
- Часть 1. Этиология и патогенез воспаления. Классификация.
- Часть 2. Особенности обмена веществ при воспалении.
- Часть 3. Физико – химические изменения. Роль нервной и эндокринной систем в развитии воспаления.
- Часть 4. Изменения в периферическом кровообращении при воспалении.
- Часть 5. Экссудация. Экссудат и транссудат.
- Часть 6. Эмиграция лейкоцитов. Хемотаксис.
- Часть 7. Фагоцитоз. Асептическое и острое воспаление.
- Часть 8. Распространение. Последствия. Принципы лечения воспаления.
