Углеводный обмен при воспалении
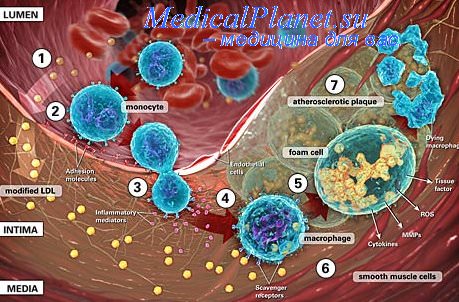
На начальном этапе воспаления в ткани
(не только зоны первичной, но и вторичной
альтерации) преобладают реакции
катаболизма, затем — при развитии
артериальной гиперемии и активации
процессов пролиферации, как правило,
начинают доминировать анаболические
реакции.
Углеводный обмен: в очаге воспаления
метаболизм углеводов претерпевает
характерные изменения, выражающиеся в
преобладании гликолиза и развитии
ацидоза.
Проявления
увеличение поглощения тканью кислорода
при одновременном снижении эффективности
окисления глюкозы в процессе тканевого
дыхания;активация гликогенолиза и гликолиза;
уменьшение уровня АТФ в ткани;
накопление избытка лактата и пирувата.
Липидный обмен: обмен липидов в
очаге воспаления характеризуется
доминированием липолиза над реакциями
их синтеза.
Проявления
активация процессов липолиза и накопление
продуктов липолизаторможение реакций синтеза липидов
активация перекисного окисления липидов
и накопление перекисей и гидроперекисей
липидов
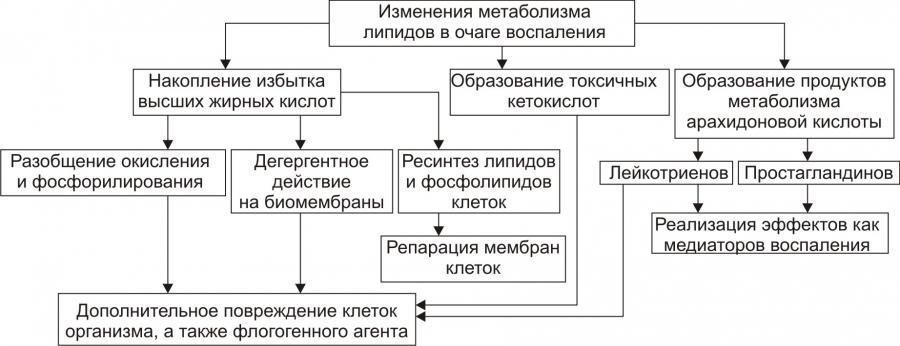
Рис. 7. — Изменения
метаболизма липидов в очаге воспаления
(по П.Ф. Литвицкому,
2002)
Белковый обменхарактеризуется
преобладанием протеолиза над процессами
протеосинтеза.
Проявления
активация процессов протеолиза и
накопление продуктов протеолиза.торможение реакций протеосинтеза.
денатурация молекул белка (образование
аутоантигенов).
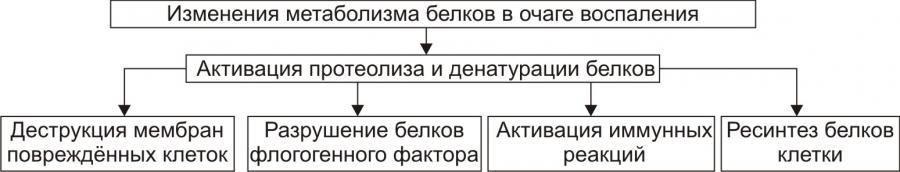
Рис. 8. — Изменения
метаболизма белков в очаге воспаления
(по П.Ф. Литвицкому,
2002)
Обмен ионов и воды
Для ионов и воды характерен трансмембранный
дисбаланс ионов, увеличение внутриклеточного
содержания Na+иCa2+и внеклеточного содержанияK+и Mg2+, гипергидратация клеток и
отёк ткани в очаге воспаления.
Проявления
нарушения распределения ионов по обе
стороны плазмолеммы; происходит потеря
клеткой K+,Mg2+,
микроэлементов и накопление их в
межклеточной жидкости. В клетку же
поступаютNa+,Ca2+и некоторые другие ионы.нарушения соотношения между отдельными
ионами как в клетке, так и вне клетки в
результате расстройства механизмов
трансмембранного переноса ионов.гипергидратация ткани в очаге воспаления
в связи с высокой гидрофильностью
накапливающихся в нём Na+иCa2+, а также
продуктов гидролиза органических
соединений.высвобождение дополнительного количества
катионов (K+,Na+,Ca2+, железа, цинка)
при гидролизе солей, распаде гликогена,
белков и др. органических соединений,
а также клеточных мембран.выход большого количества Ca2+из повреждённых внутриклеточных депо
(митохондрий и цистерн эндоплазматической
сети и митохондрий).
Медиаторы воспаления
В ходе первичной и вторичной альтерации
высвобождаются большие количества
разнообразных медиаторов и модуляторов
воспаления.
Медиаторы воспаления — БАВ, образующиеся
при воспалении, обеспечивающие
закономерный характер его развития и
исходов, формирование местных и общих
признаков. По происхождению делятся на
гуморальные (образующиеся в жидких
средах — плазме крови и тканевой
жидкости) иклеточные. Всегуморальные
медиаторы являются предсуществующими,
т.е. имеются в виде предшественников
до активации последних (производные
комплемента, кинины и факторы свертывающей
системы крови).Среди клеточных
медиаторов выделяют предсуществующие
(депонированные в клетках в неактивном
состоянии) — вазоактивные амины,
лизосомальные ферменты, нейропептиды,
ивновь образующиеся (т.е. продуцируемые
клетками при стимуляции) — эйкозаноиды,
цитокины, лимфокины, активные метаболиты
кислорода (таб. 2–4).
Таблица 2. Клеточные предшествующие
медиаторы воспаления
Основные | Основные | Основные | Основные |
Вазоактивные | Гистамин | Базофилы Тучные клетки Тромбоциты | Вазодилятация Повышение Спазм |
Серотонин | Тромбоциты | Зуд Угнетение Стимуляция | |
Лизосомальные | Протеиназы | Гранулоциты | Тканевая Усиление эмиграции Пролиферация |
Неферментные | Гранулоциты | Микробицидность Повышение Дегрануляция Адгезия | |
Нейропептиды | Вещество | С-волокна | Вазодилятация Повышение Дегрануляция Спазм |
Нейромедиаторы | Ацетилхолин | Холинергические | Вазодилятация Спазм гладкой Стимуляция |
Таблица 3. Клеточные, вновь образующиеся,
медиаторы воспаления
Основные | Основные | Основные | Основные эффекты |
Производные (эйкозаноиды) | Простагландины | Моноциты-макрофаги | Активация Вазодилятация Боль |
Тромбоксаны | Моноциты | Агрегация Спазм гладкой Активация | |
Лейкотриены Гидроокси- и Липоксины | Моноциты-макрофаги | Активация Повышение Вазодилятация Спазм | |
Фосфолипиды | Фактор, | Гранулоциты | Спазм гладкой Повышение Активация Агрегация |
Монокины | Интерлейкин-1 Фактор | Моноциты-макрофаги | Активация Пролиферация и Усиление фагоцитоз Стимуляция Стимуляция |
Лимфокины | Фактор, | Т-лимфоциты | Активация и Активация |
Активные | Супероксид-анион Гипохлорид | Гранулоциты | Тканевая деструкция Активация Стимуляция Угнетение |
Другие | Окись | Моноциты-макрофаги | Тканевая деструкция Активация |
Таблица 4. Гуморальные медиаторы
воспаления
Основные | Основные | Основные | Основные эффекты |
Производные | С5b-С9 С5а des С5аС3а | Плазма Тканевая жидкость | Тканевая деструкция Активация Повышение Дегрануляция Спазм гладкой |
Кинины | Брадикинин Каллидин | Плазма Тканевая | Вазодилятация Повышение Спазм гладкой Угнетение Стимуляция Боль |
Факторы | Фибринопеп-тиды Продукты деградации | Плазма | Активация Усиление фагоцитоза |
Изменения углеводного, жирового и белкового обмена в очаге воспаления многоплановы и динамичны, поскольку на каждой стадии процесса между метаболическими реакциями возникают новые взаимосвязи, адекватные тем требованиям, которые в каждый конкретный момент предъявляются к клеткам и тканям. Поэтому ниже будут определены только принципиальные изменения этих видов обмена веществ, что необходимо для понимания патогенеза воспалительной реакции.
Углеводный обмен. Начиная с самых ранних стадий воспалительного процесса, в его очаге резко возрастает потребность тканей в кислороде. Несмотря на возникающую артериальную гиперемию, а в дальнейшем — из-за венозной гиперемии, тканям начинает не хватать кислорода. В то же время в воспаленных тканях очень интенсивно используется приносимая в больших количествах с током крови глюкоза. В результате этого усиливается гликолиз, и, как следствие этого, в очаге воспаления происходит накопление больших количеств молочной кислоты.
Характерным для изменений углеводного обмена в очаге воспаления является отсутствие эффекта Пастера, заключающегося в том, что в присутствии кислорода тормозится анаэробное расщепление углеводов. Это обусловлено тем, что при анаэробном расщеплении углеводов на каждую молекулу глюкозы образуется 2 молекулы АТФ, а при аэробном — 38, то есть аэробный путь является гораздо более выгодным для клеток в энергетическом отношении. В условиях развития воспалительной реакции этот механизм нарушается и происходит интенсификация процессов анаэробного расщепления углеводов.
Жировой обмен. В крови, оттекающей от очага воспаления, повышается содержание свободных жирных кислот, так как в воспаленной ткани усиливаются процессы липолиза. Одновременно в этом регионе нарастает количество кетоновых тел, что свидетельствует не только об усилении, но и об извращении жирового обмена.
Белковый обмен. В воспаленных тканях происходит значительное усиление протеолитических процессов, в связи с чем здесь накапливается большое количество аминокислот и полипептидов. Последние в ряде случаев обладают высокой биологической активностью, инициируя ряд метаболических превращений, как в тканях, так и в экссудате.
Физико-химические изменения в очаге воспаления. Как было сказано выше, вследствие усиления гликолиза в тканях очага воспаления накапливается молочная кислота; нарушения липидного обмена ведут к увеличению концентрации свободных жирных кислот и кислых по своей реакции кетоновых тел. Это приводит к тому, что в очаге воспаления накапливается большое количество свободных ионов водорода, то есть развивается состояние ацидоза.
В динамике изменения кислотно-основного состояния при воспалении различают три фазы. В самый начальный период воспалительной реакции развивается кратковременный первичный ацидоз, связанный с ишемией, в процессе которой в тканях увеличивается количество кислых продуктов. При наступлении артериальной гиперемии кислотно-основное состояние в тканях воспалительного очага нормализуется, а затем развивается длительный выраженный метаболический ацидоз, который вначале является компенсированным (происходит снижение щелочных резервов тканей, но их рН не меняется). По мере прогрессирования воспалительного процесса развивается уже некомпенсированный ацидоз вследствие нарастания концентрации свободных водородных ионов и истощения тканевых щелочных резервов. Концентрация водородных ионов повышается тем больше, чем сильнее выражено воспаление. Для гнойного воспаления характерен очень низкий рН (5.0-4.0).
В тканях воспалительного очага происходит резкое изменение осмотического и онкотического давления. При альтерации клеток высвобождается большое количество внутриклеточного калия. В сочетании с увеличением количества водородных ионов это приводит к гиперионии в очаге воспаления, а последняя вызывает повышение осмотического давления. Накопление полипептидов и других высокомолекулярных соединений приводит к возрастанию онкотического давления. В результате возрастает степень гидратации тканей и их тургор, то есть напряжение, которое при воспалении увеличивается в 7-10 раз, что в свою очередь усиливает альтерацию тканей.
Биологически активные вещества в очаге воспаления. В очаге воспаления накапливается большое количество биологически активных веществ, которые меняют течение обменных процессов, вызывают дальнейшую альтерацию тканей и стимулируют процессы пролиферации. К таким веществам в первую очередь относятся лизосомные ферменты, которые, как уже говорилось, «запускают» процессы альтерации, повышают сосудисто-тканевую проницаемость, влияют на клеточный метаболизм и стимулируют пролиферацию.
Второй важной группой биологически активных веществ, концентрация которых в очаге воспаления повышена, являются простагландины. На роли этого класса соединений в динамике воспаления следует остановиться несколько подробнее. В настоящее время считается, что воспалительный агент через активацию фосфолипазы А действует на фосфолипиды клеточных мембран, приводя к образованию арахидоновой кислоты, являющейся основным предшественником простагландинов. При воздействии фермента циклооксигеназы начинается цепь превращений арахидоновой кислоты, в результате которых в очаге воспаления накапливаются простагландины, которые в настоящее время рассматриваются как важнейшие регуляторы воспаления. Они ускоряют кровоток в сосудах воспаленного участка, повышают сосудисто — тканевую проницаемость, усиливают влияние брадикинина на сосуды. Наблюдается тесная связь простагландинов с циклическими нуклеотидами — соединениями, инициирующими целый ряд внутриклеточных метаболических реакций. Установлено, например, что простагландин D повышает в клетке уровень цАМФ и, тормозя тем самым выброс медиаторов, ослабляет интенсивность развития воспалительной реакции. Другой, простогландин F, — повышает уровень клеточного цГМФ, усиливает выброс медиаторов и интенсифицирует течение воспаления.
Наконец, в очаге воспаления обнаружена группа активных полипептидов, которые вызывают повышение температуры тканей, ведут к их некрозу, стимулируют движение лейкоцитов, оказывают влияние на пролиферативные процессы.
Таковы основные нарушения обмена веществ в очаге воспаления.
Оглавление темы «Изменения клеток при воспалении.»:
1. Изменение клеток при воспалении. Изменение морфологии и обмена веществ при воспалении.
2. Метаболизм углеводов при воспалении. Нарушение обмена углеводов при воспалении.
3. Метаболизм липидов при воспалении. Нарушение обмена липидов при воспалении.
4. Метаболизм белков при воспалении. Нарушение обмена белков при воспалении.
5. Метаболизм ионов и воды при воспалении. Нарушение обмена ионов и воды при воспалении.
6. Физико-химические изменения в очаге воспаления. Ацидоз.
7. Гиперосмия в очаге воспаления. Гиперонкия в очаге воспаления.
8. Изменение поверхностного натяжения мембран в очаге воспаления. Изменения коллоидного состояния цитозоля в очаге воспаления.
9. Медиаторы воспаления. Виды медиаторов воспаления.
10. Биогенные амины. Серотонин. Адреналин. Норадреналин.
В очаге воспаления метаболизм углеводов претерпевает характерные изменения, выражающиеся в преобладании гликолиза и развитии ацидоза.
Причины нарушения обмена углеводов при воспалении.
• Повреждения мембранного аппарата и митохондриальных ферментов, возникающие под действием как флогогенного агента, так и других факторов, активирующихся или образующихся в ходе воспалительной реакции вторично. К этим последним относятся свободные радикалы и пе-рекисные соединения, вещества с детергентным действием (ВЖК, гидроперекиси липидов), гидролазы лизосом, избыток Н+ и других агентов.
• Избыток Са2+, оказывающий (наряду с жирными кислотами) существенное разобщающее действие на окислительное фосфорилирование.
• Увеличение в клетках уровня АДФ, АМФ и неорганического фосфата. Это активирует ключевые (лимитирующие) ферменты гликогенолиза и гликолиза. В связи с этим в очаге воспаления начинает возрастать удельный вес гликолитического ресинтеза АТФ.

Проявления нарушения обмена углеводов при воспалении.
• Увеличение поглощения тканью кислорода при одновременном снижении эффективности окисления глюкозы в процессе тканевого дыхания.
• Активация гликогенолиза и гликолиза.
• Уменьшение уровня АТФ в ткани.
• Накопление избытка лактата и пирувата.
Последствия нарушения обмена углеводов при воспалении.
• Образующаяся при гликолизе АТФ, хотя и в недостаточной мере, но тем не менее может обеспечить поддержание энергозависимых процессов в клетках, особенно транспорта ионов и сокращения мышц, сохранение жизнеспособности и жизнедеятельности гистологических элементов в очаге воспаления.
• Активация гликолиза сопровождается накоплением в клетках и во внеклеточной жидкости избытка промежуточных продуктов этого процесса, в том числе пировиноградной, молочной и других кислот, что ведёт к формированию метаболического ацидоза.
• На начальном этапе воспаления (когда многие митохондрии сохраняют свою структуру, а их ферменты — кинетическую активность) возобновление нормальной или близкой к ней оксигенации тканей сопровождается быстрым восстановлением эффективности тканевого дыхания, снижением интенсивности гликолиза и нормализацией энергетического обеспечения клеточных процессов.
— Читать далее «Метаболизм липидов при воспалении. Нарушение обмена липидов при воспалении.»
Изменения углеводного, жирового и белкового обмена в очаге воспаления многоплановы и динамичны, поскольку на каждой стадии процесса между метаболическими реакциями возникают новые взаимосвязи, адекватные тем требованиям, которые в каждый конкретный момент предъявляются к клеткам и тканям. Поэтому ниже будут определены только принципиальные изменения этих видов обмена веществ, что необходимо для понимания патогенеза воспалительной реакции.
Углеводный обмен. Начиная с самых ранних стадий воспалительного процесса, в его очаге резко возрастает потребность тканей в кислороде. Несмотря на возникающую артериальную гиперемию, а в дальнейшем — из-за венозной гиперемии, тканям начинает не хватать кислорода. В то же время в воспаленных тканях очень интенсивно используется приносимая в больших количествах с током крови глюкоза. В результате этого усиливается гликолиз, и, как следствие этого, в очаге воспаления происходит накопление больших количеств молочной кислоты.
Характерным для изменений углеводного обмена в очаге воспаления является отсутствие эффекта Пастера, заключающегося в том, что в присутствии кислорода тормозится анаэробное расщепление углеводов. Это обусловлено тем, что при анаэробном расщеплении углеводов на каждую молекулу глюкозы образуется 2 молекулы АТФ, а при аэробном — 38, то есть аэробный путь является гораздо более выгодным для клеток в энергетическом отношении. В условиях развития воспалительной реакции этот механизм нарушается и происходит интенсификация процессов анаэробного расщепления углеводов.
Жировой обмен. В крови, оттекающей от очага воспаления, повышается содержание свободных жирных кислот, так как в воспаленной ткани усиливаются процессы липолиза. Одновременно в этом регионе нарастает количество кетоновых тел, что свидетельствует не только об усилении, но и об извращении жирового обмена.
Белковый обмен. В воспаленных тканях происходит значительное усиление протеолитических процессов, в связи с чем здесь накапливается большое количество аминокислот и полипептидов. Последние в ряде случаев обладают высокой биологической активностью, инициируя ряд метаболических превращений, как в тканях, так и в экссудате.
Физико-химические изменения в очаге воспаления. Как было сказано выше, вследствие усиления гликолиза в тканях очага воспаления накапливается молочная кислота; нарушения липидного обмена ведут к увеличению концентрации свободных жирных кислот и кислых по своей реакции кетоновых тел. Это приводит к тому, что в очаге воспаления накапливается большое количество свободных ионов водорода, то есть развивается состояние ацидоза.
В динамике изменения кислотно-основного состояния при воспалении различают три фазы. В самый начальный период воспалительной реакции развивается кратковременный первичный ацидоз, связанный с ишемией, в процессе которой в тканях увеличивается количество кислых продуктов. При наступлении артериальной гиперемии кислотно-основное состояние в тканях воспалительного очага нормализуется, а затем развивается длительный выраженный метаболический ацидоз, который вначале является компенсированным (происходит снижение щелочных резервов тканей, но их рН не меняется). По мере прогрессирования воспалительного процесса развивается уже некомпенсированный ацидоз вследствие нарастания концентрации свободных водородных ионов и истощения тканевых щелочных резервов. Концентрация водородных ионов повышается тем больше, чем сильнее выражено воспаление. Для гнойного воспаления характерен очень низкий рН (5.0-4.0).
В тканях воспалительного очага происходит резкое изменение осмотического и онкотического давления. При альтерации клеток высвобождается большое количество внутриклеточного калия. В сочетании с увеличением количества водородных ионов это приводит к гиперионии в очаге воспаления, а последняя вызывает повышение осмотического давления. Накопление полипептидов и других высокомолекулярных соединений приводит к возрастанию онкотического давления. В результате возрастает степень гидратации тканей и их тургор, то есть напряжение, которое при воспалении увеличивается в 7-10 раз, что в свою очередь усиливает альтерацию тканей.
Биологически активные вещества в очаге воспаления. В очаге воспаления накапливается большое количество биологически активных веществ, которые меняют течение обменных процессов, вызывают дальнейшую альтерацию тканей и стимулируют процессы пролиферации. К таким веществам в первую очередь относятся лизосомные ферменты, которые, как уже говорилось, «запускают» процессы альтерации, повышают сосудисто-тканевую проницаемость, влияют на клеточный метаболизм и стимулируют пролиферацию.
Второй важной группой биологически активных веществ, концентрация которых в очаге воспаления повышена, являются простагландины. На роли этого класса соединений в динамике воспаления следует остановиться несколько подробнее. В настоящее время считается, что воспалительный агент через активацию фосфолипазы А действует на фосфолипиды клеточных мембран, приводя к образованию арахидоновой кислоты, являющейся основным предшественником простагландинов. При воздействии фермента циклооксигеназы начинается цепь превращений арахидоновой кислоты, в результате которых в очаге воспаления накапливаются простагландины, которые в настоящее время рассматриваются как важнейшие регуляторы воспаления. Они ускоряют кровоток в сосудах воспаленного участка, повышают сосудисто — тканевую проницаемость, усиливают влияние брадикинина на сосуды. Наблюдается тесная связь простагландинов с циклическими нуклеотидами — соединениями, инициирующими целый ряд внутриклеточных метаболических реакций. Установлено, например, что простагландин D повышает в клетке уровень цАМФ и, тормозя тем самым выброс медиаторов, ослабляет интенсивность развития воспалительной реакции. Другой, простогландин F, — повышает уровень клеточного цГМФ, усиливает выброс медиаторов и интенсифицирует течение воспаления.
Наконец, в очаге воспаления обнаружена группа активных полипептидов, которые вызывают повышение температуры тканей, ведут к их некрозу, стимулируют движение лейкоцитов, оказывают влияние на пролиферативные процессы.
Таковы основные нарушения обмена веществ в очаге воспаления.
