Воспаление руки после химиотерапии

Восстановление после химиотерапии должно быть не полностью самопроизвольным, растянутым на месяцы процессом с неизвестными результатами. В любом случае через некоторое время неприятности лекарственного противоопухолевого лечения существенно уменьшатся, но восстановление пойдет быстрее и успешнее только под контролем врача, а лучше команды специалистов, отлично разбирающихся во всех аспектах реабилитации онкологических пациентов.
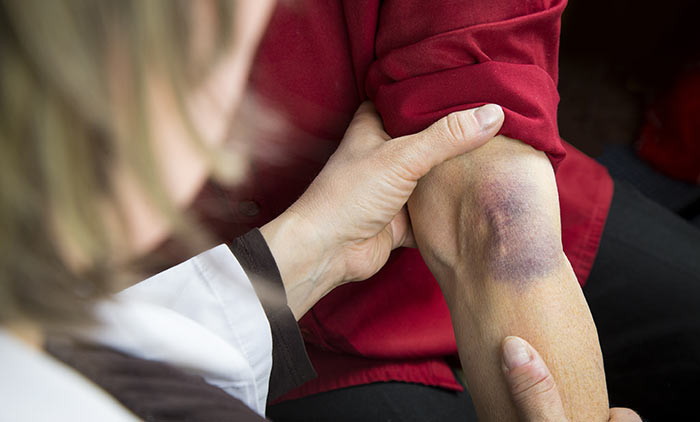
Причины появления синяков
Синяк или гематома у онкологических больных встречаются часто, потому что химиотерапия связана с внедрением в организм посредством разрушения кожных покровов — внутривенными введениями лекарств, что не всегда удается без кровоизлияния в кожу и клетчатку вокруг сосуда. Противоопухолевые лекарства изменяют состав крови, в частности численность тромбоцитов, увеличивая кровоточивость, а также впятеро повышают вероятность образования тромбов, тогда как хронически существующая варикозная болезнь увеличивает тромбообразование всего лишь вдвое.
Злокачественная опухоль меняет реологические свойства крови, приводя к образованию тромбов. У каждого пятого пациента ещё до операции выявляют скрытый тромбоз. При раке кишечника и поджелудочной железы обильное образование тромбов может быть первым признаком злокачественного заболевания. Химиотерапия, как и метастатическая стадия любой опухоли, увеличивает вероятность тромбоза в среднем в пять раз. В организме онкологического больного одновременно сосуществуют два процесса — избыточная кровоточивость и повышенная свертываемость.
Факторы риска тромбозов у онкобольных как у всех «обычных» людей: большой вес и возраст «после 40», хронические болезни сосудов и сердца, сахарный диабет, гипертония и конечно варикозная трансформация вен нижних конечностей.
К этим стандартным причинам у онкологического пациента примешиваются специфические, то есть инициируемые злокачественной опухолью и усугубляемые необходимым лечением:
- сдавливание опухолевым конгломератом кровеносных и лимфатических сосудов;
- лимфостаз после удаления подмышечных лимфоузлов, в результате облучения или удаления клетчатки малого таза с лимфоузлами, а также блок метастатическим паховыми узами оттока лимфы из ноги;
- длительный приём гормональных препаратов;
- стимуляция красного ростка кроветворения эритропоэтинами;
- постоянно установленный для частых вливаний лекарств венозный катетер;
- вынужденное из-за слабости ограничение подвижности;
- операции и облучение, а также побочные эффекты химиотерапии на сосуды и форменные элементы крови.
Для инициации тромба внутри сосуда больному раком достаточно всего трёх поводов и не обязательно сразу всех:
- повреждение внутренней оболочки сосуда, что для обычно для внутривенной химиотерапии;
- застой крови, что называют «нарушением кровообращения», в том числе в результате опухолевого конгломерата;
- избыточная свертываемость вместе с нарушением формирования сгустков.
Запись
на консультацию
круглосуточно
Симптомы воспаления вен после химиотерапии
Большинство химиопрепаратов применяется только в растворе, не в таблетках, что объясняется нестойкостью лекарственных молекул к желудочному соку и сильнейшим раздражающим действием цитостатика на слизистые оболочки желудочно-кишечного тракта. При непосредственном контакте цитостатика с венозной стенкой происходит его проникновение в клетки эндотелия с изменением структуры ДНК. Произошедшая химическая реакция направляет эндотелиальную клетку к воспалительным изменениям либо к смерти — апоптозу. Повреждение усугубляется травмой стенки вены инъекционной иглой или катетером.
Воспаление венозной стенки — флебит, к которому быстро подключаются факторы риска образования тромбов, и в поврежденной химиотерапией вене развивается тромбофлебит.
Флебит проявляется болью, причём в процессе введения цитостатика боль может быть очень интенсивной, и не только в месте инъекции, но по всей руке, когда больной как будто ощущает движение лекарства по сосудистой сети, так и говорят, что «вена горит». Боль может быть краткой, а может остаться на несколько дней и даже неделю, зависит это не только от выраженности ожога эндотелия, но и личностных особенностей больного по восприятию болевых ощущений.
Боль при прохождении лекарства приводит к спастическому сокращению вены, в ответ на которое расширяются впадающие в неё мелкие венки, на внутренней поверхности руки появляется сеточка из расширенных синих сосудиков на фоне побледневшей из-за спазма артериол кожи.
Воспаленную вену можно прощупать, она как тяж плотная из-за местной отечности тканей. Когда в просвете сосуда возникнет тромб, его тоже можно будет нащупать и увидеть при УЗ- дуплексном сканировании.
Со временем воспаление пройдет, уплотнение сосуда может остаться, кожа над ним может потемнеть. Внутренний просвет сосуда после нескольких химиотерапевтических ожогов уменьшится вплоть до закрытия — облитерации. За время течения флебита откроются и расширятся подходящие к больной вене мелкие сосудики — коллатерали, но останется вероятность небольшой отечности руки ниже места венозного повреждения.
Основные методы лечения вен
После внедрения цитостатика внутрь клеток остается только ждать завершения побочного процесса и помогать восстановлению.

Патофизиология лекарственного токсического флебита мало изучена, клинических исследований по проблеме не проводилось, все рекомендации базируются только на личном опыте медицинского персонала. В каждом случае и после каждого введения необходимо консультироваться с лечащим врачом, знающим особенности локального взаимодействия цитостатика и спектр местных побочных реакций.
Для купирования болевого синдрома и уменьшения воспаления лучше всего подходят НПВС — нестероидные противовоспалительные средства, но не доказано преимуществ какого-либо одного препарата, лучше опираться на «житейские» предпочтения пациента, потому что и чувствительность к боли разная, и обезболивающий эффект тоже индивидуален.
При высоком риске легочной тромбоэмболии пациенту назначается специальная — «разжижающая кровь» терапия, как правило, длительная — никак не менее недели и при регулярном контроле свертываемости.
Можно использовать мази с гепарином для втирания в зону поврежденного сосуда. Любимый пациентами гель Гепатромбин™ состоит из гепарина и преднизолона, последний имеет противовоспалительное действие, препарат официально не сертифицирован для использования при периферическом флебите и тромбофлебите.
Хорошая репутация у мази Троксевазин™ (троксерутин), одновременно уменьшающей воспаление и отечность тканей, изменяющей реологические свойства крови в сторону разжижения, но меньше, чем это присуще гепарину. Тем не менее, исследования показали, что препарат способен растворять микротромбы.
Гель Индовазин™ представляет смесь троксерутина и НПВС индометацина, поэтому уменьшает выраженность боли и делает всё, что присуще Троксевазину™. Нецелесообразно сочетать обе мази, поскольку спектр действий комбинированного препарата больше, но с Индовазином™ вполне можно чередовать нанесение Гепатромбина™. Всасывание мазей микроскопическое, они не подменяют собой принимаемые внутрь НПВС и антикоагулянты, но помогают перенести неприятные последствия лечения.
Как восстанавливаются вены после капельниц: полезные процедуры
Местное раздражение слизистой, выстилающей внутреннюю стенку вены, пытаются уменьшить большим разведением и медленным введением в капельницах, буквально часами. Не все цитостатики выдерживают большое разведение и долгое введение, некоторые теряют свои свойства, поэтому их вводят болюсно — шприцем. В этом случае сразу же после химиопрепарата вену «моют» физиологическим раствором, стараясь уменьшить её повреждение.
Обязательно до введения и в процессе капельницы неоднократно проверяется проходимость сосуда и возможность экстравазации — распространение цитостатика в клетчатке при микроскопических разрывах сосудистой стенки.
Рекомендуется не делать химиотерапию в одну и ту же вену, лучше чередовать руки, давая сосуду больший срок на восстановление своей слизистой оболочки. Профилактическое использование мазей с гепарином или троксерутином до химиотерапии лишено патоморфологических оснований, то есть бесполезно.
При планировании многомесячной химиотерапии целесообразно подумать об установке венозного порта, срок его службы, как минимум, пятилетка. Устройство полностью исключает такой побочный эффект как лекарственный флебит, но от тромбозов спасает только приём антикоагулянтов.
Профилактика осложнений
Многие цитостатики повреждают вены, особенно усердны в инициации химических флебитов агрессивные цисплатин, антрациклины и винкаалкалоиды, а также сравнительно «мягкие» гемцитабин с фторурацилом. По действию на ткани антрациклины с винкаалкалоидами отнесены к кожно-нарывным, цисплатин всего лишь к раздражающим, а гемцитабин точно не кожно-нарывной. Тем не менее любой химиопрепарат, а тем более комбинация цитостатиков, способны повредить вену, поэтому во время внутривенного введения персонал должен строго исполнять инструкцию по длительности и способу инъекции.
Помогают восстановлению физиотерапевтические процедуры и акупунктура, фототерапия и инфракрасное облучение, стимуляция магнитным полем.
В нашей Клинике каждому больному проводится определённая и ориентированная на особенности организма и сопротивляемость тканей программа сопровождения химиотерапии и восстановления после лечения.
Запись
на консультацию
круглосуточно
Список литературы:
- Российские клинические рекомендации по профилактике и лечению венозных тромбоэмболических осложнений у онкологических больных// М.: Планида; 2012
- Сомонова О.В., Антух Э.А., Елизарова А.Л., с соавтр. /Практические рекомендации по профилактике и лечению тромбоэмболических осложнений у онкологических больных // Злокачественные опухоли: Практические рекомендации RUSSCO #3s2; 2017 (том 7).
- Antithrombotic Therapy and Prevention of Thrombosis, 9th ed: American College of Chest Physicians Evidence-Based Clinical Practice Guidelines// Chest Am Coll Chest Phys.; 2012.
- Jones S., Holmes F., O´Shaughnessey J., et al. /Docetaxel with cyclophosphamide is associated with an overall survival benefit compared with doxorubicin and cyclophosphamide: 7-year follow-up of US Oncology Research trial 9735// JCO 2009; 27.
- International Society of Lymphology. The diagnosis and treatment of peripheral lymphedema: 2013 Consensus Document of the International Society of Lymphology// Lymphology; 2013 Mar; 46(1).
- Khorana A.A., Kuderer N.M., Culakova E., et al./ Development and validation of a predictive model for chemotherapy-associated thrombosis// Blood 2008; 15.
Сильнодействующие яды, входящие в состав медикаментов, используемых при лечении раковой опухоли, оказывают негативное воздействие не только на очаг поражения, но и на кровеносные сосуды. Поэтому внимание также важно уделять восстановлению вен после химиотерапии. В настоящее время существует множество средств для устранения этой проблемы. Однако нужно понимать, какие из них будут более эффективны и менее опасны для человеческого здоровья.
Способы восстановления вен после химиотерапии
После прохождения курса химиотерапевтической терапии с помощью капельного введения лекарства онкобольные часто жалуются на появление некоторых осложнений. В частности, в местах проколов иглами начинают образовываться уплотнения и синяки. Кроме того, нередко возникает такое состояние, при котором вены начинают уходить глубоко в ткани.
При появлении первых признаков развития воспалительного процесса нужно сразу проконсультироваться с флебологом или хирургом. При отсутствии соответствующего лечения патология может перейти в гнойную форму, что затем приведет к некрозу.
Восстановить вены после химиотерапии можно, если регулярно наносить на поврежденные участки йодовые сетки. Делать такую процедуру нужно несколько раз в течение дня.
По теме
Если формирование уплотнения сопровождается высокой температурой тела и покраснением участка в месте введения иглы, лечить такое состояние необходимо при помощи нестероидных препаратов противовоспалительной группы.
Чтобы восстановить работу кровеносных сосудов, специалист пропишет антикоагулянты.
Кроме того, возникшее осложнение требует ношения тугой повязки, которую накладывают на проблемные участки.
Восстановить вены на руках и ногах также можно при помощи обезболивающих и противовоспалительных мазей. Их наносят на участок кожи, расположенного непосредственно над очагом поражения.
Среди наиболее эффективных медикаментозных средств для наружного применения выделяют следующие.
Троксевазин
Эта мазь для вен после химиотерапии относится к категории флавоноидов. Объясняется это тем, что основным действующим веществом в ее составе выступает производное рутина.
Препарат обладает венотонизирующими свойствами и направлен на решение таких задач, как:
- уменьшить ломкость и проницаемость кровеносных сосудов;
- снять воспалительный процесс;
- повысить тонус вен;
- укрепить сосудистые стенки;
- предотвратить развитие тромбозов.
По теме
Также Троксевазин обладает противосвертывающими, антиоксидантными и противоотечными действиями. Чтобы получить максимальный эффект от применения такой мази, специалисты рекомендуют одновременно пить этот же препарат, но только выпускаемый в виде капсул.
Гель необходимо наносить на поврежденные участки утром и в вечернее время легкими круговыми движениями. При этом руки нужно обмотать тугой повязкой, а на пораженные нижние конечности надеть эластичные чулки.
Гепатромбин
Такой препарат хорошо помогает при лечении ожога вен после химиотерапии. Особенность его заключается в противотромботических и антикоагулянтных свойствах. При длительном использовании мази из вен начинают выводиться вредные продукты. Также восстанавливаются регенерирующие процессы в тканях, снимается отечность.
В итоге отмечается восстановление структуры сосудистых стенок. Как правило, происходит их очищение от токсических соединений, нормализуется кровообращение.
Высокая эффективность от применения Гематромбина достигается за счет наличия в его составе натрия гепарина.
По теме
В качестве вспомогательных компонентов выступают дексапантенол и аллантоин. Эти вещества способствуют более глубокому проникновению гепарина внутрь вен, за счет чего отмечается усиление оказываемого действия. Сама кожа при этом не затрагивается.
Если в патологический процесс были вовлечены вены нижних конечностей, то мазь нужно накладывать в направлении снизу вверх.
Индовазин
В составе этого препарата выделяется два основных компонента – это индометацин и троксерутин. Первый отличается нестероидными свойствами, второй более эффективен при развитии венозной недостаточности.
После использования мази будет наблюдаться следующий результат:
- устранение болевого синдрома;
- оказание тонизирующего действия;
- снятие воспаления и отечности;
- предупреждение образования сгустков крови на стенках сосудов;
- подавление синтезирования простагландинов;
- уменьшение проницаемости и ломкости;
- ускорение восстановления поврежденных вен и рядом расположенных тканевых структур.
По теме
В результате вены после ожога восстанавливаются, нормализуется микроциркуляция. Мазь легко наносится и быстро проникает к пораженным участкам.
Если химиотерапия планируется на несколько месяцев, то в вену рекомендуют вставлять специальный порт. Он позволит предупредить развитие лекарственного флебита. Чтобы не было тромбозов, врач порекомендует препараты группы антикоагулянтов.
Токсическое действие на кожу и ее придатки
Поражения кожи токсического генеза относительно стандартны по проявлениям и свойственны отдельным цитостатикам и группам препаратов.
Часть кожных реакций носит отчетливо аллергический характер.
Ранние побочные эффекты выражаются появлением эритемы, уртикарной сыпи и могут сопровождаться кожным зудом, повышением температуры тела и снижением чувствительности с последующим развитием гиперестезии и парестезии.
Позднее они способны трансформироваться в довольно стойкие дерматопатии типа гиперкератоза, продуктивной (нередко бляшковидной) сыпи, десквамации с возможным развитием вторичной инфекции, гиперпигментации (кожи, ногтей, слизистых оболочек).
Гиперпигментация кожи в виде четко очерченных пятен или полос характерна для блеомицина, пепломицина, бусульфана. Фотосенсибилизирующий эффект наблюдается при лечении фторурацилом и дакарбазином. Множественные склеротические изменения кожи (нодулярные образования в ее толще), гиперкератоз, иногда некрозы — довольно характерные осложнения химиотерапии (XT) блеомицином.
Кожные лучевые реакции (эритема, десквамация, гиперпигментация) могут отмечаться в процессе лечения дактиномицином или после его окончания. Для прокарбазина (Натулан) характерны клинические изменения в виде эритематозных (кореподобных) экзантем, для метотрексата — макулопапулезных высыпаний. Токсикодермии при лечении противоопухолевыми антибиотиками обычно протекают более тяжело и с выраженным ульцеративно-экссудативным компонентом.
При использовании таксанов отмечаются гиперкератозы, десквамация кожи, сыпь, кожный зуд, изменение ногтей. Кожная токсичность более выражена при лечении доцетакселом. При лечении капецитабином, 5-ФУ в виде длительных инфузии, пегилированным липосомным доксорубицином, со-рафенибом часто отмечается избирательная десквамация, отек, гиперемия кожи стоп и кистей (ладонно-подошвенная эритродизестезия).
Ладонно-подошвенный синдром (ЛПС) I степени не нарушает повседневной активности больного и проявляется онемением, дизестезиями и парестезиями, покалыванием или покраснением ладоней и/или подошв, физическим дискомфортом. ЛПС II степени характеризуется болезненным покраснением кожи и отеками кистей и/или стоп, причем вызываемый этими симптомами дискомфорт нарушает повседневную активность пациента.
При ладонно-подошвенном синдроме III степени наблюдается влажная десквамация, изъязвление, образование пузырей и резкая боль в кистях и/или стопах, а также сильный дискомфорт, делающий невозможными для пациента любые виды повседневной активности. При ЛПС II или III степени применение препарата нужно прервать до исчезновения симптомов или их уменьшения до I степени. IV степень токсичности характеризуется наличием инфицированных осложнений, требующих госпитализации.
В настоящее время рекомендуются следующие мероприятия для уменьшения проявлений ладонно-подошвенного синдрома:
• снижение дозы препарата при возобновлении лечения;
• применение кожных кремов, содержащих вазелин, ланолин или молочную кислоту.
После нанесения крема следует надеть хлопковую перчатку и/или носок (особенно на ночь), чтобы максимальное количество крема могло всосаться и кожа оставалась покрытой им.
Иногда могут рекомендоваться местные или пероральные кортикостероиды, витамин В6 (пиридоксин). Применение пиридоксина в широко варьирующей дозе от 50 до 150 мг 3 раза в сутки в течение 6 нед. может способствовать уменьшению ЛПС при лечении капецитабином (Кселода). Витамин В6 не рекомендуется применять при комбинации капецитабина с цисплатином, т.к. он может снижать эффективность последнего.
Также могут использоваться холодные ванны или прикладывание к наиболее проблемным местам пакетов с замораживающим гелем. Охлаждение ладоней и стоп уменьшает кровоток и может сделать все симптомы ладонно-подошвенного синдрома менее выраженными. Иногда помогает приподнятое (высокое) положение стоп и ладоней. При развитии ЛПС пациентам рекомендуется носить комфортную и свободную одежду и обувь, дома — домашние тапочки.
Длительное использование горячей воды для рук и ног недопустимо. Для мытья рекомендуется холодная или слегка подогретая вода. После мытья кожу следует осторожно промокать досуха, но не растирать. Все открытые участки кожи должны быть защищены от солнечных лучей при нахождении вне дома. Нельзя допускать сухости кожи на руках. Рекомендуется использовать мягкие увлажняющие средства. Должны быть также исключены все виды физической деятельности, которые могут оказывать давление на кожу или трение, включая домашнюю работу, спорт, длительные пешеходные прогулки.
Многие из токсических реакций кожи (гиперпигментация, склеротические изменения, гиперкератоз, язвы) и трофические изменения ногтей проходят самостоятельно и довольно быстро после прекращения XT. Такие изменения кожи, как гиперпигментация, гиперкератоз, как правило, отмены лечения не требуют. Поражение кожи — типичное осложнение при использовании ингибиторов EGFR (гефитиниб, эрлотиниб, цетуксимаб).
Алопеция — проявление токсического повреждения придатков кожи при использовании некоторых противоопухолевых препаратов. Это осложнение возникает в результате подавления пролиферации эпителия волосяных фолликулов. Алопеция обратима, однако является тяжелой психической травмой.
Она закономерно сопровождает химиотерапию доксорубицином, эпирубицином, этопозидом, таксанами, иринотеканом и отмечается у 10-30% больных, получающих лечение циклофосфамидом, дактиномицином, митомицином, винбластином, винкристином, VM-26, гемцитабином, цисплатином. Полное восстановление волосяного покрова головы происходит через 3-6 мес. после окончания медикаментозного лечения.
Поздние осложнения
Поздние осложнения встречаются нечасто, развиваются в течение года или более длительного периода после проведенного лечения. Наиболее опасными считаются тератогенный, канцерогенный и мутагенный эффекты как отдельных препаратов, так и их комбинаций. При длительном лечении кортикостероидами и ингибиторами ароматазы может развиться остеопороз; при лечении циклофосфамидом, ифосфамидом происходит изменение слизистой оболочки мочевого пузыря и возможно развитие опухолей. У детей при лечении циклофосфамидом, метотрексатом, дактиномицином (Актиномицин D), доксорубицином и кортикостероидами возможны нарушения роста и физического развития.
При использовании метилхлорэтиламина (Эмбихин, Мустарген), бусульфана, хлорамбуцина, циклофосфамида, ломустина, кармустина, прокарбазина бывают случаи бесплодия. Инфертильность возможна при лечении цисплатином, цитарабином, доксорубицином, этопозидом, винбластином. При планировании лечения этими препаратами может осуществляться криоконсервация спермы и ооцитов у пациентов детородного возраста при желании иметь детей после излечения.
Больные, длительно получавшие XT и/или лучевую терапию, имеют более высокий риск развития вторичных опухолей.
В поздние сроки могут развиваться стойкая цитопения, минимальная диастолическая скорость (МДС), иммуносупрессия, нарушение гонадотропной функции, кардиомиопатии, пневмопатии, ухудшение памяти, снижение ментальной функции.
Токсическое действие таргетных препаратов
Появление в онкологической практике новых противоопухолевых препаратов молекулярно-нацеленного действия (таргетных) привнесло дополнения в частоту и структуру побочных реакций. Не обладая в большинстве случаев типичной для химиотерапии токсичностью, таргетные агенты характеризуются развитием новых вариантов побочного действия.
Возникновение инфузионных реакций (как правило, при первом введении) в виде повышения температуры тела, озноба, головной боли, крапивницы, артериальной гипотензии отмечается при использовании ритуксимаба, трастузумаба, цетуксимаба, бевацизумаба. Для профилактики гиперчувствительности к чужеродным белкам применяют анти гнетами иную и кортикостероидную премедикацию.
Если инфузионная реакция легкой или умеренной степени выраженности, следует временно приостановить инфузию, использовать дексаметазон (8-12 мг), жаропонижающие и другие симптоматические средства и возобновить инфузионное введение после купирования симптомов, уменьшив скорость введения. Пациент должен быть предупрежден о возможности отсроченных реакций (до 12 ч после инфузий) и проинструктирован о необходимости обращения к врачу при их возникновении.
Дерматологические реакции, нарушения структуры ногтей достаточно часто сопровождают терапию таргетными препаратами; они, в частности, характерны для ингибиторов EGFR. Угреподобная макулопапулезная сыпь, сухость кожи, шелушение развиваются при использовании гефитиниба, эрлотиниба, цетуксимаба; сорафениб может быть причиной ладонно-подошвенного синдрома.
Большинство кожных реакций развивается в первые 3 нед. лечения, несколько раньше (7-10-й день) при использовании эрлотиниба. После стихания воспалительного компонента может развиться гипо- или гиперпигментация кожи на месте бывших высыпаний. Установлено, что дерматологическая токсичность может быть косвенным показателем эффективности при лечении эрлотинибом и, в меньшей степени, цетуксимабом.
Для профилактики и ликвидации дерматологических реакций требуется щадящий для кожного покрова режим, интенсивное увлажнение кожного покрова, местное применение противовоспалительных средств (пимекролимус, такролимус). использование одновременно с местным лечением антигистаминных препаратов, гидрокортизона; при II степени выраженности и выше назначают тетрациклины.
Токсичность со стороны желудочно-кишечного тракта (ЖКТ) (тошнота, рвота, анорексия) в незначительной степени выраженности характерна для многих таргетных препаратов, но не является лимитирующей и требует стандартных лечебных мероприятий. Диарея наблюдается при использовании эрлотиниба, гефитиниба, сунитиниба, лапатиниба; обычно имеет транзиторный характер и в большинстве случаев хорошо поддается терапии лоперамидом.
Кардиотоксичность развивается нечасто при монотерапии трастузумабом и сунитинибом (до 10% случаев). Однако риск кардиотоксичности возрастает при сочетании трастузумаба с антрациклинами и, в меньшей степени, с паклитакселом, циклофосфамидом. Умеренная артериальная гипертензия возникает на фоне лечения бевацизумабом, сорафенибом и сунитинибом.
Тщательный кардиологический мониторинг (динамика фракции выброса левого желудочка), адекватная оценка состояния сердечно-сосудистой системы и стандартная лекарственная терапия клинических проявлений кардиоваскулярной токсичности позволяют эффективно предупреждать и купировать эти токсические проявления.
Миелосупрессия отмечается в основном при сочетании таргетных агентов с цитотоксическими препаратами.
Изменения свертывающей системы в виде гипокоагуляции и развития кратковременных, преимущественно носовых, кровотечений отмечаются на фоне лечения гефитинибом, сорафенибом. Большого внимания заслуживает гиперкоагуляция с формированием тромбоэмболических осложнений при использовании бевацизумаба. Наибольший риск отмечается у больных старше 65 лет и при наличии в анамнезе артериальных тромбоэмболических осложнений.
При развитии тромбоэмболии лечение бевацизумабом прекращают, вопрос о возобновлении терапии решается индивидуально с учетом динамики клинической картины и показателей коагулограммы.
Бевацизумаб характеризуется и другими нестандартными побочными явлениями различной значимости: развитие протеинурии требует исследования функции почек, тщательного наблюдения. При развитии протеинурии IV степени (нефротический синдром) лечение бевацизумабом следует отменить.
Склонность к нарушению процесса заживления ран обусловливает соблюдение временных параметров при сочетании хирургического вмешательства с использованием бевацизумаба: лечение бевацизумабом следует начинать не ранее чем через 28 дней после операции. В случае планирования хирургического воздействия после терапии бевацизумабом необходимо временно отменить препарат; время между последним введением бевацизумаба и операцией должно составлять не менее 6 нед. При выполнении малого оперативного вмешательства лечение бевацизумабом может быть начато не ранее чем через 7 дней.
Редким (
Описаны различные редкие токсические проявления при использовании таргетных препаратов (гипотиреоз, недостаточность функции надпочечников, конъюнктивит, бессимптомное повышение активности аминотрансфераз и др.).
И.В. Поддубная, Н.Ф. Орел
Опубликовал Константин Моканов
