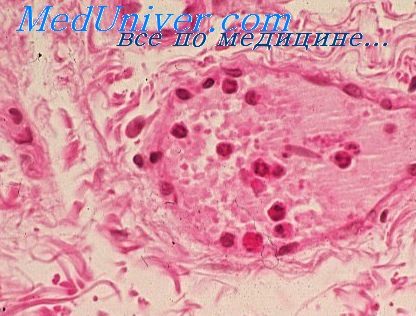
Значение иммунных процессов в воспалении

Иммунная система. ВоспалениеИммунная система и процесс воспаления участвуют в защите организма от проникающих в него микроорганизмов, отвечая на повреждение. Однако неадекватная активация этих систем приводит к широкому спектру воспалительных нарушений. Воспаление характеризуется следующими признаками: • расширением сосудов, ведущим к покраснению тканей; Физиология воспалительного процесса обладает некоторыми сходными характеристиками с физиологией повреждения. Реакции, которые они опосредуют, имеют цель обеспечить ответ организма на вторжение микроорганизмов, стресс или увеличение местного кровотока в области повреждения, обеспечивая тем самым миграцию в эту область лейкоцитов и других форменных элементов крови. Реакции обеспечивают выполнение большого количества важных процессов: возникновение боли в попытке уменьшить степень повреждения, изменение местной среды для уменьшения концентрации повреждающих веществ и миграцию лейкоцитов для уничтожения микроорганизмов.
Кроме того, многие аутакоиды, выделяемые в ответ на повреждение или инфекцию, вызывают увеличение сосудистой проницаемости, приводящее к отеку, и обеспечивают процесс регенерации и защиты ткани, который в случае неадекватности может приводить к изменению функции ткани. Ключевой дополнительной характеристикой иммунного ответа является способность лимфоцитов распознавать чужеродные белки (антигены), которые могут быть поверхностными белками на патогенах или, у некоторых людей, совершенно безвредными белками (такими как пыльца растений или чешуйки кожи животных), вызывающими аллергические реакции. Лимфоциты образуются из стволовых клеток костного мозга, затем в тимусе развиваются Т-лимфоциты, а в костном мозге — В-лимфоциты. Т-лимфоциты имеют на своей поверхности антигенные Т-клеточные рецепторы. Т-лимфоциты специфически распознают антигены, ассоциированные с главным комплексом гистосовместимости (HLA-антигены), на антигенпрезентирующих клетках — макрофагах и дендритных клетках. В случае активации Т-лимфоцитов посредством антигена через Т-клеточные рецепторы продуцируются растворимые белки, называемые цитокинами, которые передают сигнал Т-лимфоцитам, В-лимфоцитам, моноцитам/макрофагам и другим клеткам. Т-лимфоциты классифицируют на два подвида: — Также рекомендуем «В-лимфоциты. Причины начала воспаления» Оглавление темы «Препараты влияющие на иммунную систему»: |
Роль реактивности в развитии воспаления.
В зависимости от реактивности организма воспаление может быть нормергическим, гиперергическим и гипергическим.
Нормергическое воспаление — обычно протекающее, воспаление в нормальном организме
Гиперергическое воспаление — бурно протекающее, воспаление в сенсибилизированном организме. Классическими примерами являются феномен Артюса, реакция Пирке и др. Характеризуется преобладанием явлений альтерации.
Гипергическое воспаление — слабовыраженное или вялотекущее воспаление. Первое наблюдается при повышенной устойчивости к раздражителю, например, в иммунизированном организме, и характеризуется уменьшенной интенсивностью и более быстрым завершением (положительная гиперергия). Второе — при пониженной общей иммунологической реактивности (иммунодефициты, голодание, опухоли, сахарный диабет и др.) и отличается слабой динамикой, затяжным течением, задержкой элиминации флогогена и поврежденной им ткани, разрешения реакции (отрицательная гипергия).
Значение реактивности в патогенезе воспаления позволило рассматривать его как общую реакцию организма на местное повреждение.
Связь местных и общих явлений при воспалении.
Местные изменения в ткани при воспалении и механизмы, их обусловливающие, взаимосвязаны друг с другом (например, увеличение притока оксигемоглобина и повышение температуры и т.п.) и определяют приспособительное значение самого очага воспаления. Увеличение притока артериальной крови (покраснение) способствует доставке кислорода и субстратов окисления, гуморальных факторов защиты, фагоцитов в очаг воспаления.
Повышение температуры обеспечивает бактерио- и вируслитический, а также статический эффекты, активирует фагоцитоз, стимулирует обмен веществ и продукцию энергии в клетках. Ток жидкости к центру очага воспаления при усиленной экссудации препятствует резорбции инфекта и токсических агентов из очага воспаления (обеспечивает изоляцию), фагоциты и ферменты отечной жидкости местно уничтожают микроорганизмы и их токсины, очищают очаг воспаления.
Боль предупреждает чрезмерную функцию органа и ограждает его от дополнительных воздействий. Даже ограничение функции имеет приспособительный аспект; большая часть энергии в специализированных клетках идет на выполнение функции, и при ее ограничении в случае повреждения перераспределение энергии происходит в пользу пластических процессов, определяющих целостность субклеточных структур.
Вместе с тем та же активная гиперемия может приводить к разрывам сосудов и кровоизлияниям, вымыванию в общую систему кровообращения большого количества гормонов и биологически активных веществ из эндокринных органов при их воспалении (тиреотоксический криз, коллапс при остром панкреатите), интоксикации и сепсису. Локальное повышение температуры может способствовать развитию сладж-феномена и тромбозов, а чрезмерная экссудация и отек — возникновению боли и повреждению паренхиматозных клеток. Ограничение функции сердца и легких при кардитах и пневмониях может стать причиной сердечной и легочной недостаточности, угрожающих жизни.
При воспалении нет ничего местного, все — общее с местным проявлением. Такое мнение можно считать справедливым лишь частично. Местное (часть) и общее (целое) существуют объективно, и их взаимоотношение определяется диалектическими закономерностями. Воспаление возникает в ответ на патогенный фактор и местное повреждение ткани, очаг воспаления существует реально, и реакции организма как целого направлены на локализацию этого очага. Следовательно, принципиально важным необходимо считать другое: при воспалении существует и местное, и общее; местное включает общие реакции организма, которые в соответствии с его свойствами трансформируют местные явления.
Значение имунных реакций в воспалительном процессе.
Между воспалением и иммунитетом существует как прямая, так и обратная связь, так как оба процесса направлены на «очищение» внутренней среды организма от чужеродного фактора или измененного «своего» с последующим oтторжением чужеродного фактора и ликвидацией последствий повреждения. В процессе воспаления формируются иммунные реакции, а сам иммунный ответ реализуется через воспаление и от выраженности иммунного ответа организма зависит течение воспаления. Если иммунные средства защиты эффективны, воспаление может вообще не развиться. При возникновении иммунных реакций гиперчувствительности воспаление становится их морфологическим проявлением — развивается иммунное воспаление.
Иммунокомплексный вариант воспаления
Воспаление может быть ответом на образование продуктов протеолиза компонентов комплемента при активации системы комплемента при участии иммунных комплексов.
Среди таких продуктов протеолиза особое место занимают хемоаттрактанты и анафилатоксины (С3а, С4а, С5а), которые стимулируют тучные клетки и гранулоциты к дегрануляции и секреции вазоактивных медиаторов.
Анафилатоксины индуцируют секрецию медиаторов, вызывающих быстрое повышение проницаемости сосудов.
Рецепторы для С3а и С4а экспрессированы на тучных клетках, базофилах, гладко-мышечных клетках, лимфоцитах. Рецепторы для С5а экспрессированы на тучных клетках, базофилах, нейтрофилах, моноцитах/макрофагах, эндотелиальных клетках. Экспрессия С5а-рецепторов была выявлена и на эпителиальных клетках бронхов и легких, и на гладкомышечных клетках и эндотелиальных клетках сосудов легких. При связывании анафилатоксинов со специфическими для них рецепторами на базофилах и тучных клетках индуцируется экзоцитоз гранул, содержащих вазоактивные медиаторы (гистамин и др.).
Пептид С5а обладает дополнительно активностью хемоаттрактанта для гранулоцитов, которых он заставляет мигрировать строго по градиенту его концентрации. Пептид С5а стимулирует окислительный метаболизм нейтрофилов, их дегрануляцию и адгезию к эндотелию, повышая одновременно проницаемость эндотелия. Кроме того, С5а индуцирует секрецию гистамина тучными клетками (рис. 6.4).

Рисунок 6.4. Участие продуктов активации комплемента в патогенезе иммунного воспаления. Связанные с клетками антитела или иммунные комплексы могут инициировать активацию системы комплемента по классическому пути. Образующиеся при этом анафилатоксины С3а и С5а могут непосредственно вызывать дегрануляцию тучных клеток. С5а является хемоаттрактантом для нейтрофилов и обеспечивает их приток в очаг воспаления. Эти клетки секретируют активные медиаторы и разрушающие ферменты. Медиаторы влияют на функции лейкоцитов, эндотелия и гладких мышц сосудистой стенки. Ферменты вызывают повреждение тканей и активацию системы кининов. В результате повышения проницаемости сосудов развивается местный отек. Параллельно активируется система свертывания крови, что вместе с аггрегацией тромбоцитов способствует тромбозу. Продукты повреждения тканей могут усиливать активацию системы комплемента по альтернативному пути.
Сочетание этих эффектов анафилатоксинов обеспечивает аккумуляцию клеток и белков сыворотки, характерную для острого воспаления. Основными воспалительными клетками при этом являются нейтрофилы, которые очищают очаг воспаления от возбудителей и, в то же время, могут повреждать ткани организма секретируемыми продуктами: протеазами, реактивными кислородными радикалами.
Поскольку С3а пептид является хемоаттрактантом и для моноцитов/макрофагов, то продуцируемые этими клетками провоспалительные цитокины вносят свой вклад в развитие воспаления. Показана патогенетическая роль С 5а при опосредованных лейкоцитами легочных дисфункциях при остром респираторном дистресс-синдроме, бактериальных пневмониях, кистозном фиброзе, хронических заболеваниях легких.
В формирующемся на месте отложения иммунных комплексов очаге воспаления иммунных комплексов (ИК) могут связываться с воспалительными клетками через FcR или CR1 рецепторы и индуцировать местную секрецию цитокинов и вазоактивных медиаторов, которые тоже вносят свой вклад в развитие воспаления.
Для воспаления легких, опосредованного иммунными комплексами и активацией комплемента, характерно воспалительное повреждение легочной ткани. При этом последовательность событий может быть следующей: альвеолярные макрофаги активируются при воздействии иммунных комплексов через FcR и активированными компонентами комплемента через CR1, это приводит к усиленной продукции и секреции провоспалительных цитокинов TNF-a, IL-1, которые усиливают экспрессию молекул ICAM-1 и Е-селектина на сосудистом эндотелии, к которому прикрепляются нейтрофилы, и активируются при участии IL-8 и PA F из эндотелиальных клеток.
Их трансмиграция в альвеолы индуцируется С5а, который генерируется в альвеолах при взаимодействии иммунных комплексов с системой комплемента. Рекрутирование гранулоцитов из сосудов идет при участии интегринов LFA-1 и Мас-1. Активация альвеолярных макрофагов с усилением секреции TNF-a приводит к повышению экспрессии адгезионных молекул ICAM-1 на альвеолярном эпителии.
К этим адгезионным молекулам прикрепляются клетки внутри альвеол: макрофаги и нейтрофилы, которые активируются, секретируют повреждающие цитокины и ферменты. Воспалительное повреждение легких при таком типе воспаления опосредуется рекрутированными нейтрофилами.
На модели воспалительного повреждения легких после депозиции иммунных комплексов было показано, что природным регулятором воспаления служит цитокин IL-10, который способен супрессировать продукцию TNF-a, экспрессию адгезионных молекул ICAM-1 и рекрутирование нейтрофилов в очаг. За счет всех этих механизмов IL-10 уменьшает степень повреждения легких. Продукция IL-10 в легких является конститутивной, она усиливается в первые часы развития иммунокомплексного воспаления.
Иммунное воспаление — гиперчувствительность замедленного типа
Иммунное воспаление — гиперчувствительность замедленного типа (ГЗТ) представляет собой эффекторную фазу специфического клеточного иммунного ответа и включает следующие события: активацию цитокинами сосудистого эндотелия, рекрутирование моноцитов и лимфоцитов из кровяного русла и тканей в очаг ГЗТ, активацию функций макрофагов лимфокинами в очаге гиперчувствительности замедленного типа, элиминацию причинного антигена путем очищения очага ГЗТ от возбудителей и/или повреждение тканей секретируемыми продуктами активированных макрофагов и лимфоцитов. Основными участниками иммунного воспаления являются: моноциты/макрофаги, Т-лимфоциты (ТН1) и эндотелиальные клетки (рис. 6.5).

Рисунок 6.5. Реакция гиперчувствительности замедленного типа (ГЗТ). В верхней левой части рисунка — стадия сенсибилизации при первой встрече с антигеном включает: представление антигена антиген-представляющей клеткой (АРС) Т-лимфоциту (ТН) с последующей его активацией, пролиферацией, дифференцировкой в ТН1, продукцией соответствующих цитокинов. В правой нижней части рисунка — стадия ответа на повторную встречу с тем же антигеном включает: представление антигена и его распознавание ТН1, что ведет к его активации, секреции цитокинов и активации макрофагов.
В процессе иммунного воспаления ведущую роль играют следующие цитокины: IFNy, TNF-a, TNF-в, IL-1, IL-6. В реакциях гиперчувствительности замедленного типа различают острую фазу и стадию хронического воспаления. Острая фаза по своим проявлениям сходна с ранним воспалительным неспецифическим ответом, но отличается тем, что макрофаги исходно активируются не микробными продуктами, а IFNy и другими цитокинами (MIF, GM-CSF). Продукты активированных Т-лимфоцитов IL-3, GM-CSF стимулируют и продукцию моноцитов, и их рекрутирование из кровяного русла (TNF-a, TNF-в, МСР). В результате на месте очага иммунного воспаления формируется мононуклеарный инфильтрат.
В стадии хронического воспаления те же провоспалительные цитокины (IL-1, IL-6, TNF-a) стимулируют пролиферацию фибробластов и синтез коллагена как непосредственно, так и через индукцию каскада других цитокинов: PDGF, TGFp, FGF, которые в совокупности еще усиливают ангиогенез.
Сочетанный эффект перечисленных медленно действующих цитокинов и ростовых факторов при длительной неконтролируемой активации макрофагов в очаге хронического иммунного воспаления ведет к замещению тканей органов (в том числе легких) фиброзной тканью. Фиброз, как правило, сопутствует хроническому иммунному воспалению, приходящему на смену неэффективному острому воспалению, которое не привело к элиминации причинного антигена.
При хроническом течении воспаления с персистенцией сдвигов сывороточных белков, описанных выше в связи с ранним воспалительным ответом, повышенный уровень сывороточного амилоида А может вести к его отложению в интерстициальной ткани в форме фибрилл. Развивается амилоидоз, нарушающий жизненно важные функции.
При ГЗТ активированные макрофаги постепенно претерпевают ряд изменений: увеличиваются в размерах, приобретают морфологию «эпителиоидных» клеток или сливаются, образуя многоядерные гигантские клетки. Такие активированные видоизмененные макрофаги собираются в конгломераты вокруг антиген-содержащих частиц или клеток. Образуется узел воспалительной ткани — гранулема. Гранулема — это характерный ответ в виде хронической формы ГЗТ на длительно персистирующую в ткани микробную инфекцию, например, при туберкулезе или микозах, которые препятствуют распространению инфекции. Исходом гранулемы может быть деструкция ткани вплоть до некроза с последующим фиброзом.
Проникающий через респираторный тракт Cryptococcus neoformans в случаях недостаточно эффективного раннего воспалительного ответа не вычищается из ткани легкого и вызывает персистирующую хроническую инфекцию. В этих случаях защитную роль берет на себя Т-клеточный ответ, эффективность которого во многом зависит от вирулентности возбудителя. Высоковирулентные штаммы гриба вырабатывают меланин, который является скавенджером для свободных радикалов и тем самым защищает возбудителя от антимикробного действия супероксидных и нитроксидных радикалов.
При высоком уровне продукции меланина возбудитель индуцирует минимальный воспалительный ответ в легких, отсроченный и неэффективный. В этом случае снижена продукция TNF-a альвеолярными макрофагами и снижен про-лиферативный ответ Т-лимфоцитов. Дефектность клеточного иммунного ответа на меланин-продуцирующие штаммы гриба проявляется низким содержанием в легких СD4+Т-клеток, минимальным рекрутированием воспалительных клеток, сниженной активацией макрофагов, сниженным очищением легких, повышенной диссеминацией гриба в центральную нервную систему, минимальной выраженностью обоих типов ответа: ТН1 и ТН2.
В генезе индуцированной туберкулезным антигеном в ткани легкого гранулемы ведущую роль играют IFNy и TNF-a. Эти два цитокина обеспечивают максимальную выраженность местного воспаления за счет усиления экспрессии адгезионных молекул и хемокинов, необходимых для рекрутирования моноцитов/макрофагов в очаг воспаления. К тому же IFNy активирует функции макрофагов и способствует дифференцировке ТН1 лимфоцитов в региональных лимфоузлах, а также может усиливать адгезию лимфоцитов к эндотелию при их рекрутировании.
Активированные макрофаги продуцируют не только провоспалительные цитокины, но и противовоспалительные, в том числе IL-10. Этот цитокин ингибирует генерацию ТН1 лимфоцитов в региональных лимфоузлах, ингибирует их активность, препятствует формированию гранулемы и тем самым способствует диссеминации инфекции.
Результатом ГЗТ в респираторном тракте может быть развитие эксудативного воспаления и аккумуляция лейкоцитов в просвете дыхательных путей. Экссудация — выход плазмы через ткани дыхательных путей в просвет — происходит в два этапа. Сначала белки плазмы выходят из мелких сосудов через эндотелий в интерстициальную ткань. Трахео-бронхиальные микрососуды образуют густую сеть в подслизистой и проявляют очень высокую чувствительность к действию провоспалительных медиаторов.
Далее жидкость преодолевает слой эпителия и поступает в просвет дыхательных путей, откуда она может удаляться механизмами очищения. Эффекторная фаза легочной реакции ГЗТ, как правило, достигает максимума через 24 часа после повторной встречи с антигеном и проявляется накоплением в просвете жидкости, гранулоцитов и моноцитов, рекрутированных из кровяного русла.
При системной гранулематозной болезни легких — саркоидозе иммуно-гистологическими исследованиями показано совместное отложение в гранулемах фибрина и цитокина IL-1в. Высказано предположение, что в очаге хронического воспаления, где условия способствуют коагуляции и аккумуляции фибрина, взаимодействие между мононуклеарами и фибриновым матриксом ведет к продукции IL-1в.
Федосеев Г.Б.
Опубликовал Константин Моканов